Des chercheurs de l’Unité Mixte de Recherche 1190 «Recherche Translationnelle sur le Diabète» (Université de Lille – Inserm – CHRU de Lille) dirigée par le Pr Pattou, viennent d’expliquer le mécanisme physiologique par lequel la chirurgie de l’obésité dite «bypass» gastrique améliore le diabète de type 2. D’un point de vue plus général, leur découverte tend à démontrer que de simples mesures diététiques mimant l’effet de la chirurgie, comme la diminution de l’ingestion simultanée de sel et de sucre, pourraient contribuer à prévenir le diabète. Ces travaux sont publiés dans la revue Cell Metabolism.
(c) François Pattou/ Inserm
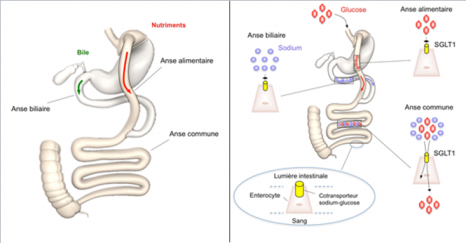
Fig. 2 : Le glucose est absorbé uniquement lorsqu’il entre en contact de la bile et du sel qu’elle contient
Depuis sa recommandation par la Haute Autorité de Santé en 2009, la chirurgie bariatrique a été réalisée chez plus de 200 000 français atteints d’obésité sévère. Chez les patients présentant également un diabète de type 2, la dérivation de l’estomac, appelée bypass gastrique (voir Fig.1 pour schéma de l’intervention) entraîne aussi une diminution rapide du taux de sucre dans le sang (glycémie). Une fois opérés, de nombreux patients peuvent diminuer voire interrompre leurs médicaments antidiabétiques, avant même avoir perdu du poids. Les mécanismes de cet effet spectaculaire de la chirurgie sur le diabète restent mystérieux. Leur compréhension est cependant essentielle. Au-delà de la chirurgie, l’élucidation des liens unissant l’intestin, l’alimentation et l’équilibre glycémique pourrait ouvrir de nouvelles perspectives pour la prise en charge du diabète de type 2, une maladie qui frappe 5% des français et plus de 300 millions de personnes dans le monde. Ce sujet fait donc l’objet depuis une décennie d’intenses recherches dans le monde. Plusieurs mécanismes complexes ont déjà été suggérés, impliquant le rôle de signaux sanguins ou nerveux induits par la chirurgie et modulant la sécrétion d’insuline ou l’utilisation du sucre par les tissus cibles.
Aucun de ces travaux, réalisés le plus souvent chez le rongeur, ne permet cependant d’expliquer de façon satisfaisante l’ensemble des résultats observés chez l’homme. Sur le site du campus Hospitalier et Universitaire lillois, l’Unité Mixte de Recherche 1190 «Recherche Translationnelle sur le Diabète» dirigée par le Pr François Pattou (Université de Lille – Inserm – CHRU de Lille), une équipe du LABEX European Genomic Institute for Diabetes (Egid) avec les équipes médicales du CHRU de Lille se sont penchées sur la question. Grâce à la disponibilité de patients volontaires, ces chercheurs ont d’abord observé que le bypass gastrique limitait l’absorption des sucres ingérés, et par conséquent l’élévation de la glycémie après le repas. Pour expliquer ces résultats, ils ont ensuite étudié les conséquences de l’opération chez le miniporc, un mammifère omnivore, dont l’anatomie et la physiologie digestives sont très proches de celles de l’homme. Le 25 février, ils rapportent dans un article publié par la revue Cell Metabolism des résultats inattendus.
Les chercheurs lillois ont en effet mis en évidence un mécanisme tout simple : après un bypass gastrique, le sucre ingéré n’est plus absorbé que dans la partie basse de l’intestin, lorsqu’il entre en contact avec la bile. De plus, cet effet de la bile est annulé en présence de phlorizine, un inhibiteur de l’absorption du glucose, naturellement contenu dans l’écorce de pommier . Enfin, l’addition de sodium (sel) au repas, a suffi aux chercheurs pour restaurer l’absorption du sucre dans la partie haute de l’intestin, et accroître le taux de sucre postprandial chez les animaux opérés. Profitant du contexte anatomique particulier du bypass gastrique, les chercheurs soulignent ainsi l’influence essentielle du sodium sur l’absorption intestinale du glucose. Ils ont aussi démontré que c’est le sodium endogène, excrété dans la bile et les secrétions digestives, qui assure la majorité de l’absorption physiologique du glucose par l’intestin.
La diminution sélective de l’absorption du glucose par l’intestin, n’est sans doute pas pas la seule explication des résultats spectaculaires du bypass gastrique. Ainsi, la perte de poids et la diminution de l’appétence pour les aliments sucrés semblent aussi jouer un rôle important pour le maintien au long cours des résultats.
L’hypothèse des chercheurs lillois réconcilie cependant la théorie et la clinique, en expliquant plusieurs observations jusque là incomprises, comme la diminution immédiate du taux de sucre après un repas chez les patients diabétiques opérés, ou la meilleure efficacité des interventions réduisant le plus la longueur d’intestin fonctionnel. Plus généralement, ces résultats confirment aussi l’influence du contenu en sel des repas sur l’élévation de la glycémie, récemment illustrée chez des individus sains, par une étude israélienne (Zeevi et al. Cell 2015). Les chercheurs lillois concluent d’ailleurs leurs travaux en soulignant l’intérêt de prévenir ou traiter le diabète en modulant l’absorption intestinale du glucose par des mesures diététiques (par la diminution de l’ingestion simultanée de sel et de sucre) ou pharmacologiques (à l’aide de molécules inhibant sélectivement le transporteur sodium-glucose intestinal, dont les premières résultats chez l’homme semblent prometteurs).
Ces travaux ont été possible grâce au soutien financier de : Fondation de l’Avenir (ET2-665) ; Fondation Francophone pour le Recherche sur le Diabète ; European Genomic Institute for Diabetes (ANR-10-LABX-46) ; Conseil Régional Nord-Pas de Calais-Picardie et Commission Européenne (ERDF CARDIO-DIABETES 12003944).
La mission principale de la Fédération de Recherche Egid (Université de Lille – CNRS – CHRU de Lille – Institut Pasteur de Lille), Institut européen de génomique sur le diabète, qui a obtenu un Labex dans le cadre du Programme d’Investissements d’Avenir, est d’identifier les facteurs de risque du diabète et de l’obésité et de mieux comprendre les mécanismes d’apparition de leurs complications afin de prévenir plus efficacement leur survenue et de mieux traiter les patients. Cette Fédération de Recherche Egid est constituée de trois équipes fondatrices:
- l’UMR 1011 « Récepteurs nucléaires, maladies cardiovasculaires et diabète» dirigée par le Pr Bart Staels (Université de Lille, Institut Pasteur de Lille, Inserm),
- l’UMR 1190 « Recherche translationnelle sur le diabète » dirigée par le Pr François Pattou (Université de Lille, Inserm, CHRU de Lille),
- et l’UMR 8199 « Génomique intégrative et modélisation des maladies métaboliques» dirigée par le Pr Philippe Froguel (Université de Lille, CNRS, Institut Pasteur de Lille, CHRU de Lille