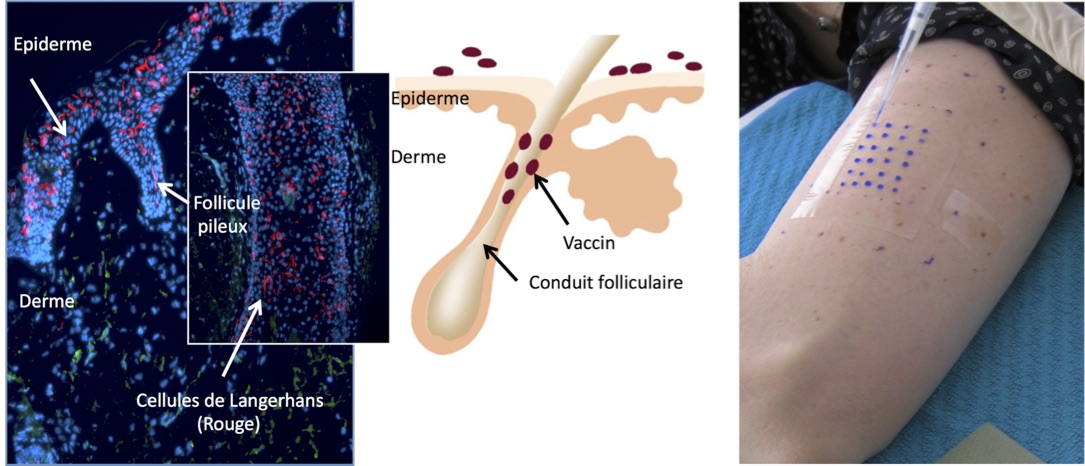
Vaccins par voie transcutanée passant par le follicule pileux. © Behazine Combadière (Inserm), Annika Vogt (Charité)
Combiner plusieurs voies d’administration vaccinales permet d’obtenir une meilleure réponse immunitaire. C’est ce que révèle une récente étude menée dans le cadre du projet CUT’HIVAC que Béhazine Combadière, directrice de recherche à l’Inserm au Centre d’immunologie et de maladies infectieuses (CIMI-Paris, Inserm/ Université Pierre et Marie Curie/ CNRS) coordinatrice au niveau Européen. Ces travaux ouvrent de nouvelles perspectives à la vaccination « personnalisée » permettant d’adapter la réponse immunitaire à l’infection. Les travaux effectués dans le cadre d’un candidat vaccin ADN contre le VIH sont parus dans Scientific Reports en octobre 2017.
Depuis la mise au point du tout premier vaccin contre la variole au XVIIIème siècle à aujourd’hui, une vingtaine de vaccins ont été créés. De nos jours, les chercheurs du monde entier travaillent dans l’élaboration de nouveaux vaccins capables d’éradiquer certains virus encore responsables de plusieurs milliers de morts tels que le virus de l’immunodéficience humaine (VIH) ou plus récemment, Zika ou Ebola.
En se basant sur la capacité innée qu’ont les êtres humains de développer des réponses immunitaires « mémoires », le vaccin consiste à administrer à un individu une forme atténuée ou inactivée d’un agent infectieux. Les vaccins peuvent être mis en contact avec l’organisme via différentes voies d’administration. Aujourd’hui, la vaccination se fait essentiellement par la voie intramusculaire ou sous cutanée. La recherche étudie actuellement une nouvelle voie appelée transcutanée, à travers la peau, encore au stade d’essais cliniques. Cette voie est rarement utilisée comme site d’injection car elle demande une technicité importante. Elle a pour avantages d’utiliser des doses faibles et de se faire sans aiguille, via le dépôt du vaccin dans le conduit des follicules pileux.
Dans le cadre d’un projet collaboratif appelé CUT’HIVAC (acronyme pour “Cutaneous and Mucosal HIV vaccination”), Béhazine Combadière accompagnée d’autres chercheurs, tentent de développer de nouveaux vaccins notamment contre le VIH. Ils étudient entre autres la qualité des réponses immunitaires induites en fonction des différentes voies d’administration du vaccin, dont la voie transcutanée. L’injection transcutanée a également ciblé plus particulièrement les cellules de Langerhans, présentatrices d’antigènes situées dans l’épiderme et qui jouent un rôle fondamental dans l’initiation d’une bonne réponse immune de type cellulaire.
Trois groupes de sujets sains ont ainsi été formés :
- le 1er premier groupe de patients a reçu une vaccination par associant une injection intramusculaire et intradermique,
- le 2ème groupe s’est vu administrer un vaccin combinant une intramusculaire et une transcutanée,
- enfin, le 3ème groupe a reçu une injection IM administrée avec électroporation, technique utilisée en microbiologie visant à rendre une membrane cellulaire plus perméable, en l’occurrence ici à l’ADN présent dans le vaccin, en lui appliquant un champ électrique d’une milliseconde.
Ces récents travaux mettent en évidence que le groupe ayant reçu l’injection intramusculaire couplée à une électroporation, obtient la réponse immunitaire la plus forte en produisant beaucoup d’interférons (cytokines sécrétées par le système immunitaire) contrairement aux autres groupes. Mais cette réponse, bien que forte n’est pas de qualité suffisante. De façon intéressante, le groupe ayant reçu une injection transcutanée présente une réponse immunitaire produisant une variété de cytokines reflétant une qualité meilleure de la réponse immunitaire.
Bien que préliminaires, ces résultats offrent de nouvelles perspectives pour l’élaboration d’une immunité cellulaire différentielle, exigée pour combattre la vaste gamme de maladies infectieuses et des tumeurs. En combinant plusieurs voies d’administration, on parvient à la meilleure réponse immunitaire, plus spécifique, qui pourrait s’adapter à n’importe quelle infection. « Ces résultats sont encourageants car ils contribuent à faire avancer la recherche sur les vaccins à ADN, notamment celui pour le VIH. L’étape suivante sera de déterminer si cette approche vaccinale peut modifier les réponses immunitaires des individus infectés par le VIH » selon les chercheurs qui ont mené l’étude.
Le projet CUT’HIVAC, a reçu les financements de l’Union Européenne à travers le programme FP7, collaboration internationale impliquant des groupes de recherche situés au Royaume-Uni, en Allemagne, en France et dans deux biotechs.
Ces contenus pourraient aussi vous intéresser :
- Imperial College London, Department of Medicine, Section of Virology, Group of Mucosal Infection and Immunity, London, United Kingdom.
- FIT Biotech Ltd., Tampere, Finland.
- Ichor Medical Systems Inc, San Diego, CA, United States.
- Human Immunology Laboratory, International AIDS Vaccine Initiative, London, United Kingdom.
- Clinical Research Center for Hair and Skin Science, Department of Dermatology and Allergy, Charité – Universitätsmedizin Berlin, Charitéplatz 1, 10117, Berlin, Germany.
- Medical Research Council Clinical Trials Unit at UCL, University College London, London, UK.
- Sorbonne Universités, UPMC Univ Paris 06, INSERM, U1135, CNRS, ERL 8255, Centre d’Immunologie et des Maladies Infectieuses (CIMI-Paris), 91 Boulevard de l’Hôpital, F-75013, Paris, France.