Contact scientifique
Alexandre Benani
Chercheur CNRS
T +33 3 80 68 16 27
Contact Presse
Presse CNRS Véronique Etienne T +33 1 44 96 51 37 rf.srnc@enneite.euqinorevPresse CNRS
Véronique Etienne
T +33 1 44 96 51 37
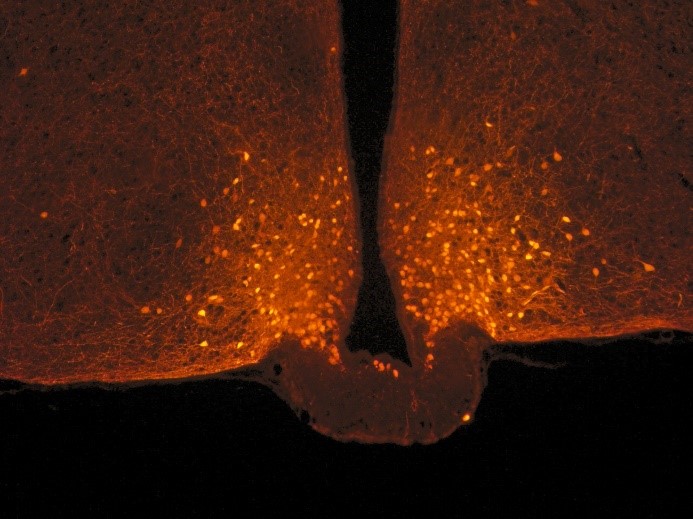
Neurones POMC (points oranges) dans l’hypothalamus, à la base du cerveau. Photo acquise chez la souris avec un microscope confocal.© Danaé Nuzzaci / CNRS / CSGA
Vous venez de terminer un bon repas et vous vous sentez repu ? Des chercheurs du CNRS, de l’Inserm, d’Inrae, de l’Université de Bourgogne, d’Université de Paris et de l’Université du Luxembourg1 viennent de comprendre les mécanismes qui, dans votre cerveau, ont conduit à cet état. Il s’agit d’une cascade de réactions déclenchée par l’élévation du taux de glucose dans le sang. Cette étude, menée chez la souris, est publiée dans Cell Reports le 3 mars 2020.
Les circuits de neurones qui gouvernent les sensations de faim et de satiété dans notre cerveau ont la capacité de modifier leurs connexions, ce qui permet d’ajuster le comportement alimentaire aux conditions de vie et de maintenir un équilibre entre apports et dépenses énergétiques. Les scientifiques soupçonnent d’ailleurs que cette plasticité pourrait être altérée chez les sujets obèses.
Dans une nouvelle étude menée chez la souris, une équipe dirigée par Alexandre Benani, chercheur du CNRS au Centre des sciences du goût et de l’alimentation (CNRS/Inrae/Université de Bourgogne/ AgroSup Dijon) montre que ces circuits sont activés à l’échelle d’un repas, ce qui contribue à la régulation du comportement alimentaire. Mais cette activation ne passe pas par un changement dans les « branchements » du circuit.
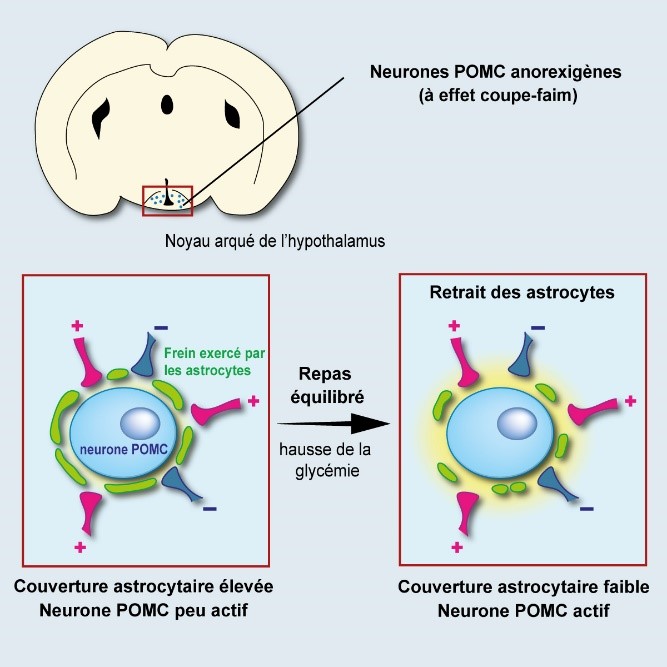
Remodelage du circuit de la satiété des neurones POMC après un repas équilibré. Encadré rouge : zone correspondant à la photo de droite.© Alexandre Benani / CNRS / CSGA
Les astrocytes sont des cellules nerveuses en forme d’étoiles, d’abord décrites pour leur rôle de support des neurones. Dans les conditions habituelles, ils recouvrent étroitement les neurones POMC et agissent un peu à la manière de plaquettes de frein, limitant leur activité. Après un repas, le taux de glucose dans le sang (glycémie) s’élève transitoirement et ce signal est ressenti par les astrocytes qui se rétractent en moins d’une heure. Le « frein » étant levé, les neurones POMC se trouvent activés, ce qui favorise in fine le sentiment de satiété.
De manière étonnante, un repas riche en graisses n’induit pas ce remodelage. Est-ce à dire que les lipides sont moins efficaces pour couper la faim ? Les scientifiques cherchent à déterminer s’ils ne déclencheraient pas la satiété par un autre circuit. Il reste aussi à savoir si les édulcorants ont les mêmes effets ou s’ils sont de véritables leurres pour le cerveau, qui ne procurent que la sensation sucrée addictive sans couper la faim.
1 L’étude a été menée au Centre des sciences du goût et de l’alimentation (CNRS/Inrae/Université de Bourgogne/Agrosup Dijon), en étroite collaboration avec des collègues de l’Institut de pharmacologie moléculaire et cellulaire (CNRS/Université Côte d’Azur), de l’Institut de génomique fonctionnelle (CNRS/Inserm/Université de Montpellier) et de l’Université du Luxembourg, et avec les contributions de l’Unité de biologie fonctionnelle et adaptative (CNRS/Université de Paris) et de l’Institut de psychiatrie et de neuroscience de Paris (Inserm/Université de Paris).
Alexandre Benani
Chercheur CNRS
T +33 3 80 68 16 27
Presse CNRS Véronique Etienne T +33 1 44 96 51 37 rf.srnc@enneite.euqinorevPresse CNRS
Véronique Etienne
T +33 1 44 96 51 37
Postprandial hyperglycemia stimulates neuroglial plasticity in hypothalamic POMC neurons after a balanced meal
Danaé Nuzzaci, Céline Cansell, Fabienne Liénard, Emmanuelle Nédélec, Selma Ben Fradj, Julien Castel, Ewout Foppen, Raphael Denis, Dominique Grouselle, Amélie Laderrière, Aleth Lemoine, Alexia Mathou, Virginie Tolle, Tony Heurtaux, Xavier Fioramonti, Etienne Audinat, Luc Pénicaud, Jean-Louis Nahon, Carole Rovère, Alexandre Benani, Cell Reports, le 3 mars 2020.
DOI : 10.1016/j.celrep.2020.02.029Postprandial hyperglycemia stimulates neuroglial plasticity in hypothalamic POMC neurons after a balanced meal, Danaé Nuzzaci, Céline Cansell, Fabienne Liénard, Emmanuelle Nédélec, Selma Ben Fradj, Julien Castel, Ewout Foppen, Raphael Denis, Dominique Grouselle, Amélie Laderrière, Aleth Lemoine, Alexia Mathou, Virginie Tolle, Tony Heurtaux, Xavier Fioramonti, Etienne Audinat, Luc Pénicaud, Jean-Louis Nahon, Carole Rovère, Alexandre Benani, Cell Reports, le 3 mars 2020. DOI : 10.1016/j.celrep.2020.02.029