En raison des dérèglements climatiques, la population mondiale est exposée à des températures de plus en plus élevées et à des vagues de chaleur de plus en plus extrêmes. Or, au cours de la grossesse, l’exposition à la chaleur peut être nocive pour la santé des femmes enceintes et des enfants à naître. Des scientifiques de l’Inserm, de l’Université de Grenoble Alpes, en collaboration avec Santé publique France, ont étudié, sur près de 21 000 femmes enceintes, l’impact de la chaleur, couplé à celui de la pollution de l’air, de la proximité d’espaces verts et de facteurs socio-économiques, sur le poids de naissance en France. Leurs résultats, parus dans Environmental Science & Technology, soulignent comment l’exposition à la chaleur en début de grossesse, modulée par ces autres facteurs, pourrait avoir un impact significatif sur le poids des nouveau-nés en favorisant les petits poids de naissance.
Les études scientifiques sont de plus en plus nombreuses à suggérer que des températures élevées pourraient augmenter les risques périnataux tels qu’un faible poids de naissance (inférieur à 2,5 kg), une naissance prématurée (avant 37 semaines d’aménorrhée), voire une mortalité néonatale. En 2020, environ 15 % des nouveau-nés dans le monde présentaient un petit poids à la naissance.
Les études se sont jusqu’à présent concentrées sur l’étude de l’effet d’un seul facteur environnemental (température, pollution, …) sur le poids de l’enfant à la naissance. Ainsi, l’effet de la chaleur n’avait été étudié que seul et sans prendre en compte le rôle de la pollution atmosphérique, de la présence d’espaces verts ou encore des facteurs de stress sociaux (position sociale individuelle et contexte socioéconomique de résidence).
Une équipe de recherche menée par Johanna Lepeule, directrice de recherche Inserm, au sein de l’Institut pour l’Avancée des Biosciences (Inserm/CNRS/Université Grenoble Alpes), et Mathilde Pascal, chargée de projet à Santé publique France, s’est intéressée à l’identification de périodes précises de la croissance fœtale durant lesquelles l’exposition maternelle à la chaleur pourrait avoir un effet significatif sur le futur poids de naissance de l’enfant. L’étude visait également à explorer comment la pollution atmosphérique (particules fines PM2.5, dioxyde d’azote et ozone), la densité de végétation et les facteurs de stress sociaux pourraient eux-mêmes moduler les effets de la chaleur sur le poids de naissance.
En s’appuyant sur les données de quatre cohortes mères-enfants françaises pilotées ou co-pilotées par l’Inserm[1], les chercheuses et chercheurs ont étudié l’exposition à ces facteurs de 21 000 participantes enceintes, recrutées entre 2002 et 2017 et suivies tout au long de leur grossesse, et son impact sur le poids de naissance des bébés.
Les résultats mettent en évidence des périodes critiques de la grossesse durant lesquelles l’exposition à une chaleur modérée, sévère ou extrême présentait un effet significatif sur le poids de naissance des enfants. Ainsi, l’exposition à la chaleur pendant les deux premiers trimestres de la grossesse apparaissait significativement associée à un poids de naissance réduit de -40 à -200 g. A contrario, l’exposition à la chaleur vers la fin de la grossesse (semaines 32 à 35) apparaissait, elle, associée à une augmentation d’environ 60 g du poids de naissance.
Nos résultats viennent appuyer les études existantes montrant un rôle potentiel de l’exposition à la chaleur dans la survenue de faibles poids de naissance. Étudier ces liens entre chaleur et poids de naissance est particulièrement important dans le contexte actuel de dérèglement climatique, car les études montrent qu’un faible poids de naissance est un facteur de risque de complications, voire de mortalité chez le nouveau-né, mais également de survenue de pathologies tout au long de la vie comme le diabète ou l’hypertension.
Lucie Adélaïde, épidémiologiste à l’Inserm et co-première autrice de ces travaux.
Enfin, lorsque l’exposition à la pollution, la présence de végétation et les facteurs de stress sociaux étaient pris en compte, l’étude montre que ces facteurs moduleraient l’impact de l’exposition à la chaleur sur le poids de naissance. Les résultats suggèrent ainsi que ces effets pourraient être plus marqués chez les femmes vivant dans des zones avec peu d’espaces verts et/ou soumises à un stress social accru.
C’est la première fois qu’une étude prend en compte le rôle de ces différents facteurs dans les effets de la chaleur sur le poids de naissance. Nos résultats soulignent l’importance de mettre en place des mesures ciblées pour protéger les femmes enceintes et l’enfant à naître dès le début de grossesse, notamment par la végétalisation des environnements de vie qui permettent de réduire l’exposition à la chaleur.
Maximilien Génard-Walton, chercheur post-doctorant à l’Inserm et co-premier auteur de la publication.
[1] Les cohortes Pélagie, pilotée par l’Inserm ; Eden, pilotée par l’Inserm, le CHU de Poitiers et le CHU de Nancy ; Sepages, pilotée par l’Inserm et le CHU Grenoble Alpes et Elfe, pilotée par l’Inserm et l’Institut national d’études démographiques (Ined).


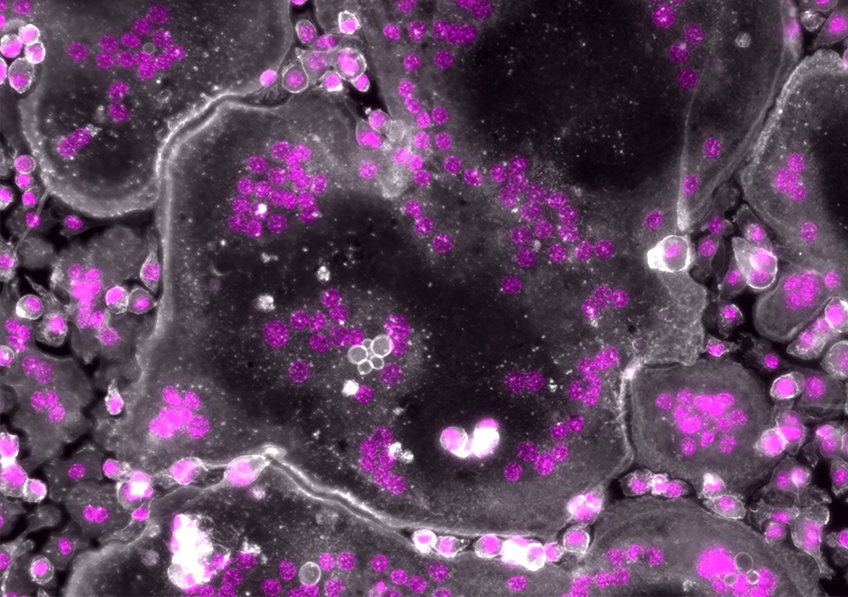
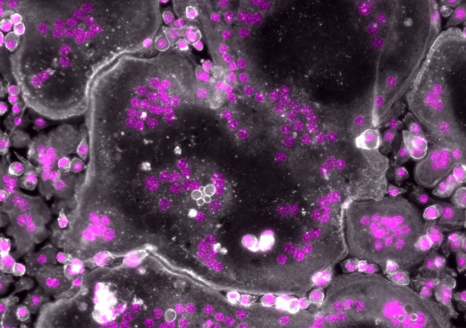 En l’absence de moésine, les ostéoclastes humains présentent des noyaux surnuméraires (en rose). L’actine est représentée en blanc. – Microscopie à fluorescence © Ophélie Dufrançais
En l’absence de moésine, les ostéoclastes humains présentent des noyaux surnuméraires (en rose). L’actine est représentée en blanc. – Microscopie à fluorescence © Ophélie Dufrançais