La présence d’un composé présent dans les crucifères, l’indole-3-carbinol, est essentiel pour rendre efficace certains traitements contre le cancer. © Photo de Monika Borys sur Unsplash
La présence d’un composé présent dans les crucifères, l’indole-3-carbinol, est essentiel pour rendre efficace certains traitements contre le cancer. © Photo de Monika Borys sur Unsplash
C’est une vérité universellement reconnue que les légumes sont bons pour la santé. Une étude menée par l’Institut Curie et l’Inserm révèle que la présence d’un composé présent dans les crucifères, l’indole-3-carbinol, est essentiel pour rendre efficace certains traitements contre le cancer. Les chercheurs mettent également en évidence les mécanismes biologiques en jeu et expliquent comment l’absence d’indole-3-carbinol induit un dysfonctionnement au niveau des lymphocytes T cytotoxiques et diminue l’efficacité de l’immunothérapie. Illustrant l’importance de comprendre les relations entre nutrition et immunité, ces résultats sont publiés dans Nature Communications le 2 décembre 2025.
« Nous savons aujourd’hui que la réponse aux traitements anticancéreux peut être influencée par de nombreux facteurs environnementaux, comme la nutrition. Il a notamment été montré que la composition du microbiote intestinal, elle-même modulée par notre alimentation, joue un rôle dans l’efficacité de certains traitements d’immunothérapie (par inhibiteur de point de contrôle immunitaire anti-PD1). Et c’est précisément ce lien entre nutrition et traitements anticancéreux que nous avons voulu explorer », explique le Dr Elodie Segura, directrice de recherche Inserm à l’Institut Curie (unité Immunité et Cancer).
Le rôle de l’indole-3-carbinol dans l’efficacité des traitements anti-PD1
Dans une étude menée à l’Institut Curie, le groupe du Dr Elodie Segura, directrice de recherche Inserm, s’est intéressée à un nutriment en particulier : l’indole-3-carbinol, une molécule présente en grandes quantités dans les crucifères (chou, brocolis, chou-fleur, cresson, navet, roquette, radis…). Afin d’en évaluer le rôle, les chercheurs ont comparé l’efficacité d’une immunothérapie chez des animaux ayant reçu deux régimes alimentaires différents : l’un contenant l’indole-3-carbinol et l’autre, non. Avec l’indole-3-carbinol, le traitement anticancéreux est efficace chez 50 à 60% des animaux. En revanche, lorsqu’on supprime l’indole-3-carbinol, l’efficacité du traitement diminue à 20%.
« Ces résultats nous montrent que lorsqu’on enlève ce composé présent dans les choux, il y a une diminution drastique de l’efficacité de l’immunothérapie anti-PD1 » résume le Dr Elodie Segura.
Les lymphocytes T cytotoxiques, pivot du mécanisme
On sait que les cellules cancéreuses sont capables d’inactiver les cellules du système immunitaire, évitant ainsi au cancer d’être attaqué par les cellules cytotoxiques ou « tueuses ». Or, les traitements d’immunothérapie, par inhibiteur de point de contrôle immunitaire anti-PD1, contrecarrent l’inhibition par le cancer des cellules T cytotoxiques et leur permet de se réactiver. Grâce à ce traitement, les lymphocytes T cytotoxiques qui sont réactivés deviennent capables de reconnaître les cellules tumorales et de les détruire.
Les chercheurs ont réussi à identifier les mécanismes d’action de l’indole-3-carbinol en jeu dans l’immunothérapie. Ils ont ainsi mis en évidence que l’indole-3-carbinol se fixe à un facteur de transcription appelé Aryl Hydrocarbon Receptor (AhR), notamment exprimé dans les lymphocytes T cytotoxiques[i].
En l’absence de l’indole-3-carbinol, les lymphocytes T cytotoxiques sont incapables de répondre au traitement.
« Normalement, lors d’une immunothérapie anti-PD1, les lymphocytes vont être stimulés et réactivés pour détecter les cellules tumorales. Or, en l’absence d’indole-3-carbinol dans le régime alimentaire, les lymphocytes ne sont pas capables de récupérer leurs fonctions », poursuit Elodie Segura.
« Nos travaux permettent de mieux comprendre le rôle des nutriments dans les réponses immunitaires antitumorales. Pour les patients, ces données pourraient permettre d’optimiser les régimes alimentaires afin d’assurer l’efficacité des traitements ».
Dans l’attente que ces résultats soient corroborés par des études cliniques spécifiques, les patients atteints de cancer sont encouragés à suivre les recommandations nutritionnelles et les conseils de leur médecin.
[i] Les lymphocytes T cytotoxiques, également appelés lymphocytes T CD8+ sont une catégorie de cellules immunitaires destinées à tuer des cellules cibles, telles que les cellules infectées par des virus, ou des cellules tumorales.



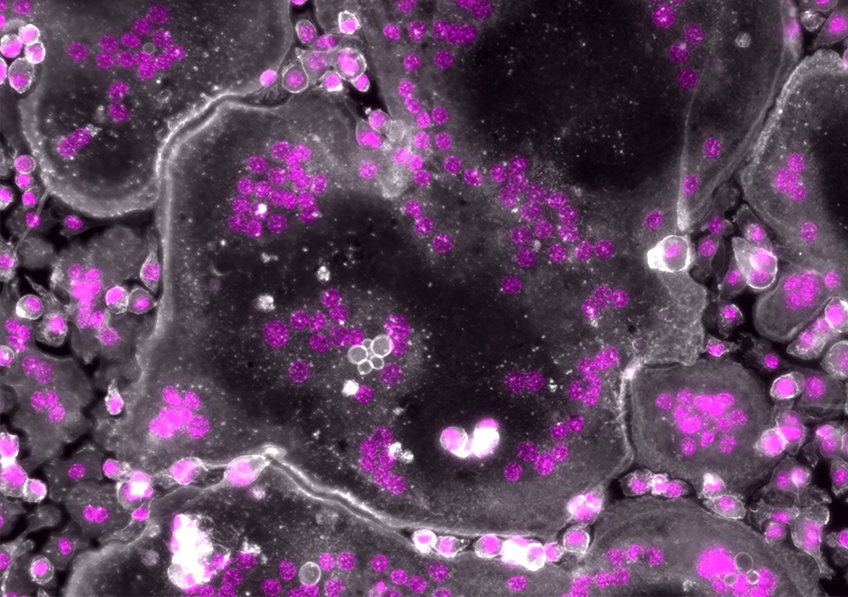
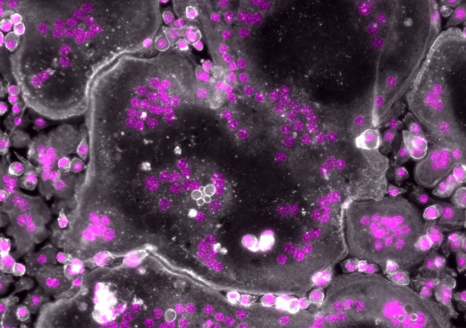 En l’absence de moésine, les ostéoclastes humains présentent des noyaux surnuméraires (en rose). L’actine est représentée en blanc. – Microscopie à fluorescence © Ophélie Dufrançais
En l’absence de moésine, les ostéoclastes humains présentent des noyaux surnuméraires (en rose). L’actine est représentée en blanc. – Microscopie à fluorescence © Ophélie Dufrançais