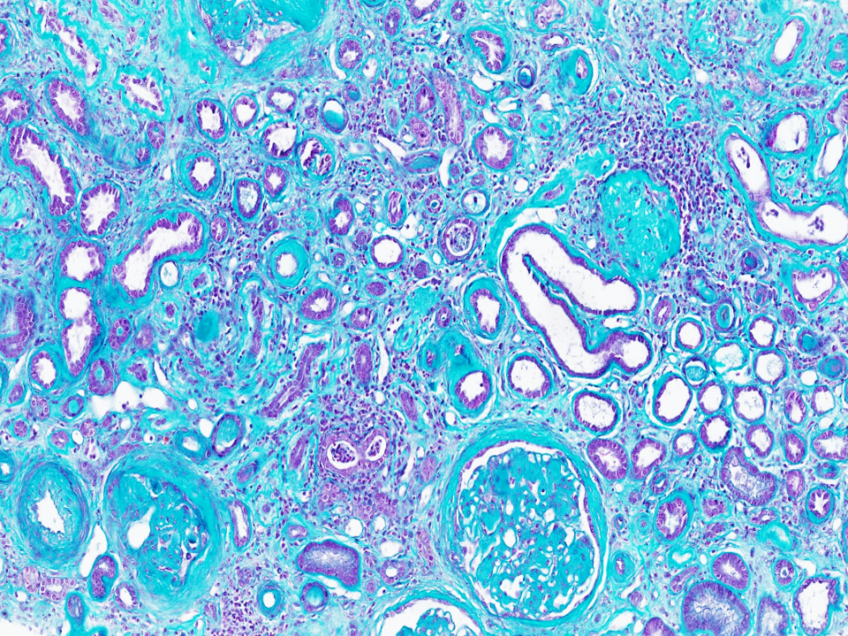
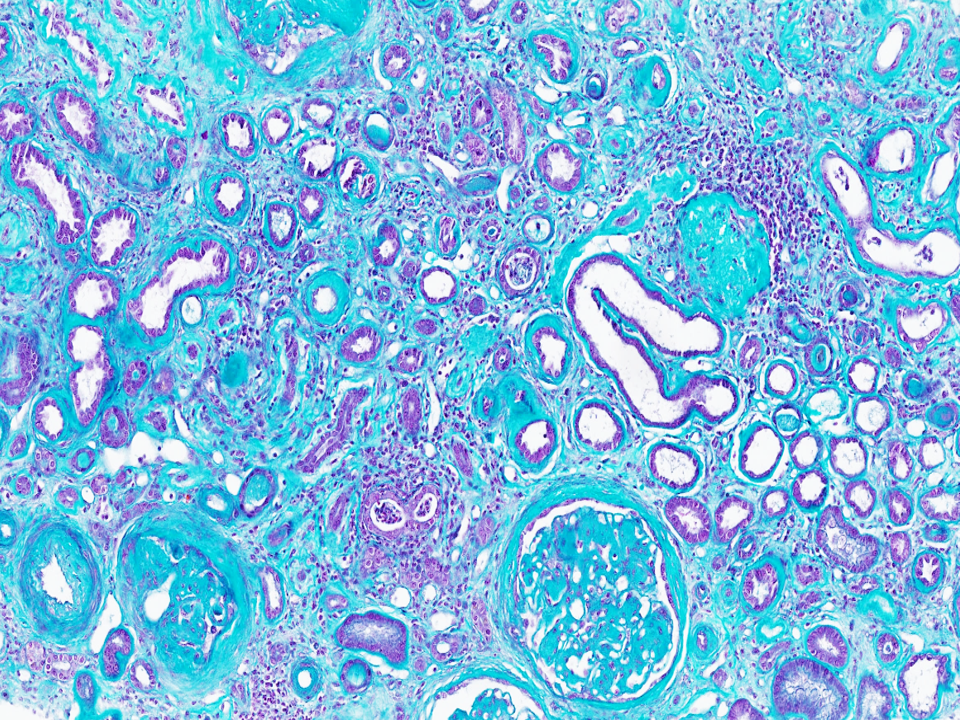
 Image de microscopie optique d’un rein de patient présentant une insuffisance rénale terminale. La fibrose interstitielle importante (collagène et tissu conjonctif fibrosé en cyan) et l’atrophie des tubules rénaux (petits canaux entourés d’une paroi épaissie en violet) témoignent d’un remplacement progressif et irréversible du tissu rénal fonctionnel par du tissu cicatriciel. Coloration : trichrome de Masson. © Fabiola Terzi, Marco Pontoglio/Inserm
Image de microscopie optique d’un rein de patient présentant une insuffisance rénale terminale. La fibrose interstitielle importante (collagène et tissu conjonctif fibrosé en cyan) et l’atrophie des tubules rénaux (petits canaux entourés d’une paroi épaissie en violet) témoignent d’un remplacement progressif et irréversible du tissu rénal fonctionnel par du tissu cicatriciel. Coloration : trichrome de Masson. © Fabiola Terzi, Marco Pontoglio/Inserm
Les maladies rénales chroniques ont un point commun : une fois amorcées, quelle qu’en soit la cause et même si celle-ci est traitée, elles finissent toujours par s’aggraver. Deux équipes de l’Inserm, du CNRS et de l’Université Paris Cité viennent de découvrir le chef d’orchestre de ce mécanisme de progression inexorable : la protéine HNF1B. Au-delà d’une avancée majeure sur le plan de la connaissance de ces maladies, les équipes ont identifié une nouvelle cible thérapeutique d’intérêt majeur. Ces travaux sont à paraître dans la revue Science.
La maladie rénale chronique touche plus de 10 % de la population mondiale, soit environ 850 millions de personnes. Elle se caractérise par une perte progressive et irréversible de la fonction rénale, pouvant nécessiter une dialyse voire une transplantation.
Plusieurs facteurs de risque sont bien identifiés : diabète, hypertension, obésité ou inflammation. Cependant, même si la cause initiale est traitée, le déclin de la fonction rénale est, dans la grande majorité des cas, inéluctable. Ce caractère auto-entretenu représente un aspect particulièrement inquiétant de la maladie rénale ; en acquérant sa propre dynamique, elle devient difficile à enrayer. Jusqu’à présent, les mécanismes biologiques responsables de cette progression continuaient de rester largement méconnus.
Deux équipes de l’Institut Necker-Enfants malades (Inserm/CNRS/Université Paris Cité) dirigées par Marco Pontoglio, directeur de recherche CNRS, et Fabiola Terzi, directrice de recherche Inserm et directrice de l’Institut Necker-Enfants malades, se sont intéressées à ces mécanismes biologiques, et plus particulièrement au rôle dans le rein adulte de la protéine HNF1B (Hepatocyte Nuclear Factor 1 beta). Elle contrôle l’expression de nombreux gènes et joue un rôle indispensable dans la formation du rein au cours du développement embryonnaire.
En effet, chez l’humain, des mutations du gène HNF1B provoquent une diminution de l’activité de cette protéine, ce qui entraîne une maladie génétique rare du rein. Et fait frappant : les lésions observées chez les patients peuvent ressembler à celles retrouvées dans les formes les plus courantes de la maladie rénale chronique, à savoir une fibrose ou encore une atrophie du tissu rénal. Cette similarité a conduit les chercheuses et chercheurs à formuler une hypothèse : le dysfonctionnement de HNF1B pourrait représenter un mécanisme commun reliant les maladies rénales rares et les formes beaucoup plus fréquentes comme la maladie rénale chronique.
Les équipes de recherche ont ainsi observé que la perte de l’activité de HNF1B dans le rein adulte humain et de souris provoquait une insuffisance rénale chronique rapide et sévère, accompagnée de fibrose et d’atrophie du tissu rénal. Privées de l’activité de HNF1B, les cellules tubulaires rénales – qui tapissent les tubules rénaux et jouent un rôle majeur dans la fonction du rein –, normalement hautement différenciées et stables, perdaient leur identité et leur spécialisation et commençaient à proliférer de façon inappropriée. Cette prolifération s’accompagnait alors de mort cellulaire ou de vieillissement prématuré des cellules, contribuant à la fibrose progressive du rein et à la dégradation de sa fonction.
Les chercheuses et chercheurs ont également identifié un ensemble de gènes dont HNF1B régule l’expression. Cet ensemble apparaissait altéré très précocement dans plusieurs modèles de maladie rénale chronique chez la souris, parfois avant même l’apparition de lésions visibles, et était associé à un défaut de réparation du tissu rénal.
Les scientifiques ont également montré que les facteurs associés à la maladie rénale, tels que l’inflammation ou la présence d’albumine[1] dans les urines, réduisaient l’activité de HNF1B. Grâce à des techniques de pointe d’analyse de l’activité des gènes, ils ont mis en évidence un phénomène clé : le stress subi par les cellules du rein lors d’une maladie rénale chronique entraîne une répression des gènes régulés par HNF1B.
« Nos résultats révèlent l’existence d’un véritable cercle vicieux qui explique le caractère auto-entretenu des maladies rénales : la diminution de l’activité de HNF1B favoriserait la maladie rénale, et en retour, la maladie rénale supprimerait progressivement l’activité de HNF1B, aggravant encore les lésions rénales. Ce mécanisme pourrait expliquer pourquoi la maladie rénale chronique à tendance à s’aggraver de façon continue, même en l’absence de nouvelle agression », résume Marco Pontoglio.
Ce mécanisme serait bien commun à de nombreuses maladies rénales. En effet, l’analyse de plus de 900 biopsies rénales de patients atteints de maladie rénale chronique de différentes origines et couvrant tous les stades de gravité, a systématiquement mis en évidence la signature moléculaire caractéristique de la perte de fonction de HNF1B.
Les anomalies étaient d’autant plus marquées que la maladie était avancée, confirmant le rôle majeur de cette protéine dans la sévérité de l’atteinte rénale. « Cette étude établit HNF1B comme un véritable gardien de la fonction du rein. Sa perte d’activité relie pour la première fois les maladies génétiques rénales rares et les formes communes de la maladie rénale chronique par un mécanisme unique », clarifie Fabiola Terzi.
Ces résultats ouvrent une nouvelle perspective thérapeutique majeure : « trouver un moyen de restaurer l’activité de HNF1B pourrait permettre de ralentir, voire de modifier l’évolution de la maladie rénale chronique » conclut Fabiola Terzi.
Ces travaux font l’objet d’un brevet déposé auprès d’Inserm Transfert en 2025.
[1] L’albumine est une protéine produite par le foie et qui circule dans le sang. Elle traverse difficilement le filtre rénal, sauf lorsque celui-ci est endommagé. Un taux élevé d’albumine dans les urines est donc révélateur d’une maladie rénale.

 Intestin de larve de poisson-zèbre montrant les cellules entéroendocrines en vert et les cellules exprimant IL-22 en magenta © Institut Curie / équipe P. Hernandez Cerda
Intestin de larve de poisson-zèbre montrant les cellules entéroendocrines en vert et les cellules exprimant IL-22 en magenta © Institut Curie / équipe P. Hernandez Cerda








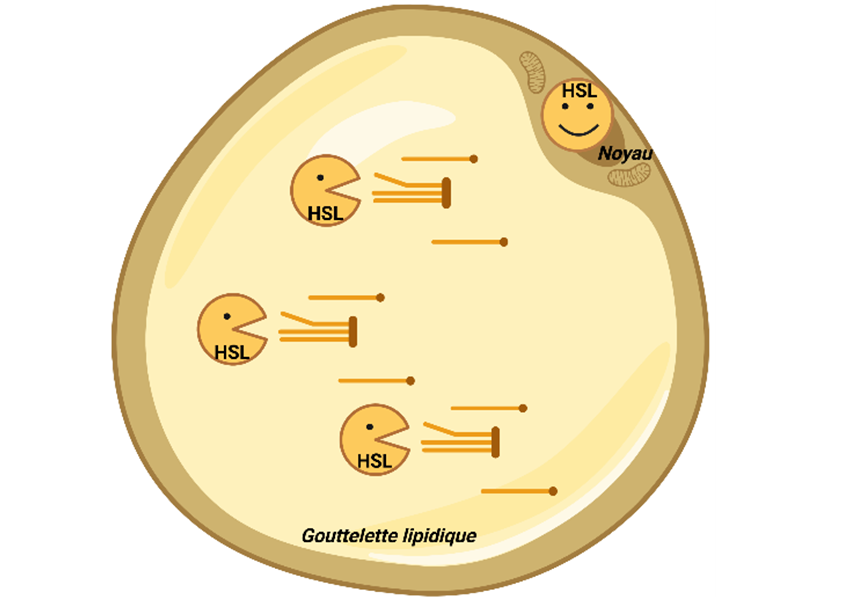
 Rôles de la HSL dans les adipocytes. La HSL participe à la mobilisation des graisses stockées dans la gouttelette lipidique. Dans le noyau, elle assure le fonctionnement harmonieux de l’adipocyte. © I2MC, 2025. Créé avec biorender.com.
Rôles de la HSL dans les adipocytes. La HSL participe à la mobilisation des graisses stockées dans la gouttelette lipidique. Dans le noyau, elle assure le fonctionnement harmonieux de l’adipocyte. © I2MC, 2025. Créé avec biorender.com.