 Lymphocyte T (bleu et jaune) interagissant avec une cellule B (en rouge) dans le cerveau d’un modèle de souris atteintes d’encéphalomyélite. © Nicolas Fazilleau// Meryem Aloulou
Lymphocyte T (bleu et jaune) interagissant avec une cellule B (en rouge) dans le cerveau d’un modèle de souris atteintes d’encéphalomyélite. © Nicolas Fazilleau// Meryem Aloulou
La sclérose en plaques (SEP) est une maladie auto-immune et inflammatoire du système nerveux central. Cela signifie que les cellules du système immunitaire s’attaquent par erreur au cerveau et à la moelle épinière, provoquant une inflammation, qu’on appelle neuro-inflammation. Comprendre les mécanismes par lesquels chacun des acteurs du système immunitaire agit dans ce contexte pathologique est un enjeu de taille pour la recherche. Dans une nouvelle étude, une équipe de recherche de l’Inserm, du CNRS et de l’université de Toulouse, regroupée au sein du laboratoire Infinity, identifie pour la première fois le rôle d’un sous type de lymphocytes T, les « Tfr régulateurs » dans l’équation. Ces cellules favorisent la migration d’autres cellules immunitaires dans le cerveau, les cellules B mémoires, responsables de la neuro inflammation et de la sévérité de la maladie. Cette découverte, réalisée à partir d’analyses du sang de patients et de modèles murins, révèle un rôle pro-inflammatoire inattendu des Tfr dans la SEP, ouvrant la voie à de nouvelles cibles thérapeutiques et biomarqueurs de l’activité de la maladie. Les résultats de cette étude sont publiés dans la revue Science Translational Medicine.
La sclérose en plaques (SEP) est une maladie qui touche le système nerveux central. Le système immunitaire du patient attaque la myéline, une gaine qui protège les fibres nerveuses, ce qui provoque des lésions et perturbe la communication entre le cerveau et le reste du corps. Cette réaction auto-immune s’accompagne d’un processus de neuro-inflammation, c’est-à-dire d’une inflammation anormale et persistante du tissu nerveux, qui contribue aux dommages neurologiques. La forme la plus fréquente de la maladie est dite rémittente-récurrente, avec des poussées[1] suivies de rémissions.
Il n’existe à ce jour pas de traitement curatif, mais des traitements de fond permettent de ralentir l’évolution de la maladie, et des soins symptomatiques aident à améliorer la qualité de vie des patients. En France, environ 120 000 personnes sont concernées, avec environ 3 000 nouveaux cas par an[2].
Comprendre les mécanismes cellulaires et moléculaires sous-jacents de cette maladie est donc un enjeu de taille pour la recherche. À Toulouse, une équipe de recherche menée par Meryem Aloulou et Nicolas Fazilleau respectivement chargée de recherche et directeur de recherche Inserm s’intéresse plus spécifiquement au rôle des cellules immunitaires dans le contexte pathologique de la SEP.
Système immunitaire et maladie auto-immune
Le système immunitaire protège l’organisme contre les agents pathogènes (comme les virus ou les bactéries) qui peuvent provoquer des maladies. Il agit par deux grands types de défense : l’immunité cellulaire, qui élimine les cellules infectées, et l’immunité humorale, qui repose sur la production d’anticorps capables de neutraliser spécifiquement ces agents étrangers.
Cette production d’anticorps est régulée par deux types de lymphocytes (ou cellules immunitaires spécialisées) : les cellules T folliculaires helpers (Tfh) et les cellules T folliculaires régulatrices (Tfr). Les Tfh stimulent la fabrication d’anticorps par d’autres cellules appelées cellules B. Tandis que les Tfr freinent ou modèrent cette production, notamment pour éviter que le système immunitaire ne s’attaque aux cellules du corps lui-même. Ces interactions ont lieu au niveau des ganglions lymphatiques.
Dans le contexte d’une maladie auto-immune, ce système est dysfonctionnel, si bien que le travail protecteur de ces lymphocytes est altéré : par un mécanisme d’interactions en cascade, les lymphocytes T et B enclenchent une inflammation en infiltrant le cerveau ce qui entraine la formation de lésions tissulaires.
Dans une nouvelle étude, l’équipe s’est intéressée au rôle des cellules T folliculaires dites régulatrices (Tfr) (encadré ci-dessus). En effet, les scientifiques ont observé la présence anormale d’une grande population de ces cellules dans le sang de patients atteints de SEP au cours d’un épisode de poussées, les mettant sur la piste du rôle des Tfr dans la neuro-inflammation caractéristique de la maladie.
Dans un modèle de souris atteintes de SEP, mais qui a la particularité de ne pas posséder de cellules Tfr, les scientifiques ont observé la présence moindre de cellules B[1], en comparaison avec un modèle porteur de Tfr. Sans l’activité des Tfr, les animaux sont atteints d’une forme plus légère de la maladie, avec moins de poussées inflammatoires.
Les chercheurs ont également identifié une molécule appelée S1PR2 à la surface des cellules B, qui est plus abondante chez les souris sans cellules Tfr. Cette molécule agit comme un frein empêchant les cellules B de quitter les ganglions lymphatiques. En l’absence de Tfr, son expression augmente, limitant le déplacement des cellules B vers le cerveau.
Ils ont ensuite décrit comment ces cellules B, une fois retrouvées dans le cerveau, contribuent à l’activation d’autres lymphocytes T responsables de l’inflammation, via la production de substances appelées cytokines pro-inflammatoires.
Ces résultats combinés suggèrent ainsi que l’activité dérégulée des Tfr favorise la neuro-inflammation épisodique (par poussées) de la sclérose en plaques. En effet, au lieu de freiner et modérer la libération des cellules B des ganglions lymphatiques, les Tfr stimulent leur activité, favorisant leur migration jusqu’au cerveau (événement à l’origine de la neuro-inflammation).
« Cette étude apporte de nouvelles connaissances sur les mécanismes en jeu dans le retournement contre soi du système immunitaire dans la SEP. Pour la première fois, nous avons identifié le rôle pro-inflammatoire des lymphocytes Tfr qui semblent favoriser l’inflammation en aidant les cellules B à atteindre le cerveau, où elles aggravent la maladie. Ces résultats apportent un éclairage nouveau sur le rôle de ces cellules et pourraient ouvrir la voie à de nouvelles approches thérapeutiques ciblant leur action. », explique Meryem Aloulou, chargée de recherche à l’Inserm, co-dernière autrice de cette étude.
« À l’avenir, nous pouvons imaginer que le suivi du niveau de Tfr dans le sang des patients pourrait être utilisé comme biomarqueur pour prédire la survenue d’une poussée. En effet, des traitements existent pour empêcher l’entrée des lymphocytes dans le cerveau, mais ils sont trop lourds pour être administrés aux patients de façon prolongée », explique Nicolas Fazilleau, directeur de recherche à l’Inserm, co-dernier auteur de cette étude.
[1] Une manifestation typique de cette affection est la poussée, un épisode marqué par l’apparition de nouveaux symptômes neurologiques ou la réapparition/aggravation de symptômes déjà présents, en lien avec une inflammation aiguë du système nerveux central.
[2] https://sante.gouv.fr/soins-et-maladies/maladies/maladies-neurodegeneratives/article/la-sclerose-en-plaques#:~:text=La%20scl%C3%A9rose%20en%20plaques%20est%20une%20maladie%20du%20jeune%20adulte,cas%20sont%20diagnostiqu%C3%A9s%20chaque%20ann%C3%A9e.
[3] Pour rappel, les cellules B ou lymphocytes B sont des éléments clefs de la réponse immunitaire humorale à l’origine de la production des anticorps.

 L’eczéma du nourrisson se manifeste par des démangeaisons intenses et des rougeurs sur le visage, le cou ou le ventre (image d’illustration). © Adobe stock
L’eczéma du nourrisson se manifeste par des démangeaisons intenses et des rougeurs sur le visage, le cou ou le ventre (image d’illustration). © Adobe stock



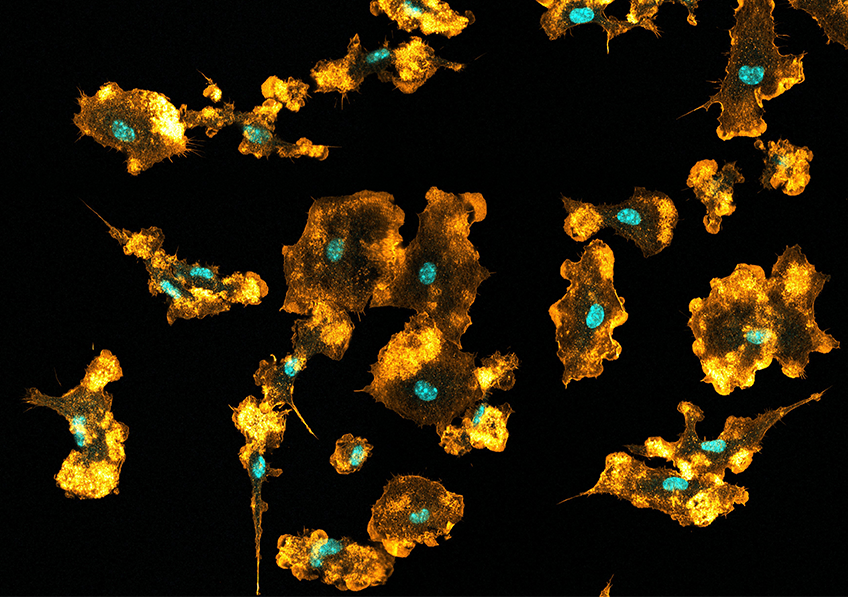 Macrophages de souris visualisés en imagerie par microscopie confocale. Les noyaux sont visibles en bleu, le réseau d’actine en orange. © Mónica Fernández Monreal, Bordeaux Imaging Centre
Macrophages de souris visualisés en imagerie par microscopie confocale. Les noyaux sont visibles en bleu, le réseau d’actine en orange. © Mónica Fernández Monreal, Bordeaux Imaging Centre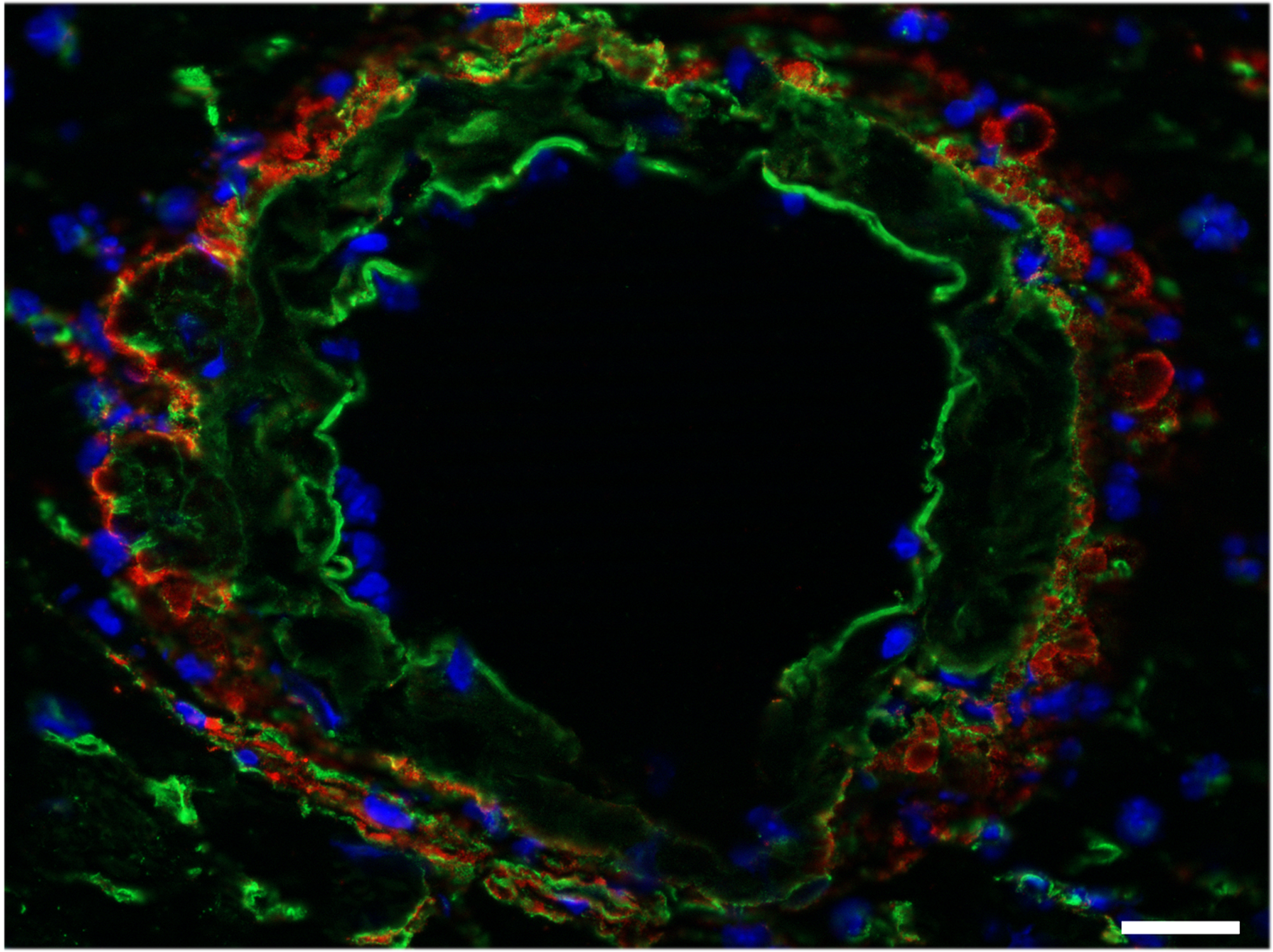




 © Photo de
© Photo de