Les participants atteints de TDAH rapportent également davantage d’épisodes de « vagabondage mental » (mind wandering) et de « blanc mental » (mind blanking), deux états directement corrélés à ces intrusions de sommeil local (image d’illustration). © Adobe Stock
Les participants atteints de TDAH rapportent également davantage d’épisodes de « vagabondage mental » (mind wandering) et de « blanc mental » (mind blanking), deux états directement corrélés à ces intrusions de sommeil local (image d’illustration). © Adobe Stock
Le trouble du déficit de l’attention avec ou sans hyperactivité (TDAH), qui touche environ 2,5 % des adultes, reste encore mal compris sur le plan biologique. Une étude internationale menée par des scientifiques de l’Inserm au sein de l’Institut du Cerveau (Inserm/CNRS/Sorbonne Université), et de l’Université Monash, en Australie, suggère que certains symptômes pourraient s’expliquer par l’intrusion d’ondes cérébrales lentes, habituellement associées au sommeil, pendant l’éveil. Ces ondes lentes pourraient ainsi constituer un biomarqueur potentiel du TDAH. À terme, ces résultats pourraient orienter de nouvelles stratégies thérapeutiques, notamment en agissant sur la qualité du sommeil et la régulation de la vigilance.
Oublis fréquents, erreurs d’inattention ou difficultés à maintenir son attention et à résister aux distractions : le trouble du déficit de l’attention avec ou sans hyperactivité (TDAH) touche environ 2,5 % des adultes, mais ses mécanismes biologiques restent encore mal compris.
Dans une étude internationale publiée le 16 mars dans le Journal of Neuroscience, des scientifiques de l’Inserm à l’Institut du Cerveau (Inserm/CNRS/Sorbonne Université), et de l’Université Monash, en Australie, suggèrent que les symptômes de ce trouble pourraient être liés à l’intrusion d’ondes lentes, habituellement observées lors du sommeil, pendant l’éveil. Ce phénomène, appelé « sommeil local », pourrait offrir une explication aux baisses d’attention et à la somnolence souvent observées chez les personnes atteintes de TDAH.
Pour parvenir à ces résultats, les scientifiques ont comparé l’activité cérébrale de 32 adultes atteints de TDAH, sous traitement médicamenteux, à celle de 31 adultes neurotypiques, tandis que les participants réalisaient une tâche nécessitant une attention soutenue.
Une densité d’ondes lentes plus élevées chez les adultes atteints de TDAH
Résultat : « Les adultes atteints de TDAH présentent une densité significativement plus élevée d’ondes lentes, habituellement observées lors du sommeil profond. Or, ces ondes ne sont pas anodines : plus leur densité est élevée, plus les participants commettent d’erreurs d’inattention et présentent des temps de réaction plus lents ou plus variables », résume Thomas Andrillon, chercheur Inserm au sein de la DreamTeam à l’Institut du Cerveau, et dernier auteur de l’étude.
Les participants atteints de TDAH rapportent également davantage d’épisodes de « vagabondage mental » (mind wandering) et de « blanc mental » (mind blanking), deux états directement corrélés à ces intrusions de sommeil local. Par ailleurs, le niveau de fatigue ressenti par les participants augmente à mesure que ces ondes lentes s’accumulent au cours de l’effort attentionnel.
« L’intrusion d’ondes du sommeil est un phénomène parfaitement normal. Pensez à une longue course à pied : au bout d’un certain temps, la fatigue physique vous oblige à faire une pause. C’est la même chose pour la fatigue mentale : après une journée passée éveillée ou après une mauvaise nuit de sommeil, le cerveau fait aussi des pauses sous la forme d’ondes lentes. Ces brefs moments d’inactivité cérébrale surviennent chez tout le monde », explique le chercheur.
Chez les personnes atteintes de TDAH, toutefois, cette activité est plus fréquente. Nos résultats suggèrent qu’elle pourrait constituer un mécanisme cérébral clé expliquant leurs difficultés à maintenir une attention et des performances stables au cours du temps.
Thomas Andrillon, chercheur Inserm
Pour les scientifiques, ces ondes lentes pourraient ainsi constituer une piste d’explication reliant le diagnostic de TDAH aux symptômes comportementaux observés au quotidien. Cette découverte suggère en effet que le TDAH pourrait être, au moins en partie, un trouble de la régulation de l’éveil et de la vigilance. « Ces ondes de sommeil local pourraient devenir un biomarqueur clé pour le diagnostic », avance Thomas Andrillon.
Ces résultats pourraient également orienter le développement de nouvelles stratégies thérapeutiques, qu’elles soient pharmacologiques ou non médicamenteuses, notamment des interventions visant à améliorer la qualité du sommeil ou à stabiliser les mécanismes de vigilance.
« Chez les personnes neurotypiques, certaines recherches ont par exemple montré que la stimulation auditive pendant le sommeil peut renforcer les ondes lentes nocturnes, ce qui pourrait réduire l’apparition d’une activité cérébrale proche du sommeil durant l’éveil le lendemain. Une prochaine étape consistera à déterminer si cette approche pourrait également diminuer ces intrusions de sommeil local chez les personnes atteintes de TDAH », conclut Thomas Andrillon.


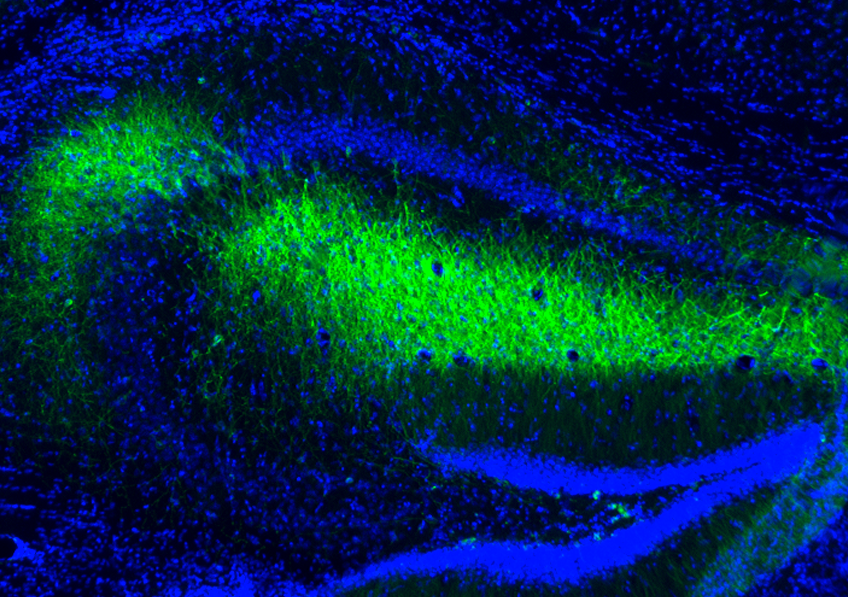
 Les tanycytes (en blanc) capturent la protéine Tau (rouge) circulant dans le liquide céphalorachidien pour la transporter le long de leurs prolongements/bras qui traversent le tissu cérébral et entrent en contact avec les vaisseaux sanguins (en vert) dans lesquels ils déversent cette protéine impliquée dans la pathologie d’Alzheimer lorsqu’elle s’accumule dans le cerveau. © Vincent Prévot/Inserm
Les tanycytes (en blanc) capturent la protéine Tau (rouge) circulant dans le liquide céphalorachidien pour la transporter le long de leurs prolongements/bras qui traversent le tissu cérébral et entrent en contact avec les vaisseaux sanguins (en vert) dans lesquels ils déversent cette protéine impliquée dans la pathologie d’Alzheimer lorsqu’elle s’accumule dans le cerveau. © Vincent Prévot/Inserm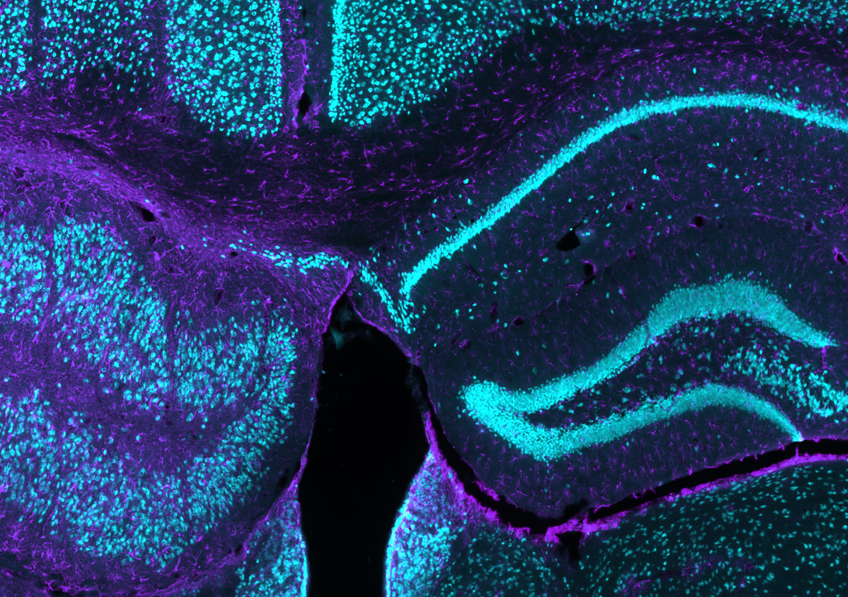



 Les neurones du cortex préfrontal dorso-médian (image ci-dessus) encodent simultanément la valence, la valeur et la saillance des stimuli provenant de l’environnement. © Daniel Jercog
Les neurones du cortex préfrontal dorso-médian (image ci-dessus) encodent simultanément la valence, la valeur et la saillance des stimuli provenant de l’environnement. © Daniel Jercog
 ©
©