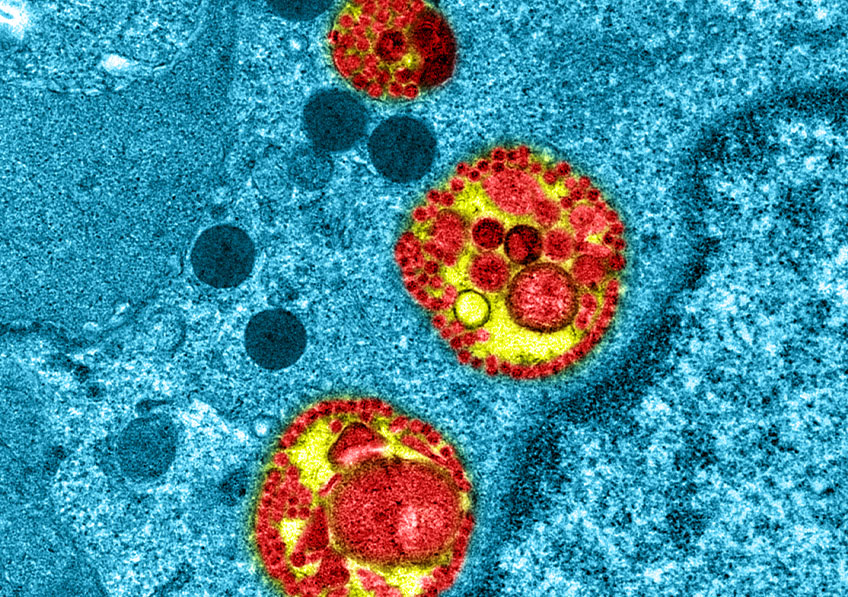
Covid-19: Observation intracellulaire d’épithélium respiratoire humain reconstitué MucilAir™ infecté par le SARS-CoV-2. © Manuel Rosa-Calatrava, Inserm ; Olivier Terrier, CNRS ; Andrés Pizzorno, Signia Therapeutics ; Elisabeth Errazuriz-Cerda UCBL1 CIQLE. VirPath (Centre International de Recherche en Infectiologie U1111 Inserm – UMR 5308 CNRS – ENS Lyon – UCBL1). Colorisé par Noa Rosa C.
Chez certains patients avec pneumonie Covid-19, un état hyperinflammatoire d’origine immunologique contribue à l’insuffisance respiratoire aigüe et au décès. La plateforme CORIMUNO-19 a été rapidement mise en place pour permettre de tester l’efficacité et la tolérance de divers médicaments immuno-modulateurs chez les patients adultes avec infection COVID-19 modérée à sévère, grâce à une série d’essais randomisés contrôlés multicentriques, qui ont débuté le 27 mars 2020.
Le tocilizumab est un anticorps monoclonal qui bloque le récepteur de la cytokine interleukine-6. Les résultats définitifs de l’essai randomisé contrôlé ouvert multicentrique du tocilizumab, sont publiés après revue par des pairs le 20 octobre 2020 dans la revue JAMA Internal Medicine.
Les résultats définitifs de cet essai confirment les résultats préliminaires communiqués le 27 avril 2020. Ils devraient être corroborés de manière indépendante par des essais supplémentaires. Les patients inclus étaient hospitalisés pour pneumonie COVID-19 modérée à sévère, nécessitant au moins 3 L/mn d’oxygène mais sans recours à la réanimation au moment de leur admission. Le critère de jugement primaire sur lequel s’est appuyée l’analyse pour juger de l’efficacité du traitement était la combinaison du besoin de ventilation (mécanique ou non invasive) ou du décès à J+14.[1] Au total, 130 patients d’âge médian 64 ans ont été inclus dans cet essai clinique randomisé ouvert : 67 pour le traitement usuel et 63 pour le tocilizumab associé au traitement usuel.
A l’inclusion les besoins médians en oxygène étaient de 5L/mn. La proportion de patients ayant nécessité une ventilation non invasive, une intubation ou décédés au 14ème jour était de 36 % avec les soins usuels et de 24 % avec le tocilizumab. Aucune différence de mortalité à 28 jours n’a été constatée entre les deux bras (11.1% et 11.9%), respectivement.
Ainsi, au 14ème jour, le risque de mourir ou d’avoir recours à la ventilation non invasive ou mécanique a été diminué de 33% dans le groupe traité par le tocilizumab.
La proportion de patients ayant dû être transférés en réanimation a été diminuée de moitié dans le bras tocilizumab (18%) comparativement au bras traitement usuel (36%). Le pourcentage de patients ayant quitté l’hôpital au jour 28 était plus importante dans le groupe tocilizumab que dans le groupe traitement usuel : 83% versus 73%.
Enfin, Le tocilizumab n’a pas entraîné plus d’effets indésirables que le traitement usuel.
Plusieurs essais CORIMUNO testant d’autres immunomodulateurs, sont en cours d’analyse et la combinaison du tocilizumab à la dexamethasone est testée dans un autre protocole de CORIMUNO.
Cet essai multicentrique a été conduit par la collaboration de recherche académique COVID-19 Assistance Publique-Hôpitaux de Paris/Université Paris-Saclay/Université de Paris/INSERM-REACTing
[1] La ventilation non invasive regroupe l’ensemble des techniques d’assistance ventilatoire, en l’absence de dispositif endo-trachéal, donc sans intubation ou trachéotomie.
La plateforme d’essais cliniques CORIMUNO-19 est promue et financée par l’Assistance Publique-Hôpitaux de Paris, et soutenue par l’Inserm via son consortium REACTing.
L’essai a reçu un financement du Programme Hospitalier de Recherche Clinique du Ministère de la Santé, un financement d’amorçage de l’Inserm par le biais du consortium REACTing/INSERM via la Fondation pour la Recherche Médicale, Paris, France, et un financement de la Fondation AP-HP pour la recherche, Paris, France. Le tocilizumab ainsi que 4 000 kits de dosage Elecsys d’interleukine 6 ont été fournis sans conditions par le laboratoire Roche, qui n’a été impliqué ni dans la conception de l’essai, la collection des données, l’analyse, l’interprétation, l’écriture du manuscrit ni dans la gouvernance de l’essai.
Ces contenus pourraient aussi vous intéresser :
- Investigateur coordinateur : Pr O. Hermine, Hôpital Necker, AP-HP, Imagine Institute, INSERM U1163, Université de Paris
- Co Investigateur coordinateur : Pr X. Mariette, Hôpital Bicêtre, AP-HP, INSERM U1184, Université Paris-Saclay
- Directeur scientifique : Dr P.L. Tharaux, Paris Centre de Recherche Cardiovasculaire (PARCC), INSERM U970, Hôpital Européen Georges Pompidou, AP-HP, Université de Paris.
- Conception et coordination de la plateforme d’essais CORIMUNO : Pr P. Ravaud, Center for Clinical Epidemiology, Hôpital Hôtel Dieu, AP-HP, CRESS, INSERM U1153, Université de Paris
- Statisticien : Dr R. Porcher, Center for Clinical Epidemiology, Hôpital Hôtel Dieu, AP-HP, CRESS, INSERM U1153, Université de Paris
- Monitoring et data management : Pr M. Resche-Rigon (Clinical Trial Unit, Hôpital Saint Louis, AP-HP), CRESS, INSERM U1153, Université de Paris.
- Organisation de la collection des données : Pr M Dougados, Hôpital Cochin, AP-HP, CRESS, INSERM U1153, Université de Paris
Résultats définitifs de l’essai randomisé contrôlé ouvert CORIMUNO-TOCI-1 publiés dans la revue JAMA Internal Medicine le 20 octobre 2020