Contact Chercheur
Manuel Rosa-Calatrava
Chercheur Inserm
U 1111 – Centre international de recherche en infectiologie (CIRI)
rf.1noyl-vinu@avartalac-asor.leunam
Tél : 04 78 77 10 37
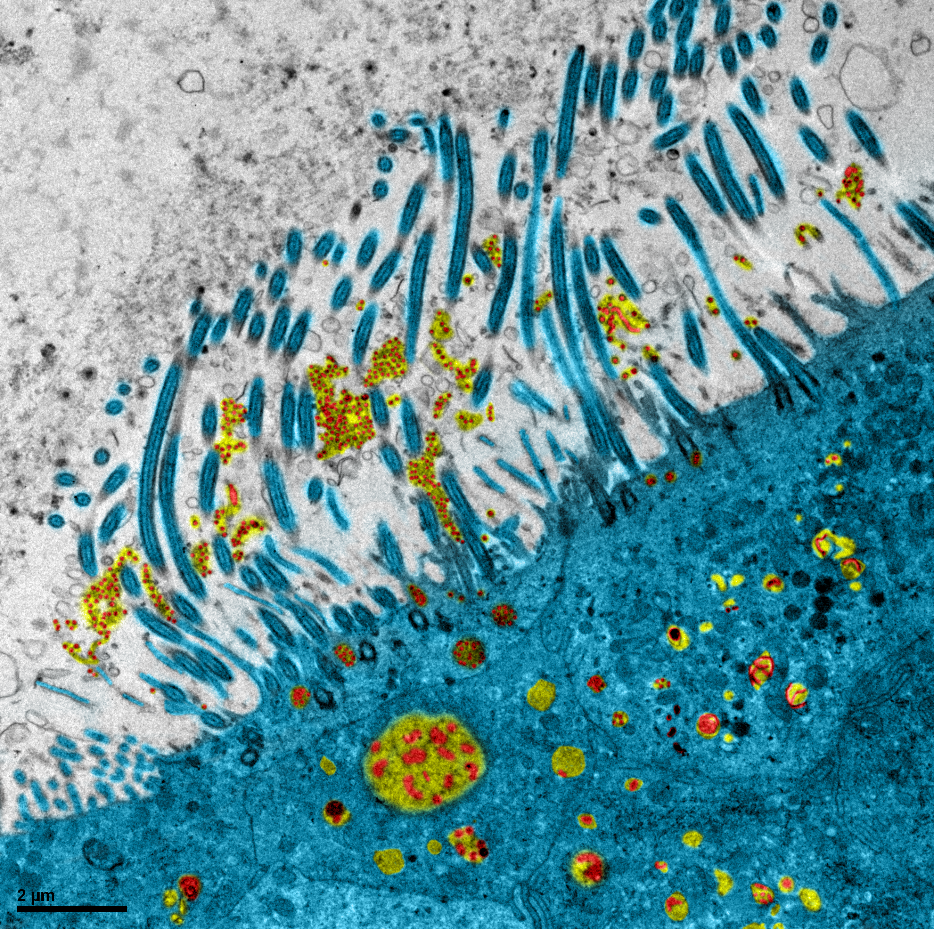
Epithélium respiratoire humain infecté par le SARS-CoV-2. Des grappes de virus au niveau des cils des cellules épithéliales ainsi que de très nombreuses vésicules cytoplasmiques très caractéristiques contenant de larges accumulations de matériel viral (dense aux électrons) et de nombreux virus en assemblage sont observés. © Manuel Rosa-Calatrava, Inserm; Olivier Terrier CNRS; Andrés Pizzorno Signia Therapeutics; Elisabeth Errazuriz-Cerda UCBL1 CIQLE. VirPath (Centre International de Recherche en Infectiologie U1111 INSERM – UMR 5308 CNRS – ENS Lyon – UCBL1). Colorisé par Noa Rosa C.
Alors que la pandémie de Covid-19 se poursuit, trouver un traitement permettant de lutter efficacement contre la maladie reste un enjeu majeur de la recherche. Des chercheurs de l’Inserm, du CNRS, de l’Université Claude Bernard Lyon 1 et de l’ENS Lyon au sein du Centre international de recherche en infectiologie (CIRI) ont mis au point une stratégie unique de sélection, d’évaluation et de repositionnement de médicaments déjà sur le marché pour évaluer leur effet contre le SARS-CoV-2. Ils ont également développé plusieurs modèles précliniques d’infections très pertinents, à partir d’épithéliums respiratoires humains d’origine nasale et bronchique reconstitués in vitro. Grâce à leur savoir-faire, les chercheurs montrent que l’association entre la molécule remdesivir, utilisée dans le traitement d’Ebola, et l’antihypertenseur diltiazem pourrait apporter un bénéfice significatif chez les patients atteints de Covid-19. Leurs résultats sont publiés dans Cell Reports Medicine.
Dans le cadre du programme REACTing coordonné par l’Inserm, l’équipe Virpath dirigée par le chercheur Inserm Manuel Rosa-Calatrava au Centre international de recherche en infectiologie (Inserm/CNRS/Université Claude Bernard Lyon 1/ENS Lyon) travaille au repositionnement pour de nouvelles indications thérapeutiques contre les infections virales de médicaments déjà disponibles sur le marché.
Pour tester l’efficacité thérapeutique de ces molécules contre le Covid-19, l’équipe a développé et caractérisé dès le mois de février des modèles expérimentaux d’infections virales. Pour cela elle a reconstitué in vitro, au plus proche de la physiologie humaine, des épithéliums respiratoires humains d’origine nasale et bronchique. « Nous utilisons depuis plusieurs années ces modèles précliniques d’infection, qui sont très prédictifs de l’infection in vivo », précise Manuel Rosa Calatrava.
Les chercheurs ont aussi développé plusieurs protocoles de quantification de génome viral et de particules infectieuses. Leurs observations et analyses ont confirmé et complété les connaissances actuelles sur les mécanismes de l’infection par le SARS-CoV-2 et les interactions entre le virus et son hôte. « Nous observons notamment dans nos modèles infectés par le virus l’induction de la production d’interleukines Il6 qui est un des marqueurs de sévérité de la maladie », précise Manuel Rosa-Calatrava.
Le diltiazem, lui, est un antihypertenseur utilisé dans le traitement de l’angine de poitrine. Il a déjà été caractérisé et repositionné par les chercheurs de VirPath afin de stimuler fortement la réponse immunitaire innée antivirale endogène, notamment contre les virus influenza et les pneumovirus. La toxicité chez l’humain de ces deux molécules repositionnées a aussi déjà été évaluée, ce qui permet de réduire considérablement les délais de leur développement clinique pour leur nouvelle indication thérapeutique contre le SARS-CoV-2.
Les résultats de cette étude montrent une réduction significative de la charge virale dans les épithéliums infectés par le SARS-CoV-2 lorsqu’ils sont traités par le remdesivir. Cet effet est accru lorsque le diltiazem est ajouté en combinaison. « En stimulant la réponse immunitaire innée des épithéliums, le diltiazem potentialise l’effet du remdesivir et offre l’opportunité d’en réduire les doses. Le remdesivir présente en effet une certaine toxicité in vivo en plus d’être un médicament très couteux », souligne Manuel Rosa-Calatrava.
L’équipe poursuit ses essais précliniques avec cette bithérapie dans des modèles animaux et espère lancer un essai clinique dès l’hiver prochain si les résultats positifs se confirment.
Manuel Rosa-Calatrava
Chercheur Inserm
U 1111 – Centre international de recherche en infectiologie (CIRI)
rf.1noyl-vinu@avartalac-asor.leunam
Tél : 04 78 77 10 37
Characterization and treatment of SARS-CoV-2 in nasal and bronchial human airway epithelia
Andrés Pizzorno1, Blandine Padey1,2, Thomas Julien1,3, Sophie Trouillet-Assant1,4, Aurélien Traversier1, Elisabeth Errazuriz-Cerda5, Julien Fouret2, Julia Dubois1, Alexandre Gaymard1,6, François-Xavier Lescure7,8, Victoria Dulière1,2, Pauline Brun1,2, Samuel Constant9, Julien Poissy10, Bruno Lina1,6, Yazdan Yazdanpanah7,8, Olivier Terrier1, Manuel RosaCalatrava1,2
1 Virologie et Pathologie Humaine – VirPath team, Centre International de Recherche en Infectiologie (CIRI), Inserm U1111, CNRS UMR5308, ENS Lyon, Université Claude Bernard Lyon 1, Université de Lyon, Lyon, France.
2 Signia Therapeutics SAS, Lyon, France.
3 VirNext, Faculté de Médecine RTH Laennec, Université Claude Bernard Lyon 1, Université de Lyon, Lyon, France.
4 Laboratoire Commun de Recherche HCL-bioMérieux, Centre Hospitalier Lyon-Sud, PierreBénite, France.
5 Centre d’Imagerie Quantitative Lyon-Est (CIQLE), Université Claude Bernard Lyon 1, Lyon, France.
6 Laboratoire de Virologie, Centre National de Référence des virus Influenza Sud, Institut des 20 Agents Infectieux, Groupement Hospitalier Nord, Hospices Civils de Lyon, Lyon, France.
7 AP-HP, Infectious and Tropical Diseases Department, Bichat-Claude Bernard University Hospital, Paris, France.
8 University of Paris, French Institute for Health and Medical Research (Inserm), IAME, U1137, Team DesCID, Paris, France.
9 Epithelix Sàrl, Geneva, Switzerland.
10 Pôle de Réanimation, Hôpital Roger Salengro, Centre Hospitalier Régional et Universitaire de Lille, Université de Lille 2, Lille, France
Cell Reports Medicine, Juillet 2020