©Inserm/ Patrick Delapierre
L’espace est un extraordinaire laboratoire pour la médecine et la recherche médicale sur Terre. C’est pourquoi l’Inserm et le CNES allient leurs forces, depuis plus d’un an1, pour accélérer la mise à disposition des avancées de la recherche pour améliorer la santé de tous. La présence de Thomas Pesquet, astronaute de l’ESA de nationalité française à bord de la station spatiale internationale pendant 6 mois a donné lieu à un grand nombre d’expériences dont les premiers résultats viennent conforter les hypothèses des chercheurs et parfois les surprendre. Thomas Pesquet présentera ces découvertes, le 10 octobre 2017, lors d’une séance exceptionnelle organisée par l’Académie des sciences, sous la Coupole de l’Institut de France.
Dans l’espace, les muscles, les os, les artères, les organes des sens, le système nerveux, le système immunitaire souffrent dans des conditions d’impesanteur et d’accélération pour lesquelles ils n’ont pas été adaptés. Pourquoi ces dérèglements ? L’évolution humaine sur Terre a optimisé notre corps pour répondre à la gravité de notre planète et pour vivre en dessous de l’enveloppe protectrice de l’atmosphère. Soudain libéré de cette contrainte gravitaire, exposé aux radiations et éléments lourds d’origine cosmique, le corps humain peut souffrir de maux spécifiques et jusqu’alors inconnus. De même, l’organisme doit affronter des conditions stressantes, la limitation des mouvements, l’alimentation peu diversifiée, le rythme veille-sommeil perturbé.
Face à ce constat, les chercheurs de l’Inserm et du CNES sont mobilisés pour :
- Protéger la santé des astronautes et diagnostiquer en temps réel leurs conditions de santé, envoyer et traiter sur Terre les
Utiliser l’espace comme un champ d’investigation permettant de mieux comprendre la physiologie et les maladies fréquentes. Des pathologies nombreuses et répandues bénéficient en effet du suivi médical poussé des astronautes, comme l’ostéoporose, les troubles du rythme circadien et du sommeil, les anomalies de l’oreille interne et de l’équilibre, les difficultés d’attention et de concentration, le vieillissement artériel.
Des premiers résultats « post flight »
Sur les données médicales et physiologiques
À bord de la station, le suivi des astronautes représente un enjeu quotidien. Le système EveryWear, développé par le MEDES, la filiale santé du CNES, propose une nouvelle approche en la matière, avec un assistant matérialisé par une simple application sur tablette tactile. Il s’agit plus précisément de regrouper un ensemble de capteurs biomédicaux portatifs connectés en Bluetooth à un terminal mobile (en l’occurrence une tablette grand public).
L’utilisation d’une tablette qui recueille un ensemble d’informations distinctes est une grande avancée pour les données médicales, physiologiques et personnelles de l’astronaute. Les principaux atouts d’EveryWear sont sa capacité à agréger les données provenant de différents outils mais aussi la simplification qu’il apporte dans les procédures pour les astronautes. C’est un dispositif adaptable qui peut couvrir un large éventail de besoins : nutrition, sommeil, étude du système cardiovasculaire, avec une collecte de données adaptée qui permet un traitement uniformisé. Là encore, le gain de temps pour l’équipage, induit par l’assistant personnel est très important. À titre d’exemple, le suivi nutritionnel de l’astronaute l’obligeait par le passé à répondre à des questionnaires au fur et à mesure de la prise de nourriture. Désormais, les données sont transmises directement.
Sur l’évaluation du sommeil
L’Unité Inserm 1075 à Caen travaille avec la société Bodycap sur des capteurs actimétriques et de température miniaturisés. Ces capteurs et les logiciels d’analyse correspondants ont été intégrés dans « l’assistant embarqué » du vol de Thomas Pesquet afin, en particulier, de procéder à une évaluation du sommeil et des rythmes chronobiologiques. Les premiers résultats, à prendre avec précaution car issus de l’analyse des données d’une seule personne, sont assez inattendus. Ils montrent que, malgré une forte influence de la pesanteur sur les mouvements corporels – et donc sur l’actimétrie – les relations entre les données actimétriques et l’état de vigilance (veille/sommeil) sont les mêmes à bord de l’ISS que sur terre. Si ce résultat se confirmait il faciliterait le suivi médicophysiologique des astronautes.
Le contrôle des données physiologiques et environnementales étant un enjeu déterminant de la nouvelle médecine personnalisée, l’amélioration de ces dispositifs peut avoir de nombreuses retombées. Par exemple, ces résultats pourraient contribuer à améliorer les montres connectées dont les capteurs (trackers de sommeil) évaluent le sommeil en fonction des mouvements et de la réorientation du poignet pendant la nuit, eux-mêmes dépendant de la gravité.
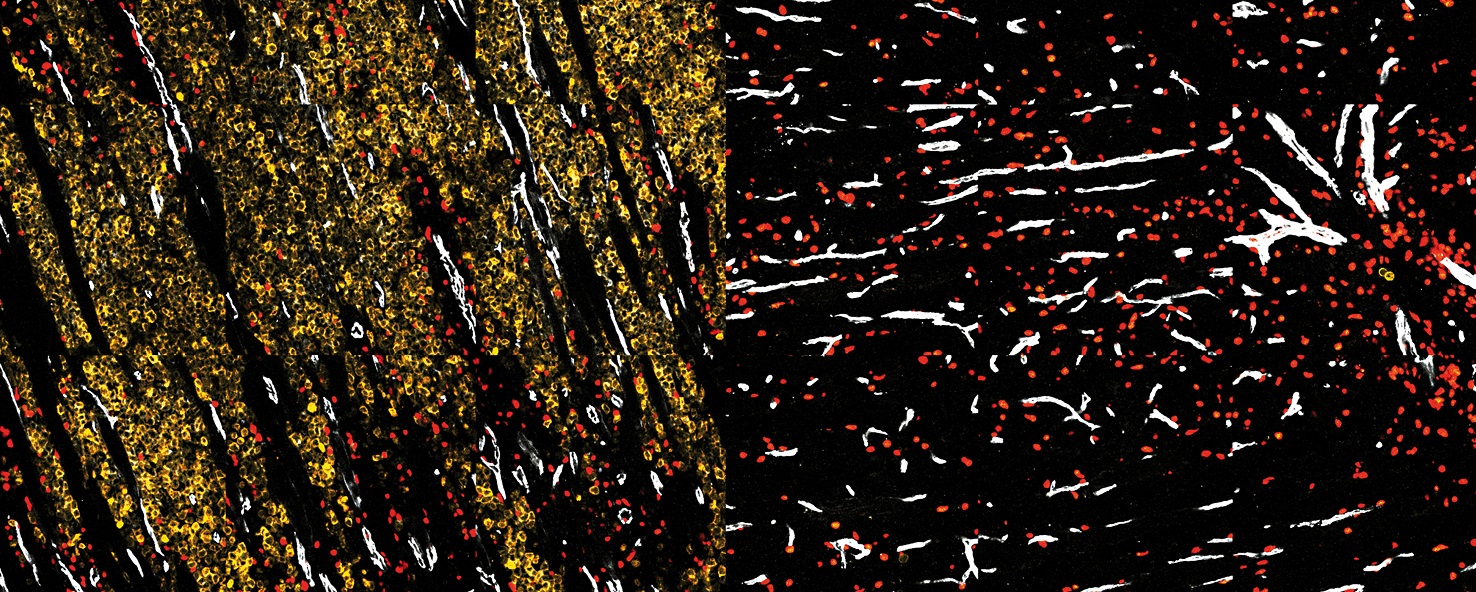
Sur la fragilité osseuse
L’équipe de Laurence Vico, directrice de recherche à l’unité Inserm 1059, étudie les changements que les vols spatiaux induisent sur la structure des os. Pour analyser la structure du radius et du tibia, les expériences utilisent un scanner haute résolution (développé avec l’aide de l’Agence Spatiale Européenne). En plus de mesurer la densité minérale osseuse, cet appareil permet de réaliser une « biopsie osseuse virtuelle » non invasive, offrant une vision très précise de l’architecture osseuse en 3 dimensions.
S’il n’est pas permis de donner les résultats individuels des mesures prises sur Thomas Pesquet, des résultats issus d’une cohorte plus importante de 13 cosmonautes montrent non seulement que les os porteurs (jambes) ne récupèrent pas une qualité identique à celle précédant le vol dans l’espace mais, fait nouveau, il apparait que les os non porteurs (bras), préservés au moment du retour sur Terre, se détériorent progressivement.
La confrontation de ces résultats à ceux obtenus sur des souris montre que les cellules qui orchestrent les activités de formation et de résorption osseuses (ostéocytes) et qui vivent normalement plusieurs années, meurent prématurément en apesanteur. Une contremesure capable d’agir sur ce vieillissement précoce est testée. Elle pourrait s’appliquer aux patients souffrant d’ostéoporose.
Sur le cœur
Pierre Boutouyrie mène ses recherches au sein de l’Unité Inserm 970. C’est un des premiers laboratoires à avoir travaillé sur les conséquences des conditions de microgravité ou hypergravité notamment sur le vieillissement accéléré de nos artères. Les vols spatiaux sont de bons modèles pour l’étudier. On sait par exemple qu’en vieillissant les artères sont moins souples, amortissent moins le flux sanguin et s’exposent à l’athérosclérose avec pour conséquences des effets délétères sur le cœur, le cerveau et les reins.
Dans le cadre du vol de Thomas Pesquet, les changements liés à la microgravité ont été étudiés grâce à la pose de capteurs piézo-électriques souples2 reliés à l’assistant embarqué de Thomas Pesquet. Là encore, les données individuelles ne peuvent pas être dévoilées mais les premiers résultats d’une étude bed-rest menée pendant 2 mois sur 10 patients, ainsi que les données publiées par une équipe internationale chez des astronautes, montrent qu’il existe un remodelage très rapide et très important du système artériel traduisant un vieillissement accéléré de celui-ci. Outre les spationautes, les patients alités longtemps pour des problèmes de santé subissent ces mêmes conséquences. Les chercheurs testent en ce moment même des contre-mesures diététiques ou d’activité physique pour pallier ces effets chez les patients alités.
Assistez à la diffusion en direct, sur le site de l’Académie des sciences, de la séance sous la Coupole en présence de Thomas Pesquet !
Le 6 décembre 2016, l’Académie des sciences ouvrait ses portes à plus de 300 lycéens et lycéennes accompagnés de leurs professeurs. À leur intention était organisé un duplex depuis l’ISS, avec Thomas Pesquet.
Le 10 octobre 2017, Thomas Pesquet revient, en personne, sous la Coupole de l’Institut de France pour raconter son quotidien dans l’espace, au sein d’un laboratoire de recherche, et présenter les résultats des expériences scientifiques développées par le CNES et l’Inserm sous l’égide de la NASA et de l’ESA.
Cette séance est également l’occasion de remettre les prix de l’Académie des sciences aux majors des grandes écoles, aux lauréats des Olympiades nationales et internationales, aux lauréats des bourses Rogissart, et aux lauréats des Grandes avancées françaises en biologie présentées par leurs auteurs.
Pour assister à la diffusion en direct sur internet, le 10 octobre à partir de 15h : http://www.academie-sciences.fr/fr/Ceremonies/seance-thomas-pesquet-2017.html