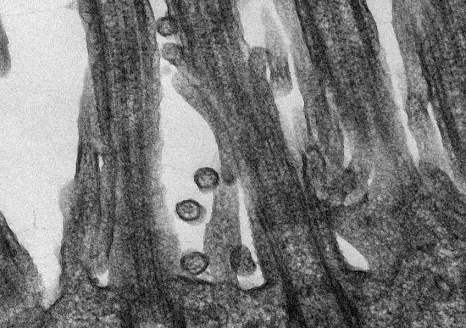
Coronavirus SARS-CoV-2 responsables de la maladie COVID-19 accrochés aux cellules épithéliales respiratoires humaines ©M.Rosa-Calatraval/O.Terrier/A.Pizzorno/E.Errazuriz-cerda
À plusieurs reprises depuis le début de la pandémie, l’idée que des mutations auraient rendu le virus plus dangereux a régulièrement été évoquée. Tout au long du mois de septembre, l’affirmation inverse, selon laquelle le SARS-CoV-2 serait devenu moins dangereux suite à des mutations survenues au cours de l’été, circulait aussi sur les réseaux sociaux.
Que sait-on aujourd’hui sur les mutations du coronavirus à l’origine de la Covid-19 ? Et que peuvent-elles nous apprendre sur l’évolution possible de la pandémie ? Canal Détox coupe court aux fausses infos.
Tous les virus peuvent muter. Après avoir infecté nos cellules, ceux-ci se multiplient en réalisant des copies d’eux-mêmes. Ce processus n’est pas parfait et les copies peuvent comporter des « erreurs » : les fameuses mutations. Le matériel génétique des copies virales diffère alors du matériel génétique du virus de départ.
Si ces mutations peuvent n’avoir aucune conséquence, elles peuvent dans certains cas avoir un impact, par exemple sur la transmissibilité ou sur la virulence du virus. Les mutations expliquent aussi le passage d’un virus d’une espèce à une autre : elles jouent un rôle dans l’adaptation du virus au nouvel hôte.
En comparaison avec les virus à ADN, les virus à ARN (comme par exemple le virus de la grippe ou le VIH) ont tendance à muter plus rapidement et plus fréquemment. Les coronavirus, qui sont également des virus à ARN, sont néanmoins plutôt stables car ils produisent une enzyme correctrice d’erreurs, appelée « exoribonucléase ». Le SARS-CoV-2 muterait ainsi environ deux fois moins rapidement que les virus grippaux.
Erreurs dans la réplication virale
Cela dit, des erreurs lors de la réplication virale restent possibles, ce qui pousse les virologues à surveiller la manière dont ce nouveau coronavirus évolue. L’enjeu n’est pas seulement de réussir à identifier d’éventuelles mutations, mais surtout de réussir à les interpréter et à évaluer leurs potentielles implications cliniques.
Pour mener à bien ce type de recherche, les scientifiques s’appuient sur des technologies de séquençage haut débit pour décrypter le génome entier du SARS-CoV-2. Ces technologies, développées pour le séquençage du génome humain, permettent d’obtenir un grand nombre de données afin de caractériser finement le génome viral. Elles sont plus précises et plus performantes que la technique « ancestrale » de séquençage appelée méthode Sanger (du nom de son inventeur). Ces techniques, assez lourdes et coûteuses, sont à l’ordinaire peu utilisées pour l’analyse des mutations virales, mais s’avèrent nécessaires dans le cas de ce nouveau coronavirus en raison de la taille de son génome viral, le plus gros retrouvé chez l’humain.
Ces travaux doivent donc s’appuyer sur une collaboration étroite entre virologues et bio-informaticiens afin de pouvoir analyser et organiser de manière cohérente les très nombreuses données qui sont issues d’un séquençage complet du SARS-CoV-2, puis d’identifier les éventuelles mutations.
Autre outil crucial ayant montré son utilité pendant cette pandémie : GISAID, la plateforme de collecte et d’analyse des données de séquences du SARS-CoV-2. Mise en place à l’origine pour rassembler à un endroit et analyser les séquences du virus de la grippe, GISAID permet aux chercheurs d’avoir accès rapidement à plus de 130 000 séquences complètes du virus provenant de 122 pays. Cette plateforme est donc très importante pour suivre les évolutions du SARS-CoV-2 et de la pandémie.
Mutations et épidémie
Plusieurs dizaines de mutations du SARS-CoV-2 ont déjà été décrites, sans que des conséquences sur l’épidémie aient été mises en évidence.
Certaines ont néanmoins fait l’objet de travaux plus poussés, publiés dans des revues scientifiques. C’est le cas notamment de la mutation D614G au niveau de la protéine Spike du virus, qui a d’abord fait l’objet d’une publication dans le journal Cell. Cette mutation s’est largement diffusée et est rapidement devenue dominante parmi les isolats de virus circulants.
D’autres études ont ensuite été publiées à son sujet, montrant que cette mutation a eu pour effet de rendre le virus plus facilement transmissible. Néanmoins, les implications de cette transmissibilité accrue du coronavirus en matière de sévérité de l’infection et de mortalité sont encore loin d’être claires. Il n’existe pour le moment aucune donnée pour soutenir l’idée que cette mutation aurait rendu le virus plus virulent.
D’autres travaux récents publiés dans The Lancet et menés en Asie sur des échantillons collectés auprès de patients ont montré que, chez 25 % d’entre eux, une délétion est présente. Autrement dit, un morceau de matériel génétique est absent. Cette délétion, appelée Δ382, concerne une région du génome qui interagit avec le système immunitaire des hôtes, modulant notamment la réponse antivirale. Étant donné cette interaction, les scientifiques vont continuer à étudier avec précision les conséquences potentielles de cette mutation.
Les auteurs de l’étude supposent pour le moment qu’elle serait associée à une infection moins sévère mais les données manquent encore pour étayer cette hypothèse. En l’état actuel des connaissances, aucune preuve concluante n’a été apportée sur les implications cliniques potentielles de cette délétion. Il n’est pas non plus encore certain que cette souche du virus circule déjà en Europe.
Dans tous les contextes épidémiques, par exemple lors des épidémies de grippe ou de polio, les mutations des virus responsables ont toujours fini par aboutir à une atténuation de leur virulence. Les virologues espèrent que ce sera aussi le cas pour l’épidémie de SARS-CoV-2.
Etudier les mutations de ce virus est essentiel pour comprendre comment mieux traiter les patients, mais aussi pour accompagner la recherche thérapeutique et vaccinale. En effet, en fonction de l’apparition de nouvelles mutations, les traitements et les candidats vaccins pourraient être plus ou moins efficaces contre le virus. Les équipes de virologues qui surveillent les mutations doivent donc continuer à travailler de concert avec les autres disciplines afin que la recherche puisse progresser.
Texte rédigé avec le soutien d’Anne Goffard, virologue au Centre d’infection et d’immunité de Lille (Inserm/Université de Lille/Institut Pasteur de Lille/CHU de Lille) et de Marie-Paule Kieny, directrice de recherche à l’Inserm.
Ce texte rend compte des connaissances disponibles au 12 octobre 2020, qui sont susceptibles d’évoluer en fonction des avancées scientifiques.


