(c) EPFL
Des primates non-humains ont retrouvé le contrôle d’un membre inférieur paralysé suite à une lésion de la moelle épinière. Cette avancée a été rendue possible grâce à une interface cerveau-moelle épinière (dite « neuroprothèse »). Ce système agit comme un pont sans fil entre le cerveau et les centres de la marche situés dans la moelle épinière, court-circuitant ainsi la lésion. Cette neuroprothèse a été développée par un consortium international mené par l’École Polytechnique de Lausanne (EPFL) au sein duquel l’Institut des maladies neurodégénératives (CNRS/Université de Bordeaux) sous la direction d’Erwan Bezard, directeur de recherche Inserm a mené la validation expérimentale chez l’animal. Les résultats sont publiés le 9 novembre 2016 dans la revue Nature. Un essai clinique a d’ores et déjà été initié à l’hôpital universitaire de Lausanne afin de tester les effets thérapeutiques de cette neuroprothèse chez des patients souffrant de lésions de la moelle épinière.
Le 23 juin 2015, un premier singe macaque porteur d’une lésion de la moelle épinière a pu retrouver le contrôle d’un membre inférieur paralysé, et donc remarcher, grâce à une neuroprothèse appelée « interface cerveau-machine » court-circuitant la lésion. Ce système est capable de restaurer la communication entre le cerveau (lieu de genèse des actions volontaires) et la région de la moelle épinière produisant les mouvements des membres inférieurs.
Comment ?
Cette interface cerveau-machine enregistre l’activité cérébrale liée à l’intention de marche, la décode, et transmet cette information à la moelle épinière sous la lésion. Cette transmission est assurée par des électrodes qui stimulent les réseaux nerveux activant les muscles des jambes pendant la locomotion naturelle. Ainsi, seuls les mouvements souhaités par le singe sont produits.
Cette neuroprothèse a été conçue à l’EPFL (Lausanne, Suisse) et techniquement développée par un groupe international composé de Medtronic (USA), l’Université Brown (USA) et le Fraunhofer ICT-IMM (Mayence, Allemagne). Elle a ensuite été testée chez le primate en collaboration avec l’Inserm, le CNRS, l’Université de Bordeaux et le Centre Hospitalier Universitaire de Lausanne (Suisse).
“C’est la première fois qu’une neuroprothèse restaure la marche chez le primate » déclare Grégoire Courtine, professeur à l’EPFL, qui conduit le consortium.
“Les deux singes ont été capables de remarcher immédiatement après la mise en fonction de la neuroprothèse. Aucun entrainement n’a été nécessaire » indique Erwan Bézard, directeur de recherches Inserm et directeur de l’Institut des maladies neurodégénératives (CNRS/Université de Bordeaux), qui a supervisé les expériences sur le primate menées dans son centre. “ Il faut toutefois conserver à l’esprit les nombreux challenges qu’il reste à relever. Même si les essais cliniques débutent, cela prendra quelques années avant que de telles approches soient disponibles en clinique pour l’Homme ».
L’interface cerveau-moelle épinière court-circuite la lésion, en temps réel et sans fil
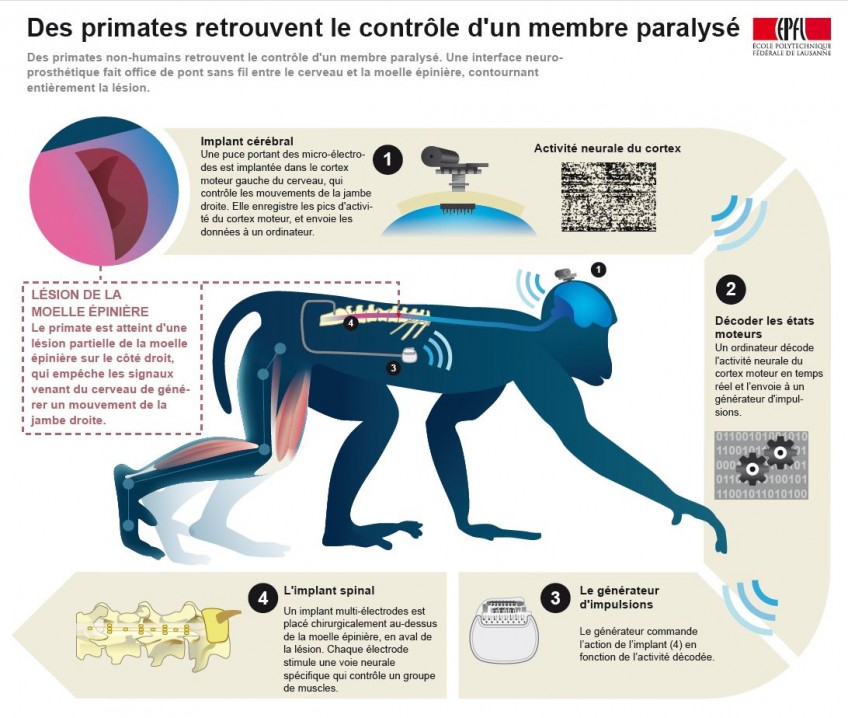
Dans le système nerveux intact, le signal électrique produisant la marche est généré au niveau des neurones cérébraux du cortex moteur. Ces signaux sont aussitôt envoyés à la région lombaire de la moelle épinière. A ce niveau, des réseaux complexes de neurones prennent le relais et contrôlent l’activation des muscles des jambes responsables de la marche. Des faisceaux de fibres nerveuses provenant du cerveau fournissent l’information requise à ces neurones quant à l’intention (ou non) de marcher, leur permettant alors de s’activer pour la réalisation du comportement. Une stimulation électrique délivrée précisément est donc capable de moduler ces réseaux et de produite l’activation désirée des muscles des jambes.
L’interface cerveau-moelle épinière court-circuite la lésion, en temps réel et sans fil. La neuroprothèse décode l’activité du cortex moteur pour « comprendre » le désir de marche ou de quelque mouvement que ce soit et transmet cette information au stimulateur. Ce dernier active les électrodes situées sous la lésion à la surface de la moelle épinière pour permettre l’activation contrôlée des muscles des jambes, en fonction du réel souhait de l’animal.
Le Pr. Jocelyne Bloch, neurochirurgienne, du centre hospitalier universitaire de Lausanne (CHUV) conduit maintenant l’essai clinique qui permettra d’évaluer, chez l’Homme, le potentiel thérapeutique de cette technologie qui permettrait à des patients avec des lésions incomplètes de la moelle épinière de remarcher.
L’interface est composée d’un implant cérébral, d’un système d’enregistrement, d’un ordinateur, d’un stimulateur implantable et d’un implant spinal.
L’implant cérébral est une puce comparable à celles déjà utilisées chez l’Homme pour des recherches sur les interfaces cerveau-ordinateur, et placée chirurgicalement sur le cortex moteur.
Développé à l’Université Brown en collaboration avec les Drs Borton et Nurmikko, le système d’enregistrement est connecté à l’implant cérébral pour enregistrer l‘activité électrique et relayer celle-ci en temps réel et sans fil à un ordinateur.
L’ordinateur décode l’activité électrique cérébrale, grâce à des algorithmes spécifiquement développés pour détecter le souhait du singe d’effectuer tel ou tel mouvement en temps réel. Cette « intention » de se mouvoir est transformée en protocole de stimulation de la moelle épinière qui est transmis, là encore sans fil, au stimulateur spinal implantable.
Le stimulateur spinal implantable est du type de ceux communément utilisés pour la stimulation cérébrale profonde (exemples : maladie de Parkinson, tremblement essentiel). Tim Denison et son équipe (Medtronic Inc.) ont développé un nouveau petit logiciel incorporé dans le stimulateur pour recevoir les informations en temps réel. Le stimulateur spinal implantable reçoit le protocole de stimulation sans fil et délivre les instructions de stimulation via l’implant spinal.
L’implant spinal est composé de 16 électrodes préalablement placées chirurgicalement à des endroits précis sur la partie dorsale de la moelle épinière lombaire. Cet implant spinal active de manière synergique les groupes de muscles de la jambe paralysée, permettant la production des mouvements de flexion et d’extension nécessaires à la marche.
(c) EPFL