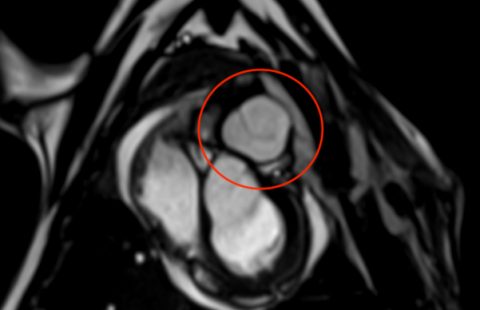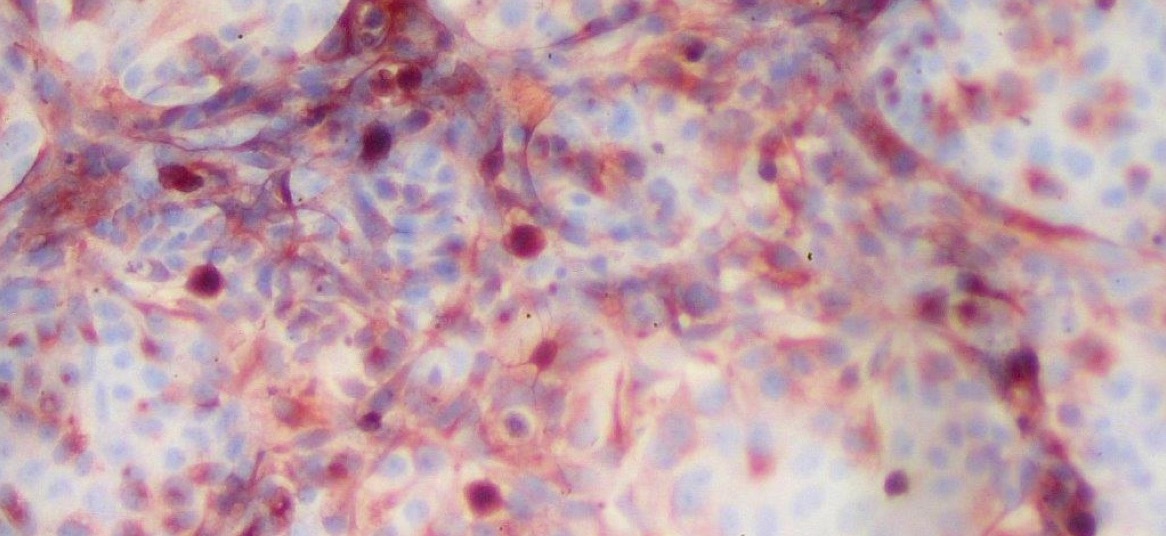
Une tri-culture Minibrain. © Marie-Christine Cumont et Monique Lafon – Institut Pasteur.
Des chercheurs de l’Institut Pasteur, du CNRS et de Sanofi Pasteur viennent de développer une nouvelle méthode alternative à l’expérimentation animale, qui permettra à terme de tester l’innocuité de vaccins comme celui contre la fièvre jaune. Cette démarche originale, repose sur la mise au point d’un dispositif in cellulo utilisant un modèle de culture 3D, le « BBB-Minibrain », pour évaluer l’innocuité de vaccins vivants à usage humain. Ce modèle a été développé par l’Institut Pasteur et une demande de brevet a été déposée par l’Institut Pasteur et l’Inserm. Il permet d’envisager une limitation du recours aux animaux dans le contrôle qualité, notamment pour les tests effectués par l’industrie pharmaceutique pour répondre aux demandes des autorités. Les résultats de cette étude ont été publiés dans la revue Biologicals en mai 2018, et en ligne le 24 mars.
Depuis plusieurs années et suite à la directive européenne 2010/63/EU1, la communauté scientifique cherche activement à réduire le recours à l’expérimentation animale. Néanmoins, cette volonté reste entravée, pour de nombreuses applications, par l’absence d’alternatives acceptées par les agences règlementaires. C’est en particulier le cas des tests règlementaires qui exigent, pour les vaccins vivants viraux comme le vaccin contre la fièvre jaune, de contrôler que les lots de semences utilisés pour produire les lots de vaccins mis sur le marché ne comportent pas un risque neurotoxique. Ces tests sont actuellement effectués chez l’animal en recherchant, dans le système nerveux central, l’apparition de signes cliniques évocateurs d’effets secondaires neurotoxiques.
Dans ce contexte, des chercheurs de l’Institut Pasteur ont mis au point en 2014 un modèle de culture 3D mimant l’interface sang-cerveau de l’homme, le « BBB-Minibrain ». Ce modèle, formé d’une barrière hémato-encéphalique (« blood–brain barrier » – BBB) associée à une culture mixte de neurones, astrocytes et microglie (Minibrain), permet de détecter l’entrée des virus dans le cerveau au travers de la BBB, leur multiplication dans le Minibrain et l’apparition d’éventuels effets neurotoxiques. Il a fait l’objet de la demande de brevet WO2016038123.
Les chercheurs ont proposé d’éprouver la capacité du BBB-Minibrain à repérer et amplifier les rares particules mutantes neuro-invasives et neurovirulentes qui pourraient être présentes dans les lots de semences des vaccins viraux vivants. Pour cela, ils ont choisi d’utiliser deux souches vaccinales du virus de la fièvre jaune, dont la souche à partir de laquelle le vaccin est actuellement produit et qui est dénuée de neurotoxicité.
En collaboration avec les équipes de recherche de Sanofi Pasteur, ils ont démontré que le « BBB-Minibrain » permet d’identifier les rares particules virales qui, à partir des préparations vaccinales, ont acquis la propriété d’entrer dans le cerveau et de s’y multiplier. Ce test devrait donc permettre, à l’avenir, d’écarter les lots de semences qui contiennent des virus mutants capables de pénétrer dans le cerveau et de devenir neuro-virulents.
Comme l’explique Monique Lafon, auteure principale de l’étude et directrice du département de Virologie à l’Institut Pasteur, « le remplacement des tests sur animaux est un défi majeur posé à la recherche. Le modèle BBB-Minibrain est un outil ingénieux qui va nous permettre de mieux analyser les bases de la neurovirulence de ces virus qui colonisent le cerveau par la voie sanguine ».
Ce travail de recherche représente donc une première preuve de concept et de faisabilité de la mise au point d’un test substitutif dans le cadre de la mise en œuvre de la règle des 3Rs. Le travail de développement de ce test est en cours. A terme, l’objectif est que ce nouveau test puisse être validé par les autorités.
Le modèle « BBB-Minibrain » permet d’espérer le développement d’une méthode de remplacement pour la réalisation, par l’industrie pharmaceutique, de tests réglementaires sur les vaccins viraux vivants. Cette méthode vise ainsi à limiter l’utilisation d’animaux tout en assurant un suivi rigoureux des bénéfices et avancées scientifiques réalisés pour la santé humaine.
Anaelle Da Costa est récipiendaire du prix Hub France R&D awards 2017 (November 2017), Sanofi Pasteur et du prix Global R&D awards 2017, we’R hope award, Innovative Post Doctoral Reasearch (May 2018), Sanofi Pasteur.