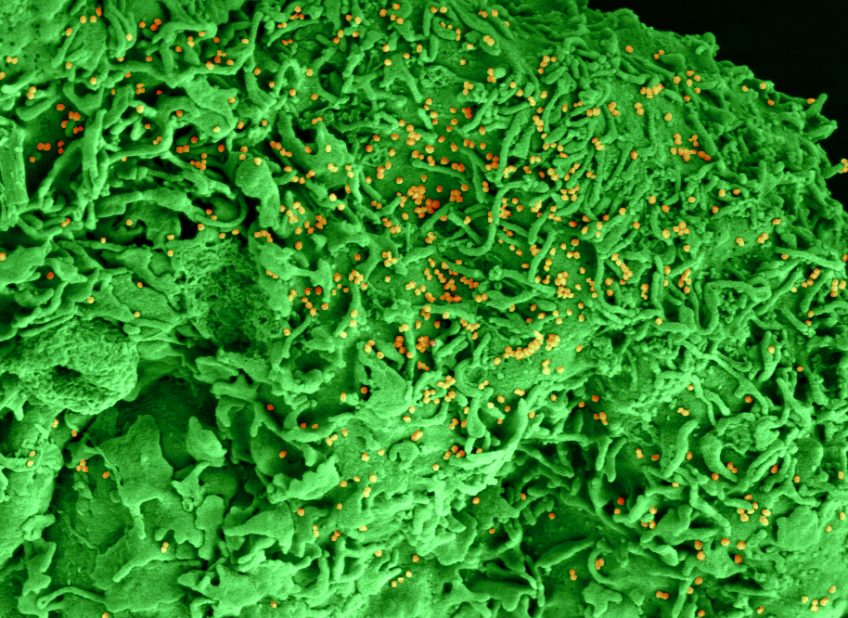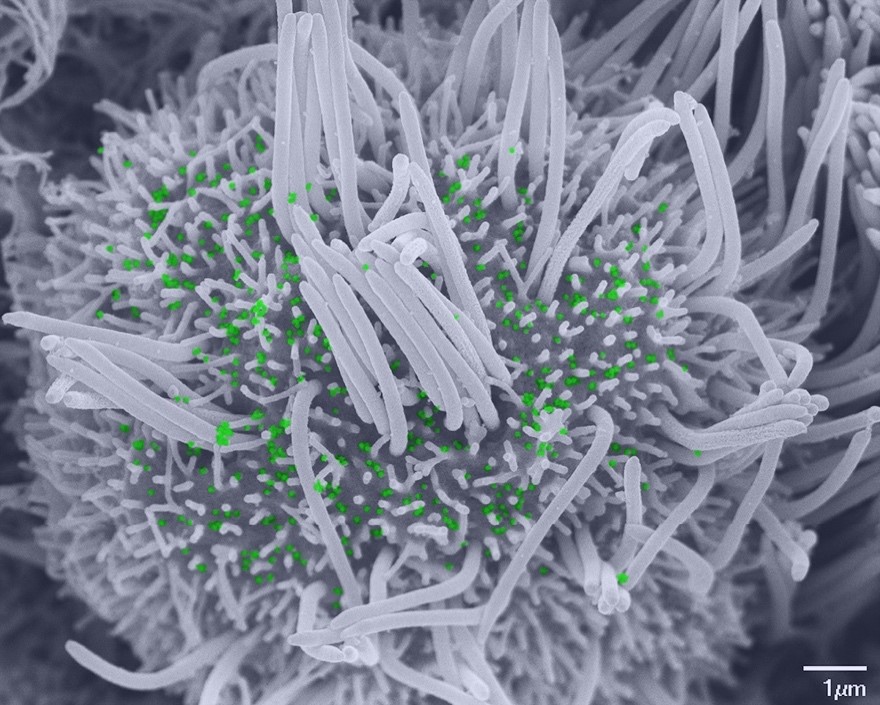
Image par microscopie électronique à balayage d’une cellule ciliée infectée par le SARS-CoV-2, avec quelques cils restants et des particules virales (colorisées en vert) dispersées au niveau de la membrane plasmique.© Vincent Michel, Rémy Robinot, MathieuHubert, Olivier Schwartz, et Lisa Chakrabarti, Institut Pasteur
La Covid-19 est une maladie d’origine virale qui cause des symptômes respiratoires pouvant aller jusqu’à une pneumopathie fatale. Comprendre comment le SARS-CoV-2 se propage dans les voies respiratoires peut aider à identifier les paramètres qui contrôlent la sévérité de l’infection. Des chercheuses et chercheurs de l’Institut Pasteur, du CNRS1 et de l’Inserm ont montré que le SARS-CoV-2 se multiplie efficacement dans les voies respiratoires, qu’il cible principalement les cellules ciliées de l’épithélium et détruit leurs cils. Cette détérioration est associée à une inhibition du mécanisme de clairance mucociliée. Ce mécanisme permet d’évacuer les particules inhalées et protège les voies respiratoires des agents pathogènes. La perte des cils pourrait donc faciliter la propagation du virus plus profondément dans les voies respiratoires, jusqu’à ce qu’il atteigne les alvéoles pulmonaires et y déclenche une pneumopathie. Les résultats de cette étude font l’objet d’un article publié dans Nature Communications le 16 juillet 2021.
L’épithélium des voies respiratoires comprend des cellules en gobelet, qui sécrètent un mucus viscoélastique, et des cellules ciliées, qui déplacent la couche de mucus par le battement coordonné de leurs cils. Les particules inhalées sont piégées dans la couche de mucus et déplacées jusqu’au pharynx où elles sont avalées. Les voies respiratoires possèdent ainsi une fonction d’auto-nettoyage, appelée clairance mucociliée, qui permet d’éviter que les particules inhalées s’accumulent dans les poumons.
Les voies respiratoires représentent la porte d’entrée du SARS-CoV-2, le virus responsable de la Covid-19. L’infection cause dans la plupart des cas des symptômes respiratoires modérés, mais peut dans les cas graves entraîner une détresse respiratoire mortelle. Comprendre comment le SARS-CoV-2 se propage dans les voies respiratoires est essentiel pour identifier les paramètres qui contrôlent la sévérité de la maladie.
Des chercheuses et chercheurs de l’Institut Pasteur, du CNRS et de l’Inserm ont examiné les conséquences fonctionnelles et structurelles de l’infection par le SARS-CoV-2 dans un modèle d’épithélium bronchial in vitro qui mime les conditions naturellement présentes dans les voies respiratoires. Ce modèle intègre les trois types de cellules composant l’épithélium des voies respiratoires : les cellules en gobelet, les cellules ciliées et les cellules basales qui jouent le rôle de cellules souches locales. Les auteurs de l’étude ont observé que le SARS-CoV-2 se multiplie efficacement dans ce système et qu’il cible principalement les cellules ciliées. La multiplication du virus dans ce système induit une altération des cellules ciliées, qui perdent leurs cils et deviennent donc incapables d’effectuer la clairance mucociliée. Ces résultats ont ensuite été confirmés en modèle animal, en collaboration avec les équipes du consortium NeuroCovid à l’Institut Pasteur.
« Ce travail met en évidence un processus qui pourrait faciliter la dissémination du SARS-CoV-2 dans les voies respiratoires. En effet, la perte des cils induite par l’infection virale pourrait limiter l’évacuation des particules virales produites localement, et donc favoriser leur progression plus profondément dans l’arbre respiratoire. Une fois que les particules virales atteignent les alvéoles pulmonaires, elles peuvent alors s’attaquer aux pneumocytes et y déclencher une pneumopathie. » commente Lisa Chakrabarti, co-dernière auteure de l’étude, et responsable du groupe Contrôle des infections virales chroniques dans l’unité Virus et immunité dirigée par Olivier Schwartz à l’Institut Pasteur.
Les résultats de l’étude montrent que la réplication du virus est également associée à une perte précoce du facteur de transcription FoxJ1, qui est important dans la formation et le maintien des cils. Cette perturbation de la régulation de FoxJ1 lors de l’infection par le SARS-CoV-2 pourrait contribuer à expliquer l’altération de la couche ciliée.
« L’altération des cils, et donc, du mécanisme de clairance mucociliée pourrait également favoriser la propagation d’autres pathogènes respiratoires inhalés, et expliquer pourquoi les patients contractant une forme de Covid-19 sévère développent souvent des infections bactériennes ou fongiques secondaires. » explique Lisa Chakrabarti.
Cette étude permet d’avancer dans la compréhension des mécanismes d’infection de la souche initiale du SARS-CoV-2. Ces recherches vont maintenant être élargies à l’étude des variants d’intérêt du virus, pour explorer les mécanismes qui sous-tendent la dissémination accrue de ces variants.
1 Des scientifiques du laboratoire Virologie (CNRS/Institut Pasteur) et du laboratoire Gènes, synapses et cognition (CNRS/Institut Pasteur) sont impliqués
Ces contenus pourraient aussi vous intéresser :
SARS-CoV-2 infection induces the dedifferentiation of multiciliated cells and impairs mucociliary clearance
Nature Communications, 16 juillet 2021
Rémy Robinot 1,2,16, Mathieu Hubert 1,2,16, Guilherme Dias de Melo 3, Françoise Lazarini 4,5, Timothée Bruel 1,2, Nikaïa Smith 6, Sylvain Levallois 7,8, Florence Larrous 3, Julien Fernandes 9, Stacy Gellenoncourt 1,2, Stéphane Rigaud 10, Olivier Gorgette 11, Catherine Thouvenot 11, Céline Trébeau 12, Adeline Mallet 11, Guillaume Duménil 11, Samy Gobaa 13, Raphaël Etournay 12, Pierre-Marie Lledo 4,5, Marc Lecuit 7,8,14, Hervé Bourhy 3, Darragh Duffy 6, Vincent Michel 12,*, Olivier Schwartz 1,2,15,*& Lisa A. Chakrabarti 1,2,*
1 Virus & Immunity Unit, Department of Virology, Institut Pasteur, Paris, France.
2 UMR 3569 CNRS, Paris, France.
3 Lyssavirus Epidemiology and Neuropathology Unit, Institut Pasteur, Paris, France.
4 Perception and Memory Unit, Institut Pasteur, Paris, France.
5 UMR 3571 CNRS, Paris, France.
6 Translational Immunology Lab, Department of Immunology, Institut Pasteur, Paris, France.
7 Biology of Infection Unit, Institut Pasteur, Paris, France.
8 INSERM U1117, Paris, France.
9 UtechS Photonics BioImaging, C2RT, Institut Pasteur, Paris, France.
10 Image Analysis Hub, C2RT, Institut Pasteur, Paris, France.
11 UtechS Ultrastructural BioImaging UBI, C2RT, Institut Pasteur, Paris, France.
12 Institut de l’Audition, Institut Pasteur, INSERM, Paris, France.
13 Biomaterials and Microfluidics Core Facility, Institut Pasteur, Paris, France.
14 Université de Paris, Necker-Enfants Malades University Hospital, Division of Infectious Diseases and Tropical Medicine, APHP, Institut Imagine, Paris, France.
15 Vaccine Research Institute, Créteil, France.
16 These authors contributed equally: Rémy Robinot, Mathieu Hubert.
* Corresponding authors