Contact scientifique
Jacky Goetz Directeur de recherche Inserm Responsable de l’équipe Tumor biomechanics Unité 1109 Immunologie et rhumathologie moléculaire (IRM) +33 3 68 85 40 11 rf.mesni@zteog.ykcaj
Des billes fluorescentes sont filmées à très haute vitesse, et analysées pour suivre leur trajectoire, pour comprendre l’influence des forces fluidiques sur l’arrêt d’une cellule tumorale sur un tapis de cellules endothéliales. ©Harlepp S. /Goetz J
Les cellules tumorales circulantes utilisent les réseaux lymphatiques et sanguins pour se disséminer dans l’organisme et former des métastases à distance de la tumeur primaire. Jacky Goetz, chercheur Inserm, et son équipe Tumor biomechanics au sein du laboratoire Immunologie et rhumatologie moléculaire (Inserm/Université de Strasbourg) ont contribué à montrer que les propriétés des flux de ces liquides biologiques influent énormément sur le risque d’apparition de ces métastases. Ils ont notamment observé que le ralentissement du flux sanguin au niveau de la ramification des artères permettait aux cellules cancéreuses de s’accrocher à la paroi vasculaire et de s’extraire des vaisseaux pour aller coloniser les tissus. L’équipe de recherche fait le point sur ses travaux dans une revue de littérature publiée dans Nature Reviews Cancer.
Les cellules cancéreuses exploitent largement les fluides biologiques pour se disséminer dans l’organisme et former des métastases à distance des tumeurs primaires. Ainsi, si certaines empruntent directement la circulation sanguine, d’autres la rejoignent en s’échappant d’abord de la tumeur par le liquide interstitiel et le réseau lymphatique pour coloniser ensuite les ganglions lymphatiques avant de rejoindre le sang.
Jacky Goetz, directeur de recherche Inserm de l’équipe Tumor biomechanics au sein du laboratoire Immunologie et rhumatologie moléculaire (Inserm/Université de Strasbourg), s’intéresse depuis plusieurs années à ces mécanismes. Ses travaux sont mis à l’honneur dans Nature Reviews Cancer.
Les chercheurs ont ainsi constaté que les cellules cancéreuses circulent rapidement dans les grandes artères sans pouvoir s’arrêter. En revanche, quand le diamètre des artères diminue et que le réseau sanguin se ramifie, le flux ralentit nettement, ce qui permet aux cellules tumorales de s’accrocher à la paroi des vaisseaux puis de s’en extraire pour aller coloniser les tissus. L’équipe de recherche a identifié un certain nombre d’endroits préférentiels (hotspots) pour cette extraction qui correspondent exactement aux sites métastatiques les plus fréquents chez l’humain, là où le réseau sanguin est formé de nombreux petits capillaires ; le cerveau, les poumons ou encore le foie. Ces travaux ont été confirmés en collaboration avec des équipes allemandes, dans une cohorte de 100 patients atteints de métastases cérébrales. L’équipe de Jacky Goetz a également découvert qu’il était possible chez le poisson zèbre de modifier l’emplacement des hotspots et donc des métastases en modifiant la vitesse du flux sanguin.
Toujours chez le poisson zèbre, les chercheurs ont observé que la formation de métastases était précédée par la libération de vésicules extracellulaires provenant de la tumeur. Celles-ci contiennent des protéines, de l’ADN ou encore des ARN et semblent agir comme de véritables éclaireurs pour les cellules tumorales, peut-être pour préparer leur implantation. L’équipe de recherche a pu montrer que le comportement dans le sang de ces vésicules est similaire à celui des cellules tumorales, et dépend également de la force du flux sanguin.
Enfin, les chercheurs ont pu corréler la force du flux avec l’action de deux protéines situées à la surface des cellules tumorales et ne pouvant agir que lorsque le flux sanguin est ralenti. La première, CD44 agit comme un frein en s’accrochant à la paroi vasculaire. La seconde, l’intégrine α5ß1 permet à la cellule de s’arrêter et de s’extraire du réseau sanguin. Chez le poisson zèbre et la souris, l’absence d’intégrine α5ß1 ralentit fortement la croissance des métastases.
« L’ensemble de ces travaux montre que pour prévenir l’apparition des métastases, il ne faut pas se focaliser seulement sur les propriétés intrinsèques de la tumeur, de son microenvironnement ou de celui des métastases, mais tenir compte aussi du rôle des fluides biologiques. Empêcher l’arrêt des cellules circulantes ou leur attachement à la paroi pourrait par exemple réduire ce risque », conclut Jacky Goetz.
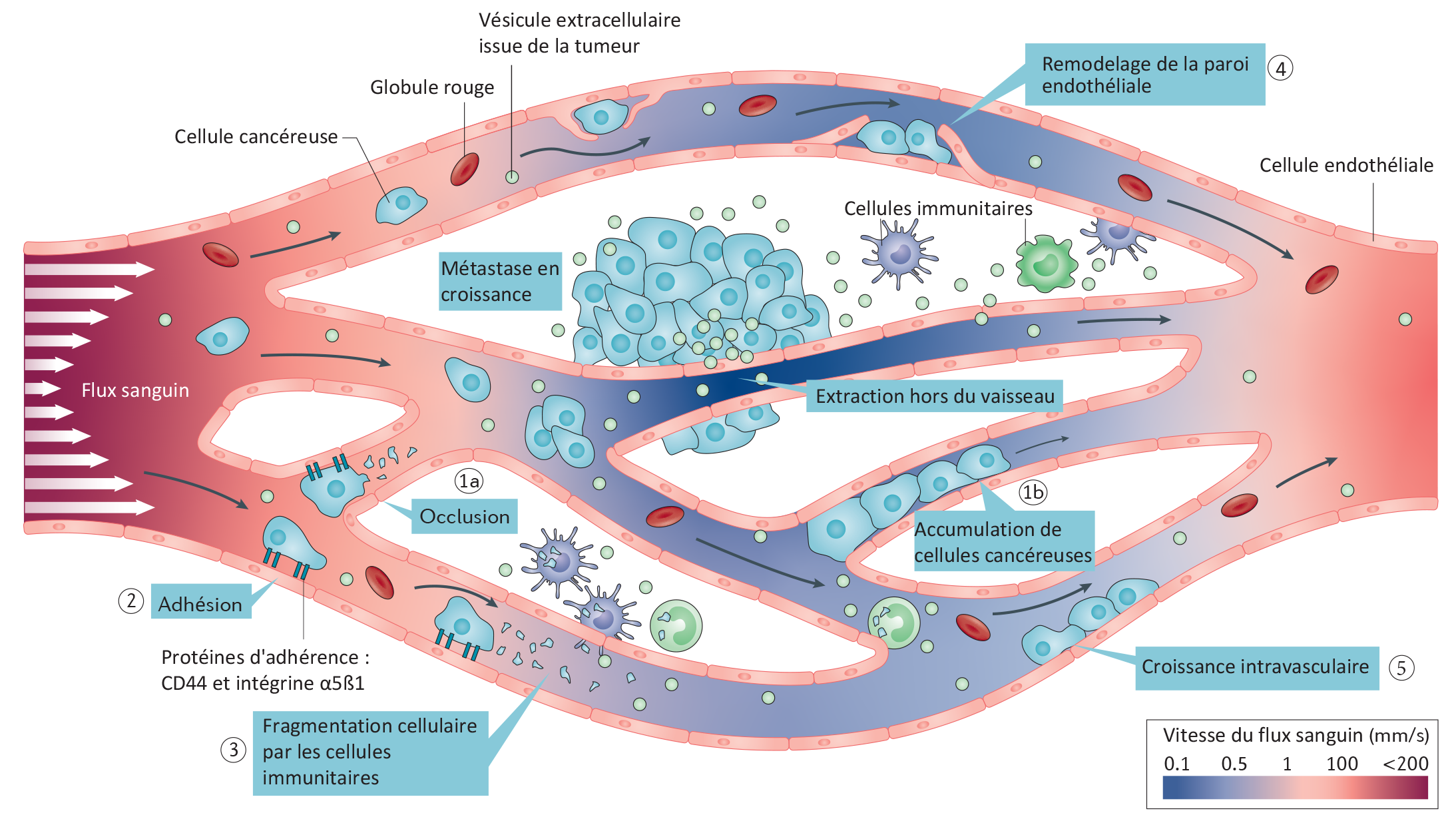
Légende : Circulation, adhérence et extraction des cellules et vésicules tumorales pour former une métastase en fonction de la variation de la vitesse du flux sanguin. ©Jacky Goetz / Nature Reviews Cancer, 2019
Jacky Goetz Directeur de recherche Inserm Responsable de l’équipe Tumor biomechanics Unité 1109 Immunologie et rhumathologie moléculaire (IRM) +33 3 68 85 40 11 rf.mesni@zteog.ykcaj
Fluids and their mechanics in tumour transit: shaping metastasis Gautier Follain1–3, 7, David Herrmann5–7, Sébastien Harlepp1–3, 7, Vincent Hyenne1-4, 7, Naël Osmani1–3, 7, Sean Warren5–6, Paul Timpson5–6 and Jacky G. Goetz1–3 1 Inserm UMR_S1109, Tumor Biomechanics, Strasbourg, France. 2 Université de Strasbourg, Strasbourg, France. 3 Fédération de Médecine Translationnelle de Strasbourg (FMTS), Strasbourg, France. 4 CNRS SNC 505, Strasbourg 67200, France. 5 The Kinghorn Cancer Centre, Garvan Institute of Medical Research, Sydney, New South Wales, Australia. 6 St. Vincent’s Clinical School, Faculty of Medicine, University of New South Wales, Sydney, New South Wales, Australia. 7 These authors contributed equally: Gautier Follain, David Herrmann, Sébastien Harlepp, Vincent Hyenne, Naël Osmani Nature Reviews Cancer : https://doi.org/10.1038/s41568-019-0221-x