Contact scientifique
Serge Picaud Tel : +33 (0) 1 53 46 25 04 Email : rf.mresni@duacip.egres
Contact Presse
rf.mresni@esserp

Adobe Stock
Depuis plusieurs années, la perspective de restaurer la vision des patients souffrant de dégénérescence maculaire liée à l’âge (DMLA) ou de rétinopathies pigmentaire devient de plus en plus tangible. De nombreux chercheurs ont ainsi tenté de développer une rétine artificielle permettant de lutter contre la cécité. Dans une nouvelle étude, une équipe de l’Institut de la vision (Inserm-CNRS- Sorbonne Université) menée par le chercheur Inserm Serge Picaud a montré, dans des modèles animaux, qu’un dispositif fabriqué par la société Pixium Vision permettrait d’induire une perception visuelle de haute résolution. Leurs résultats, publiés dans Nature Biomedical Engineering, ont ouvert la voie à des essais cliniques chez l’Homme.
Maladie du vieillissement particulièrement invalidante, la dégénérescence maculaire liée à l’âge (DMLA) se caractérise par une dégradation de la rétine pouvant mener à une perte de la vision centrale. Jusqu’à 30 % des personnes âgées de plus de 75 ans seraient concernées. Depuis des années, plusieurs groupes de chercheurs œuvrent pour développer une rétine artificielle qui pourrait redonner la vue à ces patients, ainsi qu’aux individus atteints de rétinopathie pigmentaire.
La rétine est composée de cellules sensibles à la lumière appelées photorécepteurs, dont le but est de transformer les signaux lumineux reçus par l’œil en signaux électriques acheminés vers le cerveau. Ce sont ces cellules qui sont détruites au cours de ces pathologies, ce qui peut mener à la cécité. Le principe d’une rétine artificielle est simple : elle est développée pour se substituer à ces photorécepteurs. Le dispositif est en fait constitué d’implants fixés sous la rétine et composés d’électrodes qui viennent stimuler les neurones rétiniens pour porter les messages au cerveau.
Deux dispositifs de ce type, l’Argus II (Second sight, Etats-Unis) et le Retina Implant (AG, Allemagne), ont déjà largement été implantés. « Néanmoins, ces deux entreprises se désengagent petit à petit du marché, notamment parce que le rendu pour les patients n’était pas suffisant pour cibler les patients atteints de DMLA. Les patients parvenaient à voir des signaux lumineux, mais ceux qui arrivaient à distinguer des lettres étaient très minoritaires », souligne Serge Picaud.
Réinventer le dispositif pour le rendre plus performant : telle a été l’ambition de ce chercheur Inserm et de ses collègues. Portée par l’entreprise Pixium Vision, leur rétine artificielle, inventée par le Pr Palanker à l’Université de Stanford (USA), est un dispositif sans fil, moins complexe, contrairement aux dispositifs précédents. De plus, cet implant introduit un retour local du courant induisant ainsi une meilleure résolution des images perçues par l’œil. Enfin, l’image est projetée sur l’implant par une stimulation infrarouge qui active des photodiodes reliées aux électrodes, permettant une stimulation plus directe des neurones rétiniens.
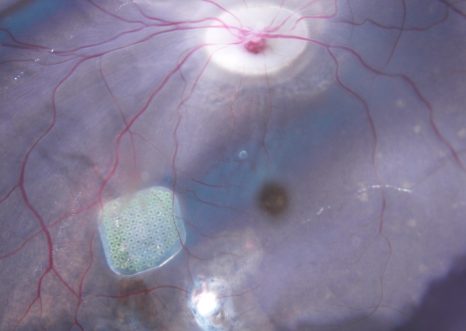
La rétine artificielle développée par Pixium Vision. Crédits : Serge Picaud
Dans leur étude publiée dans Nature Biomedical Engineering, Serge Picaud et ses collègues ont testé ce dispositif chez des primates non-humains, montrant qu’il permet de restaurer une acuité visuelle significative. Des tests in vitro ont d’abord montré que chaque pixel active des cellules différentes dans la rétine. Cette sélectivité se traduit par une très haute résolution, de sorte que des animaux implantés peuvent percevoir l’activation d’un seul pixel de l’implant dans un test de comportement.
La haute résolution de ces implants a permis d’ouvrir la voie à l’implantation du dispositif chez cinq patients français atteints de DMLA dans le service de José-Alain Sahel à la Fondation ophtalmologique A. de Rothschild. Les premiers résultats indiquent que ceux-ci retrouvent peu à peu une vision centrale. Ils sont en mesure de percevoir des signaux lumineux, et certains peuvent même identifier des séquences de lettres, de plus en plus rapidement au cours du temps.
« L’objectif est maintenant de faire un essai de phase 3 chez un groupe plus conséquent de patients atteints de DMLA. Si la rétine artificielle fonctionne chez eux, nous pensons qu’il n’y a pas de raison pour qu’elle ne fonctionne pas chez des patients souffrant de rétinopathie pigmentaire, maladie également liée à la dégénérescence des photorécepteurs », conclut Serge Picaud.
Serge Picaud Tel : +33 (0) 1 53 46 25 04 Email : rf.mresni@duacip.egres
rf.mresni@esserp
Behavioural responses to a photovoltaic subretinal prosthesis implanted in nonhuman primates Paul-Henri Prévot1, Kevin Gehere1, Fabrice Arcizet1, Himanshu Akolkar 1, Mina A. Khoei1, Kévin Blaize1, Omar Oubari1, Pierre Daye1, Marion Lanoë1, Manon Valet1, Sami Dalouz1, Paul Langlois1, Elric Esposito1, Valérie Forster1, Elisabeth Dubus1, Nicolas Wattiez2, Elena Brazhnikova1, Céline Nouvel-Jaillard1, Yannick LeMer3, Joanna Demilly4, Claire-Maëlle Fovet4, Philippe Hantraye4, Morgane Weissenburger2, Henri Lorach5, Elodie Bouillet6, Martin Deterre6, Ralf Hornig6, Guillaume Buc6, José-Alain Sahel1,3,7,8, Guillaume Chenegros1, Pouget2,9, Ryad Benosman1,7,9 and Serge Picaud 1,9* 1 Institut de la Vision, Sorbonne Université, INSERM and CNRS, Paris, France. 2 Institut du Cerveau et de la Moelle Epinière – CNRS UMR 7225, Hôpital de la PitiéSalpêtrière, Paris, France. 3 Fondation Ophtalmologique A. de Rothschild, Paris, France. 4 Molecular Imaging Research Center (MIRCen), Fontenayaux-Roses, France. 5 Hansen Experimental Physics Laboratory, Stanford University, Stanford, CA, USA. 6 Pixium Vision, Paris, France. 7 Department of Ophthalmology, The University of Pittsburgh School of Medicine, Pittsburgh, PA, USA. 8 CHNO des Quinze-Vingts, DHU Sight Restore, INSERM-DGOS CIC 1423, Paris, France. 9 These authors contributed equally: Pierre Pouget, Ryad Benosman, Serge Picaud DOI : 10.1038/s41551-019-0484-2