Contact scientifique
Carole Peyssonnaux Unité Inserm 1016 / CNRS UMR8104 – Institut Cochin rf.mresni@xuannossyep.elorac
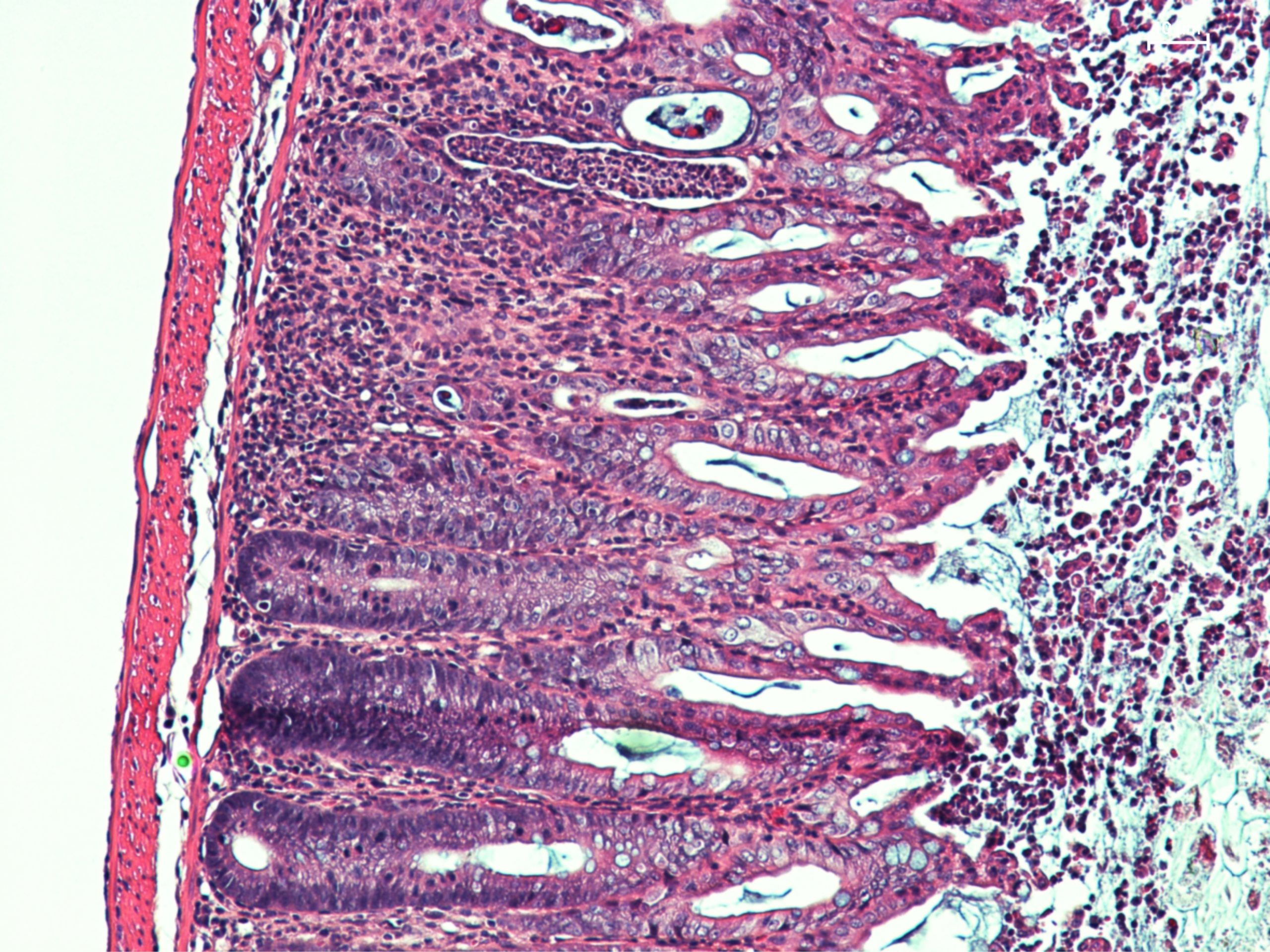
Cette image obtenue par microscope d’une coupe intestinale de souris témoigne de lésions importantes, de signes inflammatoires et d’une cicatrisation dysfonctionnelle de la muqueuse intestinale. ©Sonnenberg Lab
Les inflammations de l’intestin touchent de nombreux patients, avec des perspectives thérapeutiques souvent réduites. Le rôle du fer dans ces processus inflammatoires est de mieux en mieux documenté, permettant d’ouvrir de nouvelles pistes de traitements. Une étude collaborative entre l’équipe dirigée par la directrice de recherche Inserm Carole Peyssonnaux à l’Institut Cochin (Inserm/CNRS/Université de Paris) et l’équipe de Greg Sonnenberg à New York (Weill Cornell Medicine) montre que l’hormone qui régule le niveau de fer dans l’organisme est produite par des cellules immunitaires lors d’une inflammation de l’intestin, et qu’elle contribue à réparer les lésions de la muqueuse intestinale. Ces travaux sont publiés dans la revue Science.
Les infections, les maladies chroniques inflammatoires de l’intestin (MICI) comme la maladie de Crohn ainsi que les cancers colorectaux sont associés à une inflammation de l’intestin. Chez les patients, la muqueuse intestinale peut alors être endommagée, et des saignements ainsi qu’une distribution altérée du fer dans l’organisme sont souvent observés.
Depuis plusieurs années, la directrice de recherche Inserm Carole Peyssonnaux et son équipe au sein de l’Institut Cochin (Inserm/CNRS/Université de Paris) s’intéressent au rôle de l’hepcidine dans des contextes pathologiques. Cette hormone est régulatrice du métabolisme du fer dans l’organisme et est principalement produite par le foie. Les chercheurs avaient néanmoins déjà montré que dans le cas de certaines pathologies, l’hepcidine est également sécrétée au niveau d’autres tissus.
Leur nouvelle étude, réalisée en collaboration avec l’équipe de Gregory F. Sonnenberg de l’université de Cornell aux Etats-Unis et publiée en avril 2020 dans le journal Science, montre que dans un contexte d’inflammation intestinale, l’hepcidine est aussi exprimée par des cellules immunitaires particulières, les cellules dendritiques de l’intestin.
Les scientifiques ont d’abord étudié le processus de cicatrisation intestinale chez plusieurs groupes de souris présentant toutes une inflammation de l’intestin. Pour l’un de ces groupes de souris, le gène codant pour l’hepcidine n’était pas exprimé. Comparé aux autres groupes de souris pour qui ce gène fonctionnait normalement, cela se traduisait par une perte de poids continue plus importante, mais aussi par une cicatrisation moins efficace de la muqueuse intestinale.
Les chercheurs ont ainsi confirmé que l’hepcidine joue un rôle important pour la guérison des lésions de l’intestin. Ils se posaient néanmoins encore la question de savoir si c’est l’hepcidine normalement sécrétée par le foie qui avait cet effet bénéfique, ou si dans ce contexte pathologique, cette hormone régulatrice du fer était produite au niveau d’autres organes.
Grâce à l’utilisation de modèles de souris où le gène codant l’hepcidine était uniquement déficient dans le foie, les chercheurs ont pu montrer, de manière surprenante, que le processus de cicatrisation était indépendant de la production hépatique d’hepcidine. Suite à une lésion intestinale et dans un contexte d’inflammation, les cellules dendritiques locales de l’intestin étaient la source dominante de production de cette hormone.
Pour déterminer si ce phénomène se produit également chez l’homme, les chercheurs se sont enfin intéressés à des d’échantillons prélevés sur des patients pédiatriques atteints de MICI. Ils ont confirmé que les cellules dendritiques de l’intestin humain produisent également de l’hepcidine en réponse à une lésion. Cette voie pourrait donc s’avérer cliniquement importante chez les personnes atteintes de MICI. « Notre étude suggère que l’hepcidine aurait un rôle protecteur car en cas de suppression du gène qui code pour cette hormone la sévérité de la maladie est plus importante. L’utilisation de traitements mimétiques de l’hepcidine pourrait donc avoir un rôle thérapeutique pour favoriser la séquestration de fer, réduire sa disponibilité pour les bactéries qui prolifèrent dans l’intestin et favoriser la guérison des lésions », conclut Carole Peyssonnaux.
Carole Peyssonnaux Unité Inserm 1016 / CNRS UMR8104 – Institut Cochin rf.mresni@xuannossyep.elorac
Dendritic cell-derived hepcidin sequesters iron from the microbiota to promote mucosal healing Nicholas J. Bessman1,2,3, Jacques R. R. Mathieu4,5*, Cyril Renassia4,5*, Lei Zhou1,2,3, Thomas C. Fung1,2,3, Keith C. Fernandez1,2,3, Christine Austin6, Jesper B. Moeller1,2,3,7, Sara Zumerle4,5†, Sabine Louis4,5, Sophie Vaulont4,5, Nadim J. Ajami8, Harry Sokol9, Gregory G. Putzel1, Tara Arvedson10, Robbyn E. Sockolow11, Samira Lakhal-Littleton12, Suzanne M. Cloonan13,14, Manish Arora6, Carole Peyssonnaux4,5‡, Gregory F. Sonnenberg1,2,3‡ 1Jill Roberts Institute for Research in Inflammatory Bowel Disease (JRI), Weill Cornell Medicine, Cornell University, New York, NY, USA. 2 Joan and Sanford I. Weill Department of Medicine, Division of Gastroenterology and Hepatology, Weill Cornell Medicine, Cornell University, New York, NY, USA. 3 Department of Microbiology and Immunology, Weill Cornell Medicine, Cornell University, New York, NY, USA. 4Université de Paris, INSERM U1016, Institut Cochin, CNRS UMR8104, 75014 Paris, France. 5 Laboratory of Excellence GR-Ex, Paris,France. 6 Department of Environmental Medicine and Public Health, Icahn School of Medicine at Mount Sinai, New York, NY 10029, USA. 7 Department of Molecular Medicine, University of Southern Denmark, Odense, Denmark. 8 MD Anderson Cancer Center, Houston, TX, USA. 9 Sorbonne Université, Inserm, Centre de Recherche Saint-Antoine, CRSA, AP-HP, Hôpital Saint Antoine, Service de Gastroenterologie, F-75012 Paris, France. 10 Department of Oncology Research, Amgen Inc., Thousand Oaks, CA, USA. 11 Department of Pediatrics, Division of Gastroenterology and Nutrition, Weill Cornell Medicine, Cornell University, New York, NY, USA. 12 Department of Physiology, Anatomy and Genetics, University of Oxford, Oxford OX1 3PT, UK. 13 Division of Pulmonary and Critical Care Medicine, Weill Cornell Medicine, Cornell University, New York, NY, USA. 14Trinity College Dublin, Dublin, Ireland. Science, Avril 2020 DOI : 10.1126/science.aau6481