Contact scientifique
Erwan Bézard
Directeur de recherche Inserm
Institut des maladies neurodégénératives (CNRS/université de Bordeaux)
Téléphone sur demande
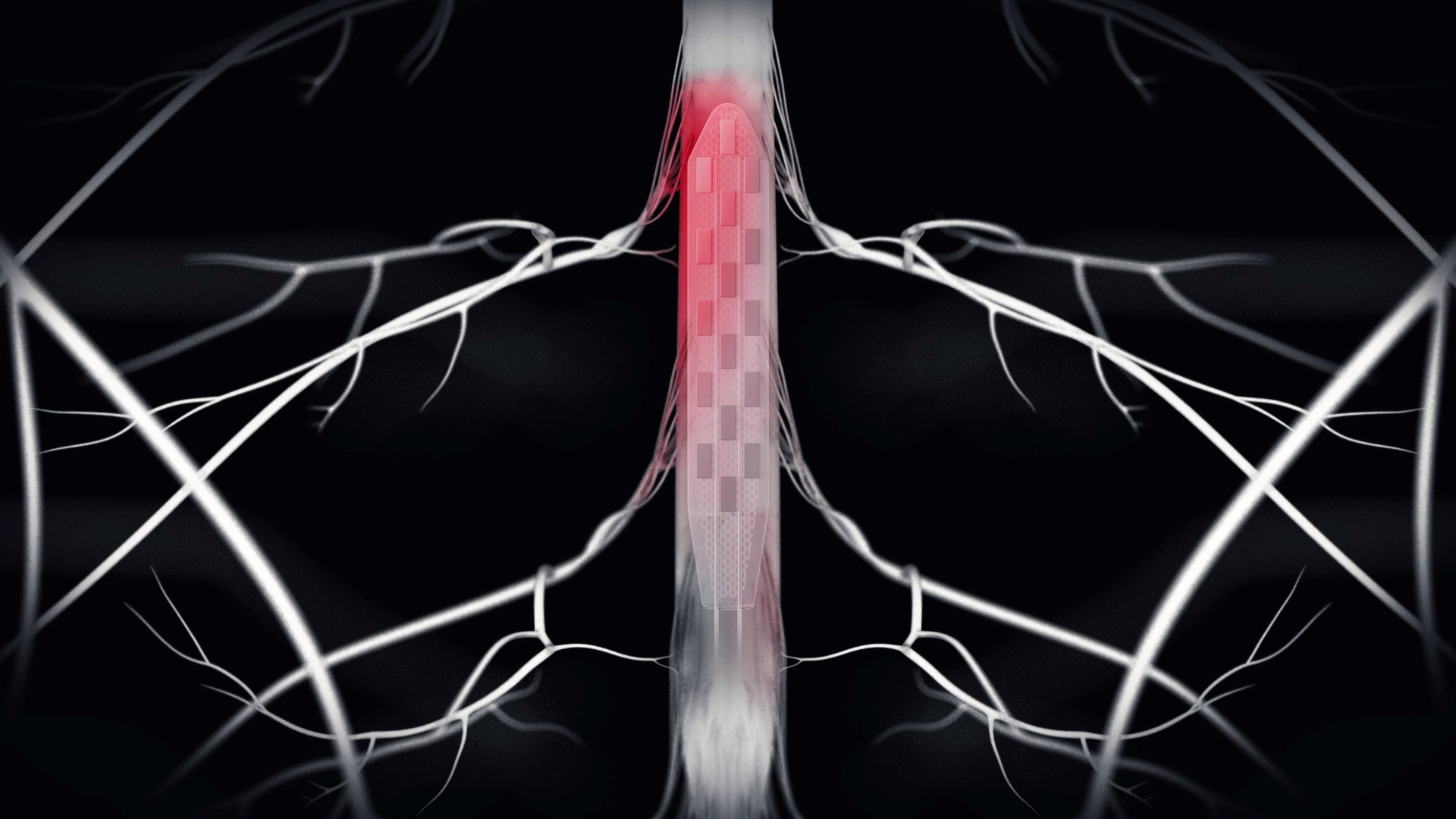 Contrairement aux traitements conventionnels de la maladie de Parkinson, cette neuroprothèse vise la zone de la moelle épinière responsable de l’activation des muscles des jambes pendant la marche. © CHUV
Contrairement aux traitements conventionnels de la maladie de Parkinson, cette neuroprothèse vise la zone de la moelle épinière responsable de l’activation des muscles des jambes pendant la marche. © CHUV
Des neuroscientifiques de l’Inserm, du CNRS et de l’université de Bordeaux en France, avec des chercheurs et neurochirurgiens suisses (EPFL/CHUV/UNIL), ont conçu et testé une « neuroprothèse » destinée à corriger les troubles de la marche associés à la maladie de Parkinson. Dans une étude publiée dans Nature Medicine, les scientifiques détaillent le processus de développement de la neuroprothèse utilisée pour traiter un premier patient atteint de la maladie de Parkinson, lui permettant de marcher avec fluidité, confiance et sans chute.
Des troubles de la marche invalidants surviennent chez environ 90 % des personnes qui présentent un stade avancé de la maladie de Parkinson. Ces troubles de la marche résistent souvent aux traitements actuellement disponibles. Développer de nouvelles stratégies permettant aux patients de remarcher avec fluidité, en écartant le risque de chute, constitue donc une priorité pour les équipes de recherche qui travaillent sur cette maladie depuis de longues années.
C’est le cas d’Erwan Bézard, neuroscientifique à l’Inserm, et de son équipe à l’Institut des maladies neurodégénératives (CNRS/Université de Bordeaux), dont le travail porte notamment sur la compréhension des mécanismes pathogéniques à l’origine de la maladie de Parkinson et sur le développement de stratégies pour rétablir la motricité dans différentes pathologies. Depuis plusieurs années, il collabore avec une équipe suisse dirigée les Pr Grégoire Courtine, neuroscientifique, et Jocelyne Bloch, neurochirurgienne, spécialisés dans le développement de stratégies de neuromodulation de la moelle épinière.
En 2016, l’équipe franco-suisse avait par exemple déjà publié dans Nature des travaux montrant l’efficacité d’une interface cerveau-moelle épinière – dite « neuroprothèse » – pour restaurer le fonctionnement d’un membre paralysé suite à une lésion de la moelle épinière. Les résultats prometteurs avaient incités les scientifiques à poursuivre leurs efforts et laissaient espérer des effets bénéfiques dans la maladie de Parkinson avec un dispositif similaire.
Éviter les chutes et le freezing
Dans cette nouvelle étude, l’équipe a donc mis au point une neuroprothèse comparable pour pallier les chutes et le phénomène de freezing – quand les pieds restent collés au sol pendant la marche – parfois associé à la maladie de Parkinson.
Contrairement aux traitements conventionnels de la maladie de Parkinson, qui ciblent les régions du cerveau directement touchées par la perte des neurones producteurs de dopamine, cette neuroprothèse vise la zone de la moelle épinière responsable de l’activation des muscles des jambes pendant la marche, qui n’est a priori pas directement affectée par la maladie de Parkinson. Néanmoins, la moelle épinière est sous le contrôle volontaire du cortex moteur, dont l’activité est modifiée par la perte des neurones dopaminergiques.
S’appuyant sur leur expertise complémentaire, les équipes française et suisse ont pu développer et tester la neuroprothèse dans un modèle de primate non humain reproduisant les déficits locomoteurs dus à la maladie de Parkinson. Le dispositif a non seulement permis d’atténuer les déficits locomoteurs, mais aussi de rétablir la capacité de marche dans ce modèle en diminuant les phénomènes de freezing.
« L’idée de développer une neuroprothèse stimulant électriquement la moelle épinière pour harmoniser la démarche et corriger les troubles locomoteurs de patients parkinsoniens est le fruit de plusieurs années de recherche sur le traitement de la paralysie due aux lésions médullaires », explique Erwan Bézard, directeur de recherche Inserm à l’Institut des maladies neurodégénératives (université de Bordeaux/CNRS).
« Des tentatives précédentes de stimulation de la moelle ont échoué car elles stimulaient en bloc les centres locomoteurs sans tenir compte de la physiologie. Dans le cas présent, il s’agit d’une stimulation qui se superpose au fonctionnement naturel des neurones de la moelle en stimulant, avec une coordination spatiotemporelle, les différents groupes musculaires responsables de la marche », ajoutent Grégoire Courtine et Jocelyne Bloch, codirecteurs de NeuroRestore, le centre de recherche installé en Suisse romande.
Ces résultats prometteurs ont permis d’ouvrir la voie à un développement clinique, pour tester le dispositif chez un patient.
Une amélioration grâce à la neuroprothèse
Un premier patient, âgé de 62 ans, et vivant avec la maladie depuis trois décennies, a ainsi été opéré il y a deux ans au Centre hospitalier universitaire vaudois (CHUV), à Lausanne. Au cours d’une intervention neurochirurgicale de précision, Marc, originaire de Bordeaux, a été équipé de cette nouvelle neuroprothèse, constituée d’un champ d’électrodes placé contre la région de sa moelle épinière qui contrôle la marche et d’un générateur d’impulsions électriques implanté sous la peau de son abdomen.
Grâce à la programmation ciblée des stimulations de la moelle épinière qui s’adaptent en temps réel à ses mouvements, Marc a rapidement vu ses troubles de la marche s’estomper. Après une rééducation de quelques semaines avec la neuroprothèse, il a retrouvé une marche presque normale.
Cette neuroprothèse ouvre donc de nouvelles perspectives pour traiter les troubles de la marche dont souffrent de nombreuses personnes atteintes de la maladie de Parkinson. Toutefois, à ce stade, ce concept thérapeutique a démontré son efficacité chez une seule personne, avec un implant qui doit encore être optimisé pour un déploiement à grande échelle.
Les scientifiques travaillent donc à la mise au point d’une version commerciale de la neuroprothèse[1] intégrant toutes les fonctionnalités indispensables pour une utilisation quotidienne optimale. Des essais cliniques sur un plus grand nombre de patients doivent également démarrer dès l’année prochaine[2].
« Notre ambition est de généraliser l’accès à cette technologie innovante afin d’améliorer significativement la qualité de vie des patients atteints de la maladie de Parkinson, partout dans le monde », concluent les chercheurs.
[1] En partenariat avec la compagnie ONWARD Medical, une entreprise installée en Suisse qui développera ces implants.
[2] Grâce à un don d’un million de dollars de la Michael J. Fox Foundation for Parkinson’s research, le centre NeuroRestore va initier des essais cliniques sur six nouveaux patients dès l’année prochaine. Ces essais visent non seulement à valider la technologie développée en collaboration avec ONWARD, mais aussi à identifier les profils de patients les plus susceptibles de bénéficier de cette thérapie innovante. Fondée par l’acteur Michael J. Fox (Back to the future), lui-même atteint de la maladie de Parkinson, cette fondation est le principal donateur privé dans le domaine de la recherche sur la maladie de Parkinson.
Erwan Bézard
Directeur de recherche Inserm
Institut des maladies neurodégénératives (CNRS/université de Bordeaux)
Téléphone sur demande
A spinal cord neuroprosthesis for locomotor deficits due to Parkinson’s disease
Nature Medicine, Novembre 2023
DOI : https://doi.org/10.1038/s41591-023-02584-1
Tomislav Milekovic 1,2,3,4,5,25, Eduardo Martin Moraud 2,3,4,25, Nicolo Macellari1,2,3,4,25, Charlotte Moerman 2,3,4,25, Flavio Raschellà1,6,25, Shiqi Sun 1,2,3,4,25, Matthew G. Perich 5,25, Camille Varescon1,2,3,4, Robin Demesmaeker 1,2,3,4,Alice Bruel7, Léa N. Bole-Feysot1,2,3,4, Giuseppe Schiavone 1,8, Elvira Pirondini2,3,9,10, Cheng YunLong11,12,13, Li Hao11,12,13, Andrea Galvez1,2,3,4, Sergio Daniel Hernandez-Charpak 1,2,3,4, Gregory Dumont1,2,3,4, Jimmy Ravier1,2,3,4, Camille G. Le Goff-Mignardot1,2,3,4, Jean-Baptiste Mignardot1,2,3,4, Gaia Carparelli1,2,3,4, Cathal Harte1,2,3,4, Nicolas Hankov1,2,3,4, Viviana Aureli1,2,3,4, Anne Watrin14, Hendrik Lambert14, David Borton 1,2,3,4,15, Jean Laurens1,16, Isabelle Vollenweider1,2,3,4, Simon Borgognon 1,2,3,4, François Bourre17,18, Michel Goillandeau17,18, Wai Kin D. Ko11,12,13, Laurent Petit 17,18, Qin Li11,12,13, Rik Buschman19, Nicholas Buse19, Maria Yaroshinsky20, Jean-Baptiste Ledoux 21, Fabio Becce 21, Mayté Castro Jimenez 22, Julien F. Bally 22, Timothy Denison23, Dominique Guehl17,18, Auke Ijspeert 7, Marco Capogrosso 1,2,3,4,9, Jordan Squair1,2,3,4, Leonie Asboth 1,2,3,4, Philip A. Starr 20, Doris D. Wang20, Stéphanie P. Lacour 1,8, Silvestro Micera 1,6,24, Chuan Qin12, Jocelyne Bloch 1,2,3,4,26 , Erwan Bezard 9,10,17,18,26 & G. Courtine 1,2,3,4,26
1 NeuroX Institute, School of Life Sciences, Ecole Polytechnique Federale de Lausanne (EPFL),Geneva, Switzerland.
2 Department of Clinical Neurosciences, Lausanne University Hospital (CHUV) and University of Lausanne (UNIL), Lausanne, Switzerland.
3 NeuroRestore, Defitech Center for Interventional Neurotherapies, EPFL/CHUV/UNIL, Lausanne, Switzerland.
4 Department of Neurosurgery, CHUV, Lausanne, Switzerland.
5 Department of Fundamental Neuroscience, Faculty of Medicine, University of Geneva, Geneva, Switzerland.
6 NeuroX Institute, School of Bioengineering, EPFL, Lausanne, Switzerland.
7 Institute of Bioengineering, School of Engineering, EPFL, Lausanne, Switzerland.
8 Laboratory for Soft Bioelectronic Interfaces (LSBI), NeuroX Institute, EPFL, Lausanne, Switzerland.
9 Rehab and Neural Engineering Labs, University of Pittsburgh, Pittsburgh, PA, USA.
10 Department of Physical Medicine and Rehabilitation, University of Pittsburgh, Pittsburgh, PA, USA.
11 Motac Neuroscience, UK-M15 6WE, Manchester, UK.
12 China Academy of Medical Sciences, Beijing, China.
13 Institute of Laboratory Animal Sciences, Manchester, UK.
14 ONWARD Medical, Lausanne, Switzerland.
15 School of Engineering, Carney Institute for Brain Science, Brown University, Providence, RI, USA.
16 Department of Neuroscience, Baylor College of Medicine, Houston, TX, USA.
17 Universite de Bordeaux, Institut des Maladies Neurodegeneratives, UMR 5293, Bordeaux, France.
18 CNRS, Institut des Maladies Neurodegeneratives, UMR 5293, Bordeaux, France.
19 Medtronic, Minneapolis, USA.
20 Department of Neurological Surgery, University of California San Francisco, San Francisco, CA, USA.
21 Department of Diagnostic and Interventional Radiology, CHUV/UNIL, Lausanne, Switzerland.
22 Department of Neurology, CHUV/UNIL, Lausanne, Switzerland.
23 Oxford University, Oxford, UK.
24 Department of Excellence in Robotics and AI, Biorobotics Institute, Scuola Superiore Sant’Anna, Pisa, Italy.
25 These authors contributed equally: Tomislav Milekovic, Eduardo Martin Moraud, Nicolo Macellari, Charlotte Moerman, Flavio Raschella, Shiqi Sun, Matthew G. Perich.
26 These authors jointly supervised this work: Jocelyne Bloch, Erwan Bezard, G. Courtine.