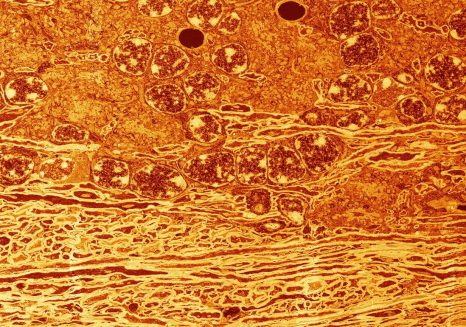
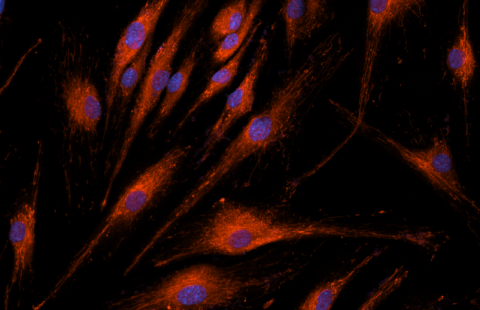
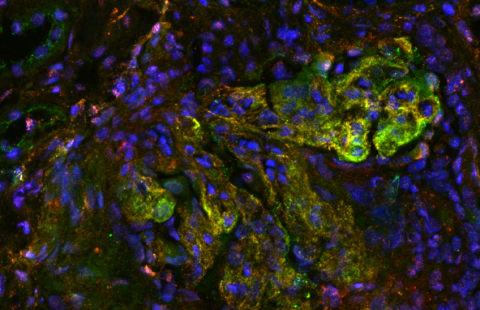
Image de coupe sagittale de cervelet de souris acquise en microscopie électronique montrant la substance blanche avec ses axones myélinisés et la substance grise avec la couche des grains. Claire-Marie Vacher (Columbia University Medical Center)/Cheryl Clarkson-Paredes and Anastas Popratiloff (The George Washington Nanofabrication & Imaging Center).
Plusieurs études ont montré que la prématurité augmentait le risque d’apparition de désordres neurodéveloppementaux tels que les troubles du spectre autistique (TSA). Plus la naissance est prématurée, plus le risque d’apparition de déficits moteurs ou cognitifs est élevé. Comment expliquer cela ? Des chercheurs de l’Université de Columbia à New York et du Children’s National Hospital de Washington, D.C., en collaboration avec l’Inserm et l’Université Paris-Saclay, se sont penchés sur cette question et ont fait l’hypothèse que la perte prématurée du placenta pourrait jouer un rôle dans les déficits observés. Grâce au développement d’un nouveau modèle préclinique chez la souris, ils ont montré que la diminution significative d’une hormone placentaire, dont le cerveau en développement devrait normalement bénéficier dans la seconde moitié de la gestation, pourrait favoriser le risque d’apparition de troubles comportementaux qui pourraient s’apparenter aux troubles du spectre de l’autisme. Ces effets sont principalement observés chez les mâles. L’étude fait l’objet d’une publication dans la revue Nature Neuroscience.
Le placenta est un organe qui permet l’alimentation du fœtus en oxygène et nutriments et élimine les déchets. Il produit également des hormones, notamment des taux élevés d’alloprégnanolone ou ALLO (une hormone dérivée de la progestérone) à la fin de la grossesse. Environ un nouveau-né sur 10 naît prématurément et de fait est privé de taux normaux de cette hormone.
Des chercheurs américains à l’Université de Colombia, en collaboration avec les équipes françaises de l’Inserm au sein de l’unité Maladies et Hormones du Système Nerveux (U 1195 Inserm) se sont intéressés au rôle du placenta dans le développement cérébral pour tenter notamment d’expliquer le lien entre prématurité et risque élevé d’apparition de déficits moteurs ou cognitifs. Dans le cadre de cette étude, les chercheurs ont créé un modèle de souris dans lequel ils ont été en mesure de réduire de manière sélective la production placentaire d’ALLO au cours de la gestation, afin que les souriceaux soient exposés à des taux placentaires d’ALLO insuffisants.
L’équipe de chercheurs a ainsi découvert que la diminution de la concentration de cette hormone dans le placenta altérait le développement du cerveau sur le long terme, entraînant l’apparition de comportements de type autistique chez les descendants mâles.
En effet, bien que les fœtus mâles et femelles aient été, les uns comme les autres, soumis à une insuffisance d’ALLO, seuls les souriceaux mâles ont présenté des comportements de type autistique après la naissance, notamment des difficultés d’interaction avec les autres animaux et des stéréotypes moteurs. Les chercheurs ont ensuite analysé leur développement cérébral et suivi les conséquences de cette insuffisance sur leur comportement jusqu’à l’âge adulte.
Les souris mâles ayant reçu des taux placentaires d’ALLO insuffisants présentaient des modifications structurelles du cervelet, une région du cerveau impliquée dans la coordination des mouvements et qui a également été liée à l’autisme.
« En particulier, nous avons observé un épaississement de la gaine de myéline, le revêtement qui protège les fibres nerveuses et accélère la propagation de l’influx nerveux », a indiqué Claire-Marie Vacher, PhD, professeure associée en néonatalogie dans le département de Pédiatrie du Vagelos College of Physicians and Surgeons de l’Université de Columbia et première auteure de l’article. « On sait que des changements comparables ont été observés de manière transitoire dans le cervelet de certains enfants de sexe masculin souffrant d’autisme. »
« Chez l’animal, l’établissement d’un lien entre une modification de la fonction placentaire au cours de la gestation et des effets persistants sur le développement ultérieur du cerveau est un résultat particulièrement frappant », indique Anna Penn, MD, PhD, cheffe du service de néonatologie à l’Université de Colombia et dernière auteure de l’étude.
Des similarités avec les tissus humains
Afin de déterminer si des modifications similaires peuvent survenir chez les nourrissons, les chercheurs ont également procédé à des examens post-mortem de tissus cérébelleux de prématurés et de nourrissons arrivés à terme, décédés peu de temps après la naissance. Leur analyse a permis de mettre en évidence des modifications similaires au niveau de la gaine de myeline spécifiquement pour les nourrissons masculins lorsque le cervelet de prématurés était comparé au cervelet de nourrissons nés à terme. Cette étude est une première étape importante pour comprendre comment les hormones placentaires peuvent contribuer au développement cérébral et comportemental chez l’homme.
L’injection de l’ALLO réduit les symptômes autistiques
L’étude a également permis de mettre en évidence que les changements affectant la structure du cervelet et les comportements chez les souris pouvaient être évités par l’injection d’ALLO à la fin de la gestation.
Les chercheurs ont constaté qu’une injection d’ALLO chez la mère au cours de la gestation pouvait prevenir les comportements de type autistique dans leur modèle préclinique. Des résultats similaires ont été observés après une injection de muscimol, un composé qui active les récepteurs GABA-A — les mêmes récepteurs qui réagissent à l’ALLO. Avec ces traitements, les chercheurs ont également constaté une normalisation des niveaux de protéines de la myéline dans le cervelet.
« Notre étude offre de nouvelles perspectives intéressantes sur l’implication de la perte d’hormones placentaires—qui se produit en cas de naissance prématurée ou si le placenta ne fonctionne pas correctement au cours de la grossesse—sur le risque de désordres neurodéveloppementaux et comportementaux chez l’enfant», indique l’auteure principale, Claire-Marie Vacher.
« On pourrait désormais également envisager des études rétrospectives en réalisant un suivi longitudinal pour corréler des défauts endocriniens pendant la grossesse avec des troubles cognitifs et/ou comportementaux des enfants. Cela permettrait d’identifier le stade de la grossesse où l’insuffisance hormonale intervient afin d’envisager une éventuelle intervention thérapeutique », ajoute Philippe Liere, PhD, ingénieur de recherche et responsable du plateau technique analytique de spectrométrie de masse de l’U1195.
Ces contenus pourraient aussi vous intéresser :