Une nouvelle voie de défense contre des bactéries comme l’agent de la tuberculose et le staphylocoque doré a été identifiée chez l’Homme grâce à l’étude d’un petit ver plat aquatique, le planaire. Cette découverte a été réalisée par des chercheurs de l’Unité de recherche sur les maladies infectieuses et tropicales émergentes (CNRS/IRD/Inserm/Aix-Marseille Université), en collaboration avec le Centre méditerranéen de médecine moléculaire (Inserm/Université Nice Sophia Antipolis), et d’autres laboratoires français et étrangers (1). Leurs travaux, publiés dans la revue Cell Host and Microbe le 10 septembre 2014, soulignent l’importance d’étudier des organismes modèles alternatifs, et ouvrent la voie vers de nouveaux traitements contre les infections bactériennes.
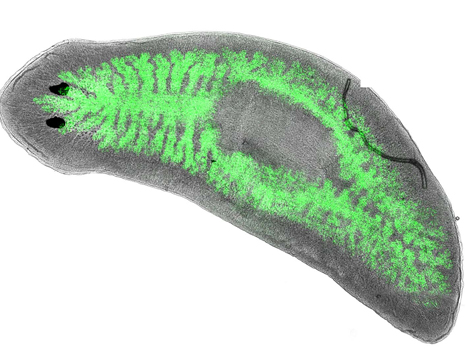
© Eric Ghigo Le planaire Dugesia japonica infecté par des bactéries Legionella pneumophila rendues fluorescentes (en vert, dans les intestins de l’animal).
En étudiant un organisme modèle original, un ver plat aquatique appelé planaire, des chercheurs ont réussi à identifier une nouvelle voie de défense contre des bactéries comme l’agent de la tuberculose (Mycobacterium tuberculosis). Présent à l’état latent chez l’Homme, ce mécanisme pourrait être stimulé de manière pharmacologique.
Les chercheurs de l’équipe Infection, Genre et Grossesse (I2G) dirigée par Eric Ghigo ont eu l’idée de travailler sur la planaire Dugesia japonica en constatant un certain essoufflement des découvertes faites sur les modèles classiques en immunologie (la mouche Drosophila melanogaster, le ver rond Caenorhabditis elegans). Précédemment, ce ver plat était surtout connu pour ses extraordinaires capacités de régénération (2), qui en font un être potentiellement immortel (il ne peut pas mourir de vieillesse). Il est aussi capable de résister à des bactéries très pathogènes voire mortelles pour l’Homme, comme l’a découvert l’équipe de chercheurs, la seule au monde à s’être lancée dans des études d’immunologie sur cet organisme.
Pour comprendre les raisons d’une défense immunitaire si efficace, les chercheurs ont étudié les gènes exprimés par la planaire suite à l’infection par des bactéries pathogènes pour l’Hommetelles que M. tuberculosis, le staphylocoque doré (Staphylococcus aureus) et l’agent de la légionellose (Legionella pneumophila). Ils ont ainsi identifié 18 gènes qui lui confèrent une résistance à ces agents pathogènes
Les scientifiques se sont penchés sur l’un de ces gènes – MORN2 – essentiel à l’élimination de tous les types de bactéries testées, et présent dans le génome humain. Ils ont surexprimé ce gène dans des macrophages humains, des globules blancs chargés d’éliminer les agents pathogènes en les digérant (un processus appelé phagocytose). Ainsi stimulés, les macrophages sont devenus capables d’éliminer les bactéries S. aureus, L. pneumophila et M. tuberculosis et bien d’autre agent pathogènes.
L’étude détaillée du mécanisme d’action de MORN2 a montré qu’il favorise la séquestration (3) de M. tuberculosis dans une cavité intracellulaire (le phagolysosome) où la bactérie est détruite. Or, l’agent de la tuberculose réussit habituellement à échapper à ce destin : la bactérie peut alors rester à l’état latent dans les cellules, et ressurgir lorsque le système immunitaire est affaibli. Cette découverte ouvre donc une nouvelle piste d’action contre M. tuberculosis, dont les souches résistantes aux antibiotiques sont de plus en plus répandues.
Ces travaux montrent aussi l’intérêt des organismes modèles « exotiques », comme la planaire. En effet, le gène MORN2 a été perdu au cours de l’évolution menant aux organismes modèles classiques tels que la mouche D. melanogaster, alors qu’il est conservé chez l’Homme. Le mécanisme de la réponse immunitaire humaine découvert dans cette étude serait donc resté inconnu sans le recours à ce nouveau modèle.
Ces recherches ont notamment bénéficié d’un soutien du CNRS au travers d’un PEPS (Projet Exploratoire Premier Soutien), financement destiné à soutenir des projets de recherche exploratoires, faisant appel à la créativité des équipes
(1) en France, le Centre commun de microscopie appliquée (Université Nice Sophia Antipolis) ; en Italie, le Département de clinique et médecine expérimentale, à Pise ; en Nouvelle-Zélande, le Département de Génomique et Bioinformatique, à Otago
(2) En 1814, JG Dalyell a découvert qu’un planaire coupé en 279 fragments se régénère, en 15 jours, pour donner 279 vers.
(3) via un mécanisme appelé « LC3-associated phagocytosis »
Ces contenus pourraient aussi vous intéresser :
Screening in planarians identifies MORN2 as a key component in LC3-associated phagocytosis and resistance to bacterial infection,
P. Abnave, G. Mottola, G. Gimenez, N. Boucherit, V. Trouplin, C. Torre, F. Conti, A. Ben Amara, C. Lepolard, B. Djian, D. Hamaoui, A. Mettouchi, A. Kumar, S. Pagnotta, S. Bonatti, H. Lepidi, A. Salvetti, L. Abi-Rached, E. Lemichez, J.-L. Mege, E. Ghigo,
Cell Host and Microbe, 10 septembre 2014.