Contact Chercheur
Christophe BernardDirecteur de recherche
Unité mixte Inserm 1106 « Institut de neurosciences des systèmes » (Marseille)
+ 33 (0) 4 91 29 98 06 / 06 18 04 49 13
rf.uma-vinu@dranreb.ehpotsirhc
De nombreux médicaments potentiellement efficaces sont créés pour traiter les désordres neurologiques, mais ne peuvent pas toujours être utilisés dans la pratique. Typiquement, pour une maladie telle que l’épilepsie, agir sur le cerveau exactement au bon moment et au bon endroit est essentiel. C’est pourquoi l’équipe de chercheurs dirigée par Christophe Bernard au sein de l’Unité Inserm 1106 « Institut de neurosciences des systèmes », avec l’aide de scientifiques de l’Ecole des Mines de St. Etienne et de l’Université de Linköping (Suède), a développé une micropompe électronique et organique qui, associée à un anti-épileptique, inhibe de manière localisée, la crise épileptique au niveau du cerveau in vitro. Ces travaux sont publiés dans la revue Advanced Materials.
Actuellement, les médicaments sont l’approche la plus utilisée pour traiter les maladies du cerveau. Pourtant, il arrive que des produits prometteurs échouent aux tests au niveau clinique pour plusieurs raisons :
– Ils sont dilués dans des solutions potentiellement toxiques,
– Ils peuvent eux-mêmes être toxiques lorsqu’ils atteignent des organes vers lesquels ils ne sont pas initialement dirigés,
– La barrière hémato-encéphalique, qui sépare le cerveau de la circulation sanguine, empêche la majorité des molécules d’atteindre leurs cibles cérébrales,
– Les médicaments qui réussissent à pénétrer dans le cerveau vont agir de manière non spécifique et donc sur des régions cérébrales saines.
L’épilepsie est un exemple typique pour lequel de nombreux médicaments n’ont pu être commercialisés à cause de leur nocivité, alors qu’ils étaient potentiellement efficaces pour traiter les patients résistants aux traitements classiques [1] .
Lors d’une crise d’épilepsie, les cellules nerveuses d’une zone précise du cerveau s’activent soudainement de manière excessive. Comment alors contrôler ce phénomène sans intervenir sur les régions cérébrales saines ? Pour répondre à cette question, l’équipe de Christophe Bernard, en collaboration avec l’équipe de George Malliaras au Campus Georges Charpak-Provence de l’Ecole des Mines de Saint-Étienne et des scientifiques suédois, ont développé une micropompe biocompatible permettant de délivrer les substances thérapeutiques directement dans les zones du cerveau concernées.
La micropompe (20 fois plus fine qu’un cheveu) est constituée d’une membrane dite « à échange de cations », c’est-à-dire que des ions négatifs sont fixés à sa surface. Ainsi, elle attire les petites molécules chargées positivement, que ce soient des ions ou des médicaments. Lorsqu’un courant électrique lui est appliqué, le flux d’électrons généré projette les molécules d’intérêt vers la zone visée.
Pour pouvoir valider cette nouvelle technique, les chercheurs ont reproduit l’hyperexcitabilité des neurones épileptiques dans le cerveau de souris in vitro. Puis, ils ont injecté le GABA, une molécule naturellement produite dans le cerveau qui inhibe les neurones, au niveau de cette région hyperactive grâce à la micropompe. Les scientifiques observent alors que la molécule a non seulement mis fin à l’activité anormale de la région ciblée mais surtout, n’interfère pas avec les fonctions des neurones avoisinants.
Cette technologie résoudrait donc les obstacles rencontrés classiquement par les thérapies en permettant une action très localisée, directement dans le cerveau et sans toxicité périphérique.
« En équipant des électrodes, comme celles utilisées pour traiter la maladie de Parkinson, avec cette micropompe, il serait envisageable de se servir de cette technologie pour soigner des patients épileptiques résistants aux traitements classiques, ainsi que ceux pour lesquels les effets secondaires sont trop importants » explique Christophe Bernard, directeur de recherche Inserm.
Sur la base de ces premiers résultats, les chercheurs travaillent désormais sur un passage au modèle animal in vivo et sur la possibilité d’allier ce système de haute technologie à la mini puce qu’ils ont déjà développée en 2013. Le dispositif pourrait être embarqué et autonome. La puce servirait à détecter l’arrivée imminente de la crise, afin de déclencher l’activation de la pompe pour l’injection du médicament au moment le plus propice. Il serait donc possible de contrôler l’activité du cerveau où et quand c’est nécessaire.
Au-delà de l’épilepsie, cette technologie de pointe combinée avec des médicaments déjà existants, offre de nouvelles perspectives pour de nombreuses pathologies du cerveau qui restent difficilement traitables aujourd’hui.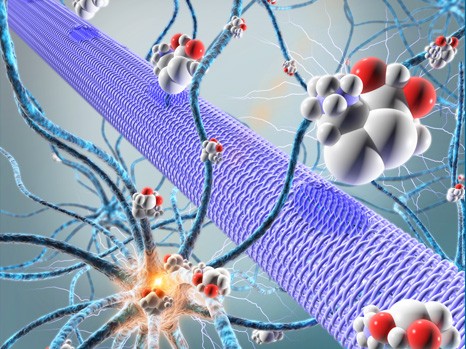
La micropompe électronique organique (représentée par un cylindre violet) permet de libérer directement au milieu des neurones des molécules actives (sphères) qui vont permettre de contrôler l’activité de ces neurones (ici elles vont stopper une activité épileptique).
© Adam Williamson, Christophe Bernard, ID Labs, Arab4D (Christophe Bernard: Controlling Epileptiform Activity with Organic Electronic Ion Pumps. DOI: 10.1002/adma.201500482. 2015. Copyright Wiley-VCH Verlag GmbH & Co. KGaA. Reproduced with permission)
Cette pathologie, qui touche près de 50 millions de personnes dans le monde, est le désordre neurologique le plus fréquent après la migraine.
Les dysfonctionnements neuronaux des épileptiques entraînent des crises aux symptômes variés : de la perte de conscience aux troubles du mouvement, des sensations ou de l’humeur.
Malgré les progrès de la médecine, 30 % des personnes touchées sont résistantes à tout traitement.