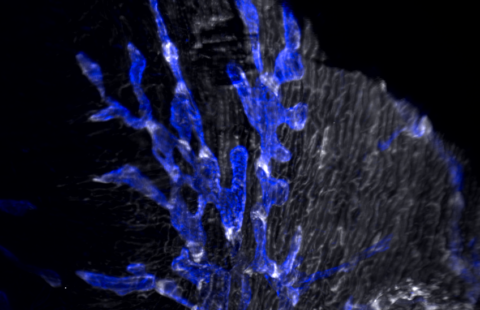
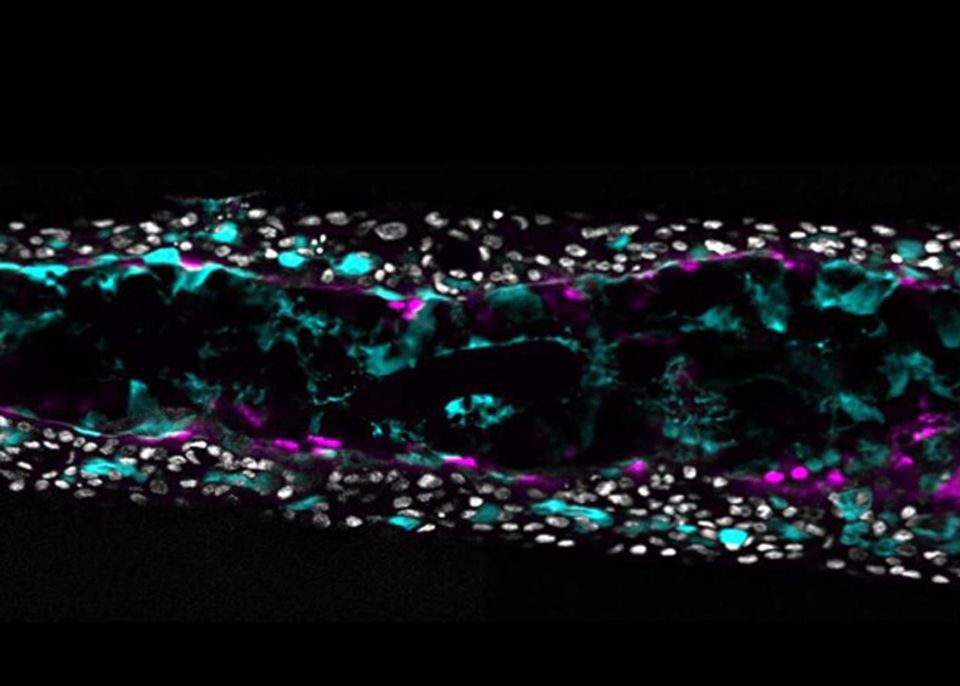
Nuclear Factor Erythroid 2-Related Factor 2 Drives Podocyte-Specific Expression of Peroxisome Proliferator-Activated Receptor γ Essential for Resistance to Crescentic GN.
1Paris Cardiovascular Centre (PARCC), Institut National de la Santé et de la Recherche Médicale (INSERM), Paris, France; Université Paris Descartes, Sorbonne Paris Cité, Paris, France; rf.mresni@xuaraht.siuol-erreip rf.mresni@euqineh.elorac.2Paris Cardiovascular Centre (PARCC), Institut National de la Santé et de la Recherche Médicale (INSERM), Paris, France; Université Paris Descartes, Sorbonne Paris Cité, Paris, France; Centre de Recherche, Centre Hospitalier de l'Université de Montréal, Montréal, Québec, Canada;3Paris Cardiovascular Centre (PARCC), Institut National de la Santé et de la Recherche Médicale (INSERM), Paris, France; Université Paris Descartes, Sorbonne Paris Cité, Paris, France;4Paris Cardiovascular Centre (PARCC), Institut National de la Santé et de la Recherche Médicale (INSERM), Paris, France; British Heart Foundation Centre of Research Excellence (BHF CoRE), Edinburgh, United Kingdom;5Paris Cardiovascular Centre (PARCC), Institut National de la Santé et de la Recherche Médicale (INSERM), Paris, France;6Department of Medical Biochemistry, Tohoku University Graduate School of Medicine, Sendai, Japan;7Paris Cardiovascular Centre (PARCC), Institut National de la Santé et de la Recherche Médicale (INSERM), Paris, France; Université Paris Descartes, Sorbonne Paris Cité, Paris, France; Department of Nephrology and.8Paris Cardiovascular Centre (PARCC), Institut National de la Santé et de la Recherche Médicale (INSERM), Paris, France; Université Paris Descartes, Sorbonne Paris Cité, Paris, France; Department of Pathology, Hôpital Européen Georges Pompidou, Assistance Publique-Hôpitaux de Paris (AP-HP), Paris, France; and.9Unité Mixte de Recherche (UMR) 702, Institut National de la Santé et de la Recherche Médicale (INSERM), Paris, France.10Paris Cardiovascular Centre (PARCC), Institut National de la Santé et de la Recherche Médicale (INSERM), Paris, France; Université Paris Descartes, Sorbonne Paris Cité, Paris, France; Department of Nephrology
Journal of American Society of nephrology, 21 May 2015