Contact Chercheur
Toby Lawrence
Chercheur Inserm
Unité 1104 Centre d’immunologie de Marseille – Luminy
+33(0)4.91.26.91.66
Contact Presse
rf.mresni@esserp
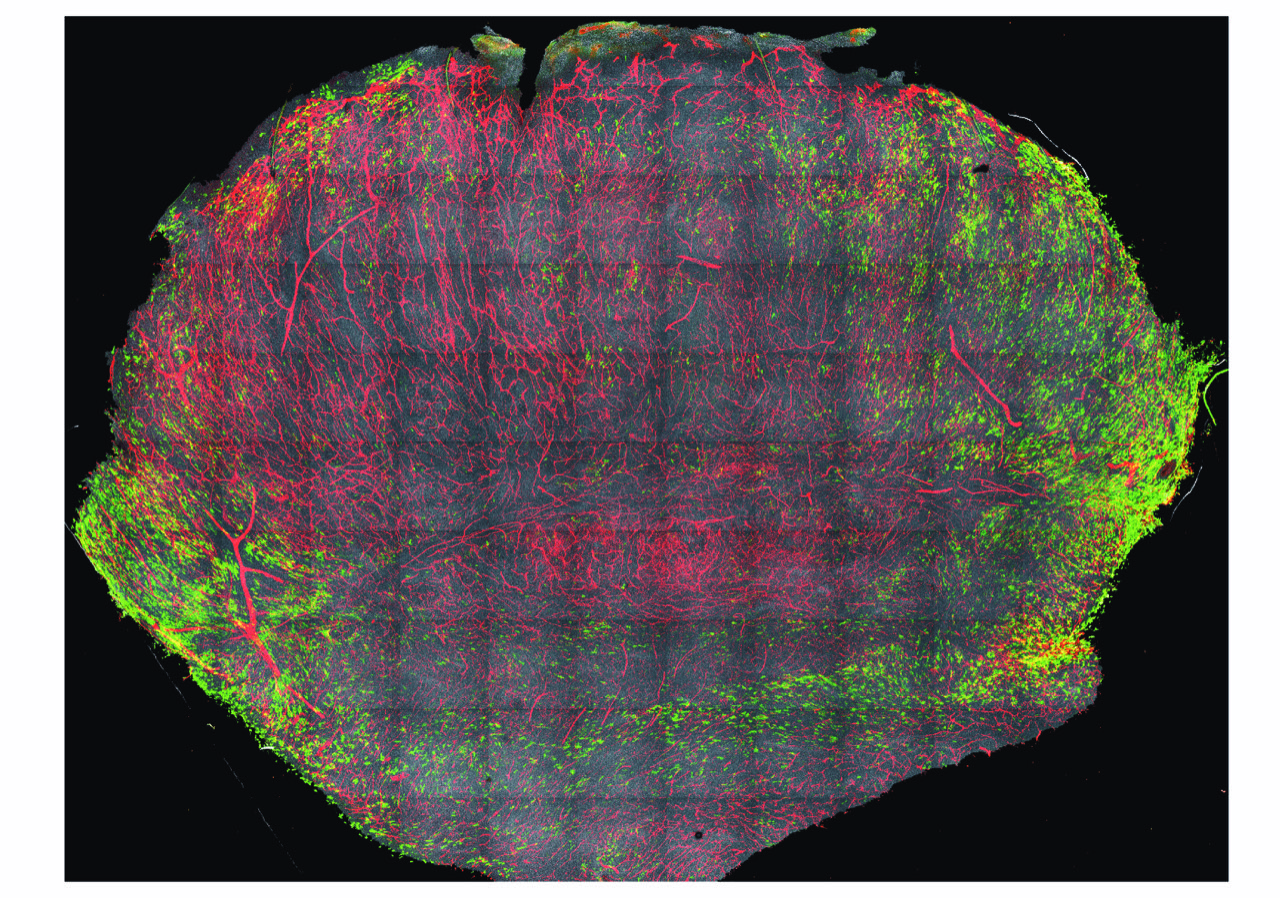
Coupe transversale d’un mélanome avec les MTA CD163 (macrophages associés aux tumeurs) colorés en vert, les vaisseaux sanguins colorés en rouge et le noyau des cellules coloré en gris. © 2019 Etzerodt et al.
Une équipe internationale de chercheurs dirigée par Toby Lawrence, chercheur Inserm au sein de l’unité 1104 Centre d’immunology de Marseille – Luminy (Inserm / CNRS / Aix-Marseille Université), vient de mettre au point une thérapie potentielle pour réduire la taille des tumeurs, là où les médicaments précédents ont échoué. Ces résultats sont publiés dans le Journal of Experimental Medicine.
Les tumeurs se développent à partir de cellules anormales dans le corps qui continuent de croître en formant des « grumeaux ». Ces derniers peuvent être bénins, mais ils peuvent aussi devenir malins et mener au cancer.
Les tumeurs malignes, infiltrées par des cellules immunitaires appelées macrophages aident habituellement les défenses immunitaires de l’organisme. Mais les macrophages associés aux tumeurs (MTA) sont manipulés par les cellules cancéreuses pour contribuer non seulement à la croissance et à la propagation des tumeurs dans l’organisme, mais aussi à la répression des défenses immunitaires naturelles contre ces tumeurs.
C’est pour contrer cette double action des MTA sur la croissance et le développement des cancers qu’une équipe internationale, regroupant des chercheurs de l’Inserm et du King’s College de Londres, a conçu une thérapie qui cible les MTA sans supprimer d’autres macrophages. Dans une étude publiée dans le Journal of Experimental Medicine, les chercheurs expliquent comment ils sont parvenus à cibler les « mauvais » MTA sans supprimer les défenses naturelles de l’organisme.
En effet, parmi les développements récents dans le domaine du traitement du cancer, il existe des médicaments appelés « inhibiteurs des points de contrôle immunitaires » (ICI). Ces derniers ont révolutionné le traitement du cancer, en particulier chez les patients atteints de mélanomes. Cependant, les patients qui répondent au traitement ICI ont des effets secondaires graves et plus de 70 % des patients ne répondent pas du tout.
Dans cette étude, les auteurs ont utilisé des modèles murins de mélanomes résistants au traitement ICI.
Selon Toby Lawrence, chercheur Inserm qui a dirigé l’étude, cette découverte pourrait mener à l’élaboration d’un médicament qui permettrait de tuer spécifiquement les MTA.
« Nous avons été stupéfaits de voir à quel point le ciblage d’un sous-ensemble spécifique de MTA était efficace pour réduire la croissance tumorale dans ce modèle où le traitement ICI n’avait aucun impact, indique Toby Lawrence. Cette étude fournit non seulement une nouvelle stratégie pour cibler des sous-ensembles spécifiques de MTA en clinique, mais montre aussi pourquoi il est important de cibler ces sous-ensembles, et non les autres macrophages qui aident les réponses immunitaires anti-tumeurs, conclut-il ».
Toby Lawrence
Chercheur Inserm
Unité 1104 Centre d’immunologie de Marseille – Luminy
+33(0)4.91.26.91.66
rf.mresni@esserp
Specific targeting of CD163+ TAMs mobilizes inflammatory monocytes and promotes T cell–mediated tumor regression
Anders Etzerodt1,2, Kyriaki Tsalkitzi1, Maciej Maniecki3,4, William Damsky4, Marcello Delfini1, Elodie Baudoin1, Morgane Moulin1,5, Marcus Bosenberg4, Jonas Heilskov Graversen6, Nathalie Auphan-Anezin1, Søren Kragh Moestrup2,6, and Toby Lawrence1,5,7
1 Aix Marseille University, CNRS, INSERM, CIML, Marseille, France;
2 Department of Biomedicine, University of Aarhus, Aarhus, Denmark;
3 Department of Clinical Biochemistry, Aarhus University Hospital, Aarhus, Denmark;
4 Department of Dermatology, Yale University School of Medicine, New Haven, CT;
5 Centre for Inflammation Biology and Cancer Immunology, School of Immunology and Microbial Sciences, King’s College London, London, UK;
6 Institute of Molecular Medicine, University of Southern Denmark, Odense, Denmark;
7 Henan Key Laboratory of Immunology and Targeted Therapy, School of Laboratory Medicine, Xinxiang Medical University, Xinxiang,China.
Journal of Experimental Medicine : https://doi.org/10.1084/jem.20182124