C’est un bond en avant qui se prépare dans la pratique chirurgicale et médecine régénératrice. Une équipe dirigée par Ludwik Leibler du laboratoire « Matière molle et chimie » (CNRS/ESPCI ParisTech) et Didier Letourneur du Laboratoire de recherche vasculaire translationnelle (Inserm/Universités Paris Diderot et Paris 13), vient de démontrer que le principe d’adhésion par des solutions aqueuses de nanoparticules peut être utilisé in vivo pour réparer des organes « mous » et des tissus. Cette méthode de collage, extrêmement simple d’utilisation, a été testée sur les rats. Appliquée à la peau, elle permet de fermer des blessures profondes en quelques secondes et d’obtenir une cicatrisation de qualité et esthétique. Elle a également été éprouvée avec succès pour réparer des organes difficiles à suturer tels le foie. Enfin, sur le cœur battant, cette solution a permis de fixer un dispositif médical démontrant ainsi le potentiel de la méthode pour délivrer des médicaments ou renforcer les tissus. Ces travaux viennent d’être publiés sur le site de la revue Angewandte Chemie.
En décembre 2013, dans la revue Nature, une équipe dirigée par Ludwik Leibler[1] a présenté un concept entièrement nouveau de collage des gels et des tissus biologiques grâce à des nanoparticules[2]. Le principe est simple : des nanoparticules contenues dans une solution étalée sur des surfaces à coller se lient au réseau moléculaire du gel (ou du tissu), phénomène appelé adsorption, et, dans le même temps, le gel (ou le tissu) lie les particules entre elles. Ainsi, se forment d’innombrables connexions entre les deux surfaces. Le processus d’adhésion, qui ne comporte aucune réaction chimique, ne prend que quelques secondes. Dans leur dernière étude qui vient d’être publiée, les chercheurs, à l’aide d’expériences réalisées sur les rats, montrent que cette méthode appliquée in vivo a le potentiel de bouleverser la pratique clinique.
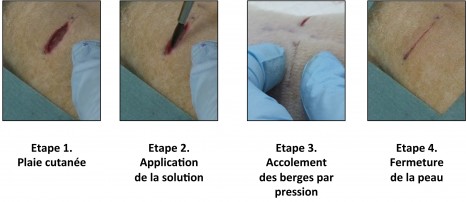
Dans une première expérience, les chercheurs ont procédé à une analyse comparée de la fermeture d’une plaie profonde de la peau par la méthode traditionnelle des points de suture et par l’application au pinceau de la solution aqueuse de nanoparticules. Cette seconde méthode simple d’utilisation permet de refermer la peau rapidement jusqu’à cicatrisation complète, sans inflammation ni nécrose. La cicatrice résultante est presque invisible.
Illustration de la première expérience réalisée par les chercheurs sur des rats : réparation d’une plaie profonde par application de la solution aqueuse de nanoparticules. La fermeture de la plaie s’effectue en trente secondes. © laboratoire « Matière molle et chimie » (CNRS/ESPCI ParisTech) Des vidéos sont disponibles sur demande auprès du bureau de presse du CNRS
Dans une seconde expérience, toujours chez des rats, les chercheurs ont appliqué cette solution à des organes « mous » qui tels le foie, le poumon ou la rate sont difficiles à suturer car ils se déchirent lors du passage de l’aiguille. Actuellement aucune colle n’allie efficacité d’adhésion et innocuité pour l’organisme. Confrontés à une entaille profonde du foie avec forte hémorragie, les chercheurs ont refermé la blessure en étalant la solution aqueuse de nanoparticules et en pressant les deux bords de la blessure. La perte de sang s’est alors arrêtée. Pour réparer un lobe de foie sectionné, les chercheurs ont également utilisé des nanoparticules : ils ont collé un pansement recouvert de nanoparticules sur la plaie, arrêtant ainsi l’hémorragie. Dans les deux situations, le fonctionnement de l’organe est préservé et les animaux survivent.
« Coller un pansement pour arrêter les fuites » n’est qu’un exemple des possibilités ouvertes par l’adhésion apportés par des nanoparticules. Dans un tout autre domaine, les chercheurs sont parvenus grâce aux nanoparticules à fixer une membrane dégradable utilisée pour la thérapie cellulaire sur le cœur et ce, malgré les fortes contraintes mécaniques liées à ses battements. Ainsi ils démontrent qu’il serait possible de fixer des dispositifs médicaux variés à des fins thérapeutiques ou de réparation et de renforcement mécaniques des organes et des tissus.
Cette méthode d’adhésion est exceptionnelle de par son potentiel champ d’applications cliniques. Elle est simple, facile à mettre en œuvre et les nanoparticules utilisées (silice, oxydes de fer) peuvent être métabolisées par l’organisme. Elle peut facilement être intégrée dans les recherches actuelles sur la cicatrisation et la régénération des tissus et contribuer au développement de la médecine régénératrice.
[1] Ludwik Leibler est lauréat de la médaille de l’innovation 2013.
[2] Voir le communiqué de presse sur ces travaux : https://www2.cnrs.fr/presse/communique/3355.htm
Ces contenus pourraient aussi vous intéresser :
Anne Meddahi-Pellé, Aurélie Legrand, Alba Marcellan, Liliane Louedec, Didier Letourneur, Ludwik Leibler.
Angewandte Chemie. Parution en ligne le 16 avril 2014.
DOI: 10.1002/anie.201401043