Contact scientifique
Serge Picaud et José-Alain Sahel
U968 Institut de la Vision
Téléphones sur demande
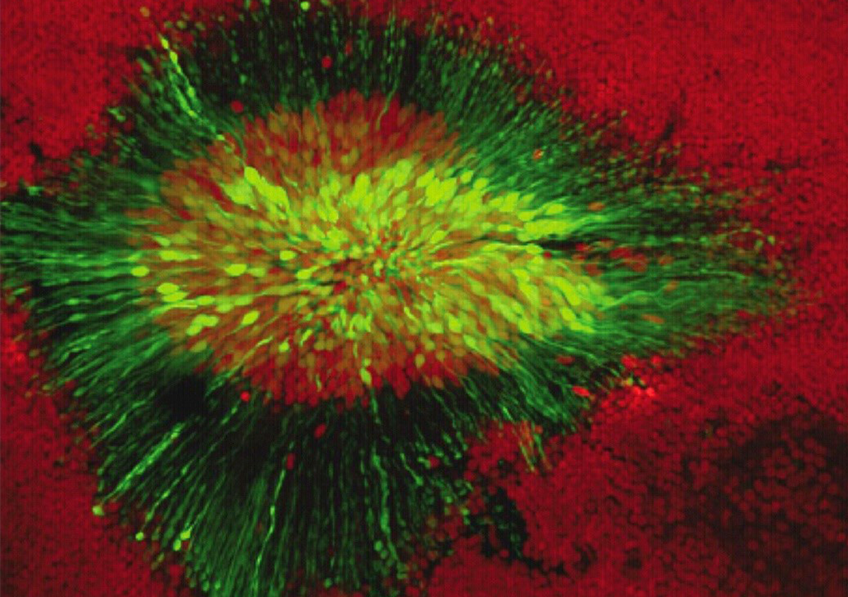
Cette photo est issue de travaux de recherche sur la thérapie génique dans le traitement de la cécité. Rétine de primate non humain après le transfert d’un gène de protéine fluorescente par un virus adéno-associé (AAV). On distingue les cellules photoréceptrices à cônes (en vert) ayant intégré le gène. © Inserm/Dubus, Elisabeth.
Les personnes atteintes de neuropathie optique héréditaire de Leber perdent la vue dès l’adolescence avec un déclin soudain au niveau des deux yeux, jusqu’à la cécité. Alors que les options de traitements étaient jusqu’ici très limitées, des chercheurs de l’Inserm, de Sorbonne Université et du CNRS à l’Institut de la Vision à Paris ont conçu une approche de thérapie génique pour ces patients. Les résultats d’un essai clinique mené sur 37 patients et publiés dans la revue Science Translational Medicine, montrent que ce traitement améliore de façon significative la vision de ces patients. GenSight Biologics (EURONEXT: SIGHT), une start-up issue de l’Institut de la vision, a mis au point et réalisé le développement clinique de ce traitement. Celui-ci a ensuite été évalué dans un essai clinique international multicentrique produit par un consortium en Europe et aux Etats-Unis, comprenant les équipes de Patrick Yu-Wai-Man de l’UCL Institute of Ophthalmology et de José-Alain Sahel (professeur à Sorbonne Université et directeur de l’Institut de la Vision) à la Fondation Ophtalmologique Rothschild et du CHNO des Quinze-Vingts.
La neuropathie optique héréditaire de Leber (NOHL), est une maladie héréditaire qui se manifeste par une baisse brutale et bilatérale de la vision pouvant conduire à la cécité. Elle est causée par des mutations de l’ADN mitochondrial[1] qui affectent la production de la protéine ND4. Cette perte visuelle intervient généralement chez l’homme jeune sur un œil puis quelques mois plus tard sur le deuxième œil. La pathologie touche une personne sur 30 000 à 50 000.
Dans l’espoir d’aider ces patients, l’équipe de Marisol Corral-Debrinski avec José-Alain Sahel et Serge Picaud à l’Institut de la Vision (Inserm/Sorbonne Université/CNRS) a mis au point un traitement qui repose sur une nouvelle approche de thérapie génique, permettant pour la première fois au monde de corriger un défaut d’un gène mitochondrial (le gène ND4)[2].
La thérapie génique est une stratégie thérapeutique qui consiste à introduire du matériel génétique dans des cellules pour soigner une maladie. Pour permettre au traitement de pénétrer correctement dans les cellules d’un patient, les scientifiques utilisent dans la plupart des cas un vecteur viral qui assure son transport jusqu’au noyau. Mais pour utiliser cette stratégie dans la neuropathie optique héréditaire de Leber, les chercheurs étaient confrontés à un obstacle majeur : comment cibler la mitochondrie alors que le vecteur viral introduit l’ADN porteur du gène correct dans le noyau ?
Dans l’essai clinique baptisé REVERSE qui a été réalisé par un consortium international en Europe et aux États-Unis et portait sur 37 patients, les chercheurs ont démontré l’efficacité de cette approche par la mesure d’une réelle amélioration clinique.
Cet effet bénéfique sur les deux yeux suite à une injection dans un seul œil était inattendu. Pour mieux comprendre le phénomène, GenSight Biologics et les auteurs de l’étude ont testé à nouveau la thérapie chez l’animal et ont montré que cet effet bilatéral s’explique par le transfert du gène sain d’un œil à l’autre.
« Cette découverte ouvre des perspectives nouvelles pour le traitement des patients atteints de neuropathie optique de Leber, alors qu’il n’en existait jusqu’à aujourd’hui aucun de réellement efficace. Nos résultats démontrent l’efficacité de cette thérapie génique innovante dans l’œil, ce qui offre une véritable option thérapeutique contre la cécité pour les patients. Ils ouvrent par ailleurs des perspectives pour son application pour d’autres maladies mitochondriales dans d’autres tissus », soulignent les auteurs de l’étude.
Suite à ces travaux, une demande d’Autorisation de Mise sur le Marché (AMM) du vecteur de thérapie génique innovant, testé dans l’essai et appelé LUMEVOQ, a été déposée en septembre par GenSight Biologics auprès de l’Agence réglementaire européenne (EMA).
[1] Les mitochondries sont des organelles présentes dans les cellules, à l’extérieur du noyau. Elles sont essentielles à la production d’énergie. Elles possèdent leur propre matériel génétique, l’ADN mitochondrial, qui code pour un certain nombre de protéines, dont la protéine ND4, affectée dans la neuropathie optique de Leber.
[2] Le développement de cette thérapie a été réalisé par GenSight Biologics, en collaboration avec l’Institut de la vision, le CHNO des Quinze Vingts et la Fondation Ophtalmologique Rothschild. Des centres experts ont participé aux études cliniques, et plus largement un consortium international en Europe et aux Etats-Unis.
Serge Picaud et José-Alain Sahel
U968 Institut de la Vision
Téléphones sur demande
Bilateral visual improvement with unilateral gene therapy injection for Leber hereditary optic neuropathy
Patrick Yu-Wai-Man1,2,3,4*, Nancy J. Newman5, Valerio Carelli6,7, Mark L. Moster8,
Valerie Biousse5, Alfredo A. Sadun9, Thomas Klopstock10,11,12, Catherine Vignal-Clermont13,14, Robert C. Sergott8, Günther Rudolph15, Chiara La Morgia6,7, Rustum Karanjia9,16, Magali Taiel17, Laure Blouin17, Pierre Burguière17, Gerard Smits18, Caroline Chevalier17, Harvey Masonson18, Yordak Salermo18, Barrett Katz18, Serge Picaud19, David J. Calkins20, José-Alain Sahel14,19,21,22
1 Cambridge Centre for Brain Repair and MRC Mitochondrial Biology Unit, Department
of Clinical Neurosciences, University of Cambridge, Cambridge CB2 0PY, UK.
2 Cambridge Eye Unit, Addenbrooke’s Hospital, Cambridge University Hospitals,
Cambridge CB2 0QQ, UK.
3 Moorfields Eye Hospital, London EC1V 2PD, UK.
4 UCL Institute of Ophthalmology, University College London, London EC1V 9EL, UK.
5 Departments of Ophthalmology, Neurology and Neurological Surgery, Emory
University School of Medicine, Atlanta, GA 30322, USA.
6 IRCCS Istituto delle Scienze Neurologiche di Bologna, UOC Clinica Neurologica, 40139 Bologna, Italy.
7 Unit of Neurology, Department of Biomedical and Neuromotor Sciences (DIBINEM), University of Bologna, 40139 Bologna, Italy.
8 Departments of Neurology and Ophthalmology, Wills Eye Hospital and Thomas Jefferson University, Philadelphia, PA 19107, USA.
9 Doheny Eye Institute and UCLA School of Medicine, Los Angeles, CA 90086, USA.
10 Friedrich Baur Institute at the Department of Neurology, University Hospital, LMU Munich, 80336 Munich, Germany.
11 German Center for Neurodegenerative Diseases (DZNE), 80336 Munich, Germany.
12 Munich Cluster for Systems Neurology (SyNergy),80336 Munich, Germany.
13 Department of Neuro-Ophthalmology and Emergencies,
Rothschild Foundation Hospital, 75019 Paris, France.
14 Centre Hospitalier National d’Ophtalmologie des Quinze Vingts, FOReSIGHT, INSERM-DGOS CIC 1423, 75012 Paris, France.
15 Department of Ophthalmology, University Hospital, LMU Munich, 80336 Munich, Germany.
16 Ottawa Hospital Research Institute and University of Ottawa Eye Institute, Ottawa, Ontario K1H 8L6, Canada.
17 GenSight Biologics, 75012 Paris, France.
18 GenSight Biologics, New York, NY 10016, USA.
19 Sorbonne Université, INSERM, CNRS, Institut de la Vision, 75012 Paris, France.
20 The Vanderbilt Eye Institute, Vanderbilt University Medical Center, Nashville, TN 37232, USA.
21 Fondation Ophtalmologique A. de Rothschild, 25-29 Rue Manin, 75019 Paris,
France.
22 Department of Ophthalmology, The University of Pittsburgh School of Medicine, Pittsburgh, PA 15213, USA.
Science Translational Medicine, décembre 2020
DOI : https://stm.sciencemag.org/lookup/doi/10.1126/scitranslmed.aaz7423