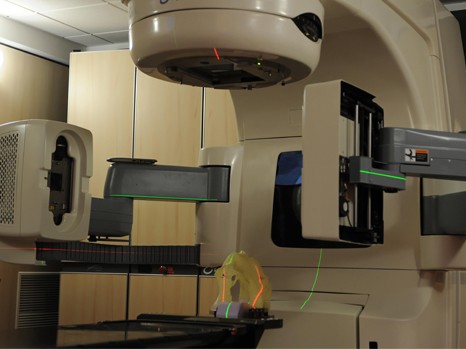
Deux études, l’une théorique, l’autre biologique et clinique, menées par Nicolas Foray, radiobiologiste au sein de l’Unité mixte de recherche 1052 « Centre de Recherche en Cancérologie de Lyon » (Inserm/CNRS/Centre Léon-Bérard/Université Lyon I), viennent d’être publiées dans les revues International Journal of Radiation Biology et International Journal of Radiation Oncology. Ces deux études permettent de mieux comprendre les effets secondaires indésirables de la radiothérapie. Elles proposent une nouvelle théorie de la réponse cellulaire aux radiations ionisantes. Cette théorie est basée sur la mise en évidence du passage d’une protéine appelée ATM du cytoplasme au noyau des cellules irradiées. Une fois dans le noyau, la protéine ATM déclenche la réparation des cassures de l’ADN : plus le retard de ce transit est grand, plus la radiosensibilité des cellules est élevée et plus les effets secondaires indésirables de la radiothérapie sont marqués.
(c) Inserm/Institut Curie/ Guénet, François
Ces deux études ont été possibles grâce à la collection COPERNIC (initiée depuis 2003) de plus d’une centaine de lignées cellulaires issues de patients radiosensibles.
- L’étude théorique résout une énigme de la radiobiologie vieille de 50 ans en donnant une interprétation biologique à une formule empirique. Cette formule relie la survie des cellules à la dose de radiation.
- L’étude biologique et clinique valide l’étude théorique. Elle rassemble 67 co-auteurs, dont 50 radiothérapeutes français, représentant une trentaine de centres anti-cancer ou de centres hospitaliers. Elle permet de développer aujourd’hui des tests prédictifs de radiosensibilité des réactions secondaires indésirables de la radiothérapie.
Quelle est l’innovation apportée par ces deux études ?
La protéine ATM a été découverte en 1995. Cette protéine est connue car ses mutations causent le syndrome associé à la plus forte radiosensibilité humaine, l’ataxie télangiectasie. Jusqu’à présent, la protéine ATM a toujours été considérée comme une protéine du noyau cellulaire et aucune étude n’avait sondé sa présence dans le cytoplasme. Le groupe de radiobiologie de l’Unité Inserm 1052 a analysé plus d’une centaine de lignées cellulaires issues de patients souffrant de réactions tissulaires indésirables après radiothérapie (dermites, rectites, etc …). Ces analyses ont montré que la protéine ATM est plutôt située dans le cytoplasme des cellules et transite dans le noyau après irradiation.
Comment s’est déroulée l’étude théorique? Quelle est sa portée ?
Larry Bodgi et Nicolas Foray ont modélisé mathématiquement toutes les étapes qui mènent la protéine ATM du cytoplasme au noyau. Dans un premier temps, l’oxydation produite par l’irradiation entraîne un changement de forme de la protéine ATM. Ce changement facilite son passage dans le noyau. Une ATM active alors la reconnaissance des cassures double-brin de l’ADN (CDB), ce qui déclenche leur réparation. Résultat de cette modélisation, la formule mathématique finale reliant la survie cellulaire à la dose de radiation s’est avérée identique à celle du modèle empirique (dit linéaire-quadratique), proposé dans les années 70. Grâce à cette étude théorique, on peut désormais mieux comprendre pourquoi une cellule est radiosensible et quelles peuvent être les conséquences d’un défaut de reconnaissance ou de réparation des CDB après irradiation au niveau cellulaire. Il restait à le valider au niveau du patient à travers une étude biologique et clinique pour prédire les effets secondaires indésirables de la radiothérapie.
Comment s’est déroulée l’étude biologique et clinique? Quelle est sa portée ?
Sur les 380 000 cas de cancers par an, la moitié des patients est traitée par radiothérapie. De 5 à 20% de ces patients peuvent subir des réactions tissulaires indésirables qui vont de la simple rougeur aux brûlures radioinduites voire, dans des cas exceptionnels à la mort. A partir de la collection COPERNIC, les cellules de chaque patient ont été amplifiées en laboratoire puis irradiées dans des conditions exactes d’une session de radiothérapie (une dose de 2 Gy[1]). Les chercheurs du groupe de radiobiologie de l’unité Inserm 1052 ont analysé la vitesse de réparation des CDB en utilisant 3 biomarqueurs d’immunofluorescence, (une technique permettant la visualisation de certaines protéines sur le site-même des cassures de l’ADN) appliqués dans de nombreuses conditions d’irradiation. En parallèle, les 50 radiothérapeutes co-auteurs de l’étude, ont fourni les données cliniques spécifiques de chaque patient avec notamment le grade[2] de sévérité des réactions tissulaires (grade 0, pas de réaction ; grade 5, décès du patient), reflétant sa radiosensibilité tissulaire. Une corrélation significative a été obtenue entre la vitesse du transit de la protéine ATM et le grade de sévérité des réactions tissulaires radioinduites. Une telle corrélation reste valable quel que soit le type de cancer traité ou le caractère précoce ou tardif de la réaction tissulaire indésirable après radiothérapie. A partir de cette corrélation, une classification de la radiosensibilité humaine en 3 groupes :
- Groupe I : Transit rapide d’ATM : radiorésistance
- Groupe II : Transit d’ATM retardé : radiosensibilité modérée.
- Groupe III : Défaut massif de la reconnaissance ou de réparation des CDB : hyper radiosensibilité
Cette classification permet aujourd’hui d’anticiper les stratégies de soins des traitements radio-thérapeutiques car cette approche est aussi valable pour les tumeurs. Compte tenu de l’impact et des applications de ces travaux, des brevets ont été déposés en collaboration avec la start-up Neolys Diagnostics créée en 2014 avec le soutien d’Inserm transfert et de la SATT de Lyon. Neolys Diagnostics a pour but d’industrialiser les tests de radiosensibilité issus de ces 2 études afin de donner aux radiothérapeutes un nouvel outil pour mieux personnaliser le traitement radiothérapique anti-cancéreux.
Soutiens financiers
Ces deux études s’inscrivent dans le cadre des Investissements d’Avenir (projet INDIRA, Radioprotection et Sûreté Nucléaire) dirigé par le Commissariat Général à l’Investissement. Les autres soutiens financiers sont : l’Association pour la recherche sur l’Ataxie Telangiectasie (APRAT), les appels d’offres AVIESAN-Plan Cancer (programmes Physicancer et Santé et Environnement), le Comité de radioprotection d’EDF, le Centre National d’Etudes Spatiales (CNES), le cancéropôle Rhône-Alpes Auvergne CLARA (programmes Oncostarter et Preuve du Concept) Toutes les expériences ont été effectués dans le Centre anti-cancer Léon-Bérard de Lyon.
[1] L’unité de dose de radiation est le Gray (Gy).
[2] Des échelles internationales consensuelles permettent aujourd’hui de classer des réactions tissulaires quelle que soit la localisation et les organes concernés (Ex : échelles CTCAE et RTOG)