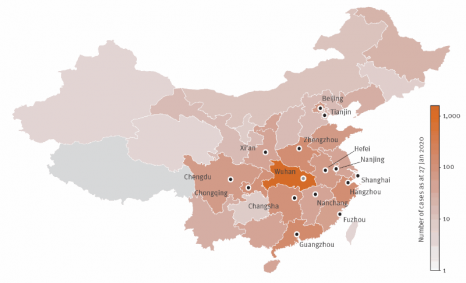
Carte des provinces chinoises affectées par l’épidémie, colorées en fonction du nombre de cas du virus, au 27 janvier 2020. Crédits Vittoria Colizza
L’Inserm est signataire de la déclaration internationale suivante, émise par le
Wellcome Trust [1] :
Partager les données et les résultats de la recherche concernant l’épidémie de nouveau coronavirus (nCoV)
L’apparition du nouveau coronavirus en Chine (2019-nCoV) représente une menace importante et urgente pour la santé mondiale. Nous appelons les chercheurs, les revues et les bailleurs de fonds à veiller à ce que les résultats de la recherche et les données relatives à cette épidémie soient partagés rapidement et ouvertement afin d’éclairer la réponse de santé publique et de contribuer à sauver des vies.
Nous affirmons notre attachement aux principes énoncés dans la déclaration de 2016 sur le partage des données dans les situations d’urgence en matière de santé publique, et nous nous efforcerons de faire en sorte que l’Organisation mondiale de la santé ait rapidement accès aux nouvelles découvertes susceptibles d’aider la réponse mondiale.
Plus précisément, nous nous engageons à travailler ensemble pour contribuer à garantir que :
– toutes les publications de recherche évaluées par des pairs et pertinentes pour l’épidémie soient immédiatement mises en libre accès, ou librement disponibles au moins pendant la durée de l’épidémie
– les résultats des recherches concernant l’épidémie soient immédiatement communiqués à l’OMS sur présentation de la revue, par la revue et avec la connaissance de l’auteur
– les résultats de la recherche soient mis à disposition en pré-print avant la publication de la revue, ou via des plateformes qui rendent les articles librement accessibles avant l’examen par les pairs, avec des déclarations claires concernant la disponibilité des données sous-jacentes
– les chercheurs partagent les données provisoires et finales de la recherche relatives à l’épidémie, ainsi que les protocoles et les normes utilisés pour collecter les données, aussi rapidement et largement que possible – y compris avec les communautés de la santé publique et de la recherche et l’OMS
– les auteurs indiquent clairement que les données ou les pré-print partagés avant la soumission ne préjugeront pas de leur publication dans ces revues.
Nous avons l’intention d’appliquer les principes de cette déclaration à des épidémies similaires à l’avenir, lorsqu’il y aura un avantage significatif pour la santé publique à garantir que les données soient partagées largement et rapidement.
Les coronavirus, qui doivent leur nom à la forme de couronne qu’ont les protéines qui les enrobent, sont une famille de virus dont le réservoir est traditionnellement animal. Dans certains cas, une transmission de l’animal à l’humain est possible, comme l’ont montré les coronavirus SRAS, MERS et probablement ce nouveau virus.
Si ces virus sont majoritairement bénins chez l’humain, deux épidémies ayant entraîné des décès ont été recensées ces dernières années au Moyen Orient (MERS-CoV, 2012-2013) et en Chine dix ans plus tôt (SRAS-CoV, 2002-2003). Pour cette troisième épidémie, le foyer proviendrait d’un marché aux poissons et fruits de mer de Wuhan, où sont également vendus des animaux vivants. La recherche du réservoir et de l’hôte est en cours.
L’Inserm est d’ores et déjà mobilisé pour répondre à l’épidémie, sous l’action du consortium REACTing, qui rassemble des groupes de recherche français d’excellence. Plusieurs initiatives ont été lancées :
- La consolidation d’un « groupe modélisation » mis en place à la demande de REACTing, pour modéliser la propagation possible de l’épidémie en France et en Europe, et anticiper son impact sur les populations.
- Le travail confié à Bruno Lina (Unité Inserm 1111 – Centre International de Recherche en Infectiologie, CIRI) pour proposer un projet de recherche sur les cibles thérapeutiques potentielles afin d’identifier des molécules capables d’agir sur plusieurs types de coronavirus
- Un appui à la recherche clinique, à travers la diffusion auprès des partenaires français et internationaux de REACTing des bonnes pratiques en matière de protocoles de recherche / standardisation de la collecte de données.
Manuel Rosa-Calatrava, chercheur Inserm dans l’équipe VirPath au sein du Centre International de Recherche en Infectiologie (CIRI) est mobilisé aux côtés de ses collègues dans le cadre de REACTing, pour mettre au point plusieurs modèles d’infection in vitro et ex vivo du virus 2019 n-CoV, afin de tester des traitements antiviraux innovants.
Les chercheurs menés par Manuel Rosa-Calatrava travaillent également au développement et à la validation d’une stratégie de repositionnement de médicaments pour de nouvelles indications thérapeutiques antivirales. Ils avaient déjà repositionné in vitro deux molécules disponibles sur le marché contre des virus respiratoires, dont le MERS-CoV. L’idée est maintenant de tester ces deux molécules en lignée cellulaire et en modèle ex vivo d’épithélium respiratoire humain reconstitué contre le 2019-nCoV.
Le groupe a ainsi l’intention de répondre à l’appel européen coronavirus-2020 en proposant leurs approches de repositionnement de médicaments.
Yazdan Yazdanpanah, directeur de l’Institut immunologie, inflammation, infectiologie et microbiologie à l’Inserm et chef du service maladies infectieuses à l’hôpital Bichat AP-HP (Paris) fait le point sur l’épidémie de coronavirus partie de Chine, et sur ce que l’on sait déjà du nouveau virus 2019-nCOV.
Que sait-on sur le virus à l’heure actuelle ?
On sait qu’il s’agit d’un virus qui appartient à la famille des coronavirus. Au départ, il a probablement été transmis de l’animal à l’homme dans un marché à Wuhan, au centre de la Chine. Ensuite, il y a une transmission d’homme à homme qui a été à l’origine de la présence de ce virus chez des patients en Chine, au Japon, en Thaïlande, aux Etats-Unis.
Quelles sont les interrogations qui subsistent ?
Il y a des questions qui restent encore en suspens. Même si on sait que le réservoir vient probablement du marché de Wuhan, on ne sait pas encore quel est l’animal à l’origine de la transmission. Par ailleurs, même si on sait qu’il y a une transmission de personne à personne, on ne connaît pas encore la durée d’incubation, c’est-à-dire le délai entre la rencontre avec le virus et l’apparition des symptômes. C’est un point important pour mettre en place des interventions afin d’arrêter la maladie. Ce qui est bien, c’est qu’on a déjà des outils diagnostics, mais on n’a pas encore de traitements ou de vaccins.
Quelle est la capacité du virus à muter ?
Au début, c’est probablement un virus qui existait chez l’animal et qui a un peu muté pour devenir adaptable à l’homme. Les coronavirus ont une capacité à muter, mais on ne sait pas si ce sera le cas ici et je ne suis pas sûr que ce soit la question pressante aujourd’hui. La grande question c’est d’identifier les malades, et de les isoler pour essayer d’arrêter la transmission. Ensuite, il faut continuer à surveiller pour s’assurer que nos outils diagnostics continuent à fonctionner.
Comment a-t-on développé les outils diagnostics ? Cela a-t-il nécessité un envoi du virus en France par les Chinois ?
Des séquences du virus ont été isolées en Chine et transmises à l’ensemble des chercheurs dans le monde. A partir de là, des outils diagnostics ont été développés. Ce n’est pas le virus entier qui a été envoyé, mais les séquences ARN, et apparemment il serait difficile de le cultiver.
Quels sont les symptômes à surveiller ?
Les symptômes principaux sont de la fièvre, un syndrome pseudogrippal, des maux de têtes, des douleurs dans les articulations et les muscles dans un premier temps. Dans un deuxième temps, des signes respiratoires, toux, crachats et essoufflements, jusqu’à des pneumonies qui peuvent être sévères dans les cas les plus graves. En sachant que l’on peut aussi développer seulement ce qui s’apparente à un simple rhume.
Quel est le dispositif de prévention mis en place en France à l’heure actuelle ? Pourquoi certains dispositifs mis en place dans d’autres pays n’ont pas été adoptés ?
La France a mis en place l’information des passagers via des messages dans les avions et des affiches. Pour le moment, elle n’a pas mis en place des mesures de contrôle de température, mais il faut savoir que ce dispositif de surveillance est très débattu. Tout le monde n’est pas d’accord qu’il s’agit d’un outil très sensible et spécifique pour essayer de détecter les malades.
Quelles précautions en France pour les voyageurs arrivant de Wuhan ?
En revenant de Wuhan, si on a de la fièvre et des problèmes respiratoires, il faut appeler le centre 15, qui redirige vers les infectiologues. Ensemble, ils décident si vous devez être hospitalisés ou pas, afin de rechercher le virus.
Au niveau individuel, quelles sont les mesures barrières recommandées ?
La transmission d’homme à homme se fait par voie respiratoire et aussi par contact entre les mains. Il faut donc mettre un masque et se laver fréquemment les mains.
Quelles sont les priorités de recherche et comment l’Inserm est-il impliqué ?
L’Inserm et le réseau REACTing a réuni les chercheurs. Nous avons identifié les questions de recherche. La question du traitement bien sûr. Des chercheurs français, notamment l’équipe de Bruno Lina à Lyon qui ont des candidats pour le traitement qu’il faut maintenant évaluer. Mais aussi la question de toute la partie diagnostique qui est en train d’être développée pour obtenir des tests plus rapides, ainsi que celle de la surveillance des mutations. Enfin, des chercheurs Inserm et Pasteur qui suivent la dynamique de l’épidémie avec des modélisations.
[1] Liste des signataires : Academy of Medical Sciences, UK; African Academy of Sciences; Assistant Secretary for Preparedness and Response / Biodefense Advanced Research and Development Authority, USA; Austrian Science Fund (FWF), Bernhard Nocht Institute for Tropical Medicine (BNITM); Bill & Melinda Gates Foundation; BioRxiv; Biotechnology and Biological Sciences Research Council (BBSRC), UK; Bulletin of the World Health Organization; The British Medical Journal (BMJ); Calouste Gulbenkian Foundation – Gulbenkian Science Institute; Canadian Institutes of Health Research; Centers for Disease Prevention and Control (CDC), USA; Chinese Centre for Disease Control and Prevention; The Department for International Development (DFID); DG Research & Innovation, European Commission; Dutch Research Council (NWO); eLife; EcoHealth Alliance; EMBO; Epicentre – MSF; European Respiratory Journal ; ERJ Open Research; F1000 Research Limited; Fondation Merieux; Food & Drug Administration, USA; French National Research Agency (ANR); The Global Health Network; Global Virus Network; GLOPID-R ; Inserm (Institut national de la santé et de la recherche médicale), France ; The Institut Pasteur; International Severe Acute Respiratory and emerging Infection Consortium (ISARIC); International Society for Infectious Diseases (ISID); Japan Agency for Medical Research and Development (AMED); Johnson & Johnson; The Lancet Luxembourg National Research Fund (FNR); Medical Research Council (UK); Médecins Sans Frontières/Doctors Without Borders (MSF); MedRxiv; Merck Research Laboratories; Microbide Limited National Academy of Medicine, USA; National Institutes of Health (NIH), USA; National Institute for Infectious Diseases Lazzaro Spallanzani, Italy; New England Journal of Medicine; Office of Global Affairs, Department of Health and Human Services, USA; Portland Press; PLOS; The Research Council of Norway; The Royal Society; Science Europe; Science Foundation Ireland ; ScienceOpen; South African Medical Research Council Takeda; Taylor & Francis; ZonMW – The Netherlands Organisation for Health Research and Development
Ces contenus pourraient aussi vous intéresser :