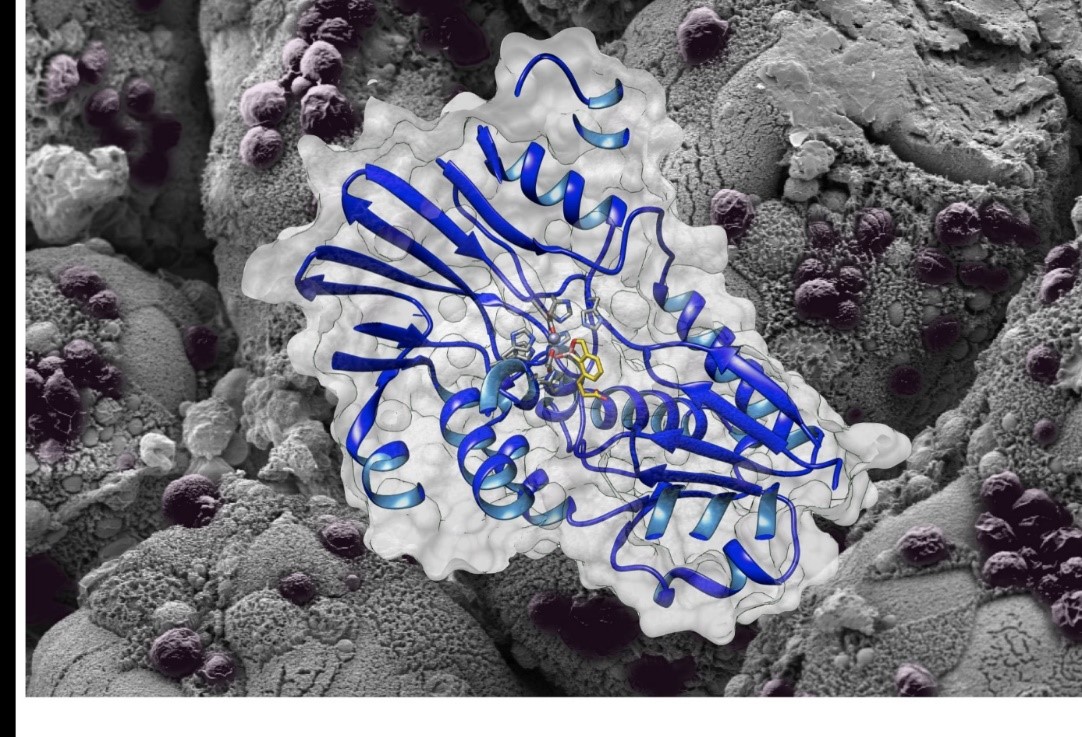
Structure 3D de l’enzyme avec la molécule AN3661 sur fond de l’intestin d’une souris immunodéficiente infectée par Cryptosporidium. ©Fabrice Laurent et Christopher Swale
Des chercheurs de l’Inserm et de l’INRA regroupés au sein des équipes de Mohamed-Ali Hakimi (Institute for Advanced Biosciences – Inserm U 1209 / CNRS UMR 5309 / UGA) et de Fabrice Laurent (INRA) viennent de découvrir un nouveau candidat-médicament pour contrôler la cryptosporidiose, une maladie intestinale grave chez l’enfant, les patients immunodéprimés et les jeunes ruminants. Au-delà de cette maladie, ces travaux sont une piste pour trouver de nouvelles pistes thérapeutiques pour d’autres infections apparentées comme la toxoplasmose ou le paludisme. Ces travaux sont publiés dans Science Translational Medicine.
La cryptosporidiose est une maladie diarrhéique causée par un parasite microscopique, Cryptosporidium, lequel se développe dans l’intestin de nombreux mammifères, notamment dans celui de l’homme. Ce parasite intestinal se propage principalement par la contamination d’eau de consommation ou de baignade où il peut survivre plusieurs jours dans les eaux chlorées, ou encore par le contact avec des animaux infectés. Au cours des 20 dernières années, l’infection par Cryptosporidium a été reconnue comme une cause fréquente de maladie hydrique chez l’homme. Selon une récente étude des Centres pour le contrôle et la prévention des maladies américains (CDC), le nombre d’épidémies à Cryptosporidium est même en augmentation. Chez l’Homme, il provoque des diarrhées aiguës, parfois fatales chez les populations les plus vulnérables comme l’enfant en bas âge souffrants de malnutrition, ou les patients immunodéprimés (par exemple ceux infectés par le VIH). Les moyens thérapeutiques sont actuellement très limités et dans certains cas inefficaces pour éliminer ce parasite.
L’étude menée par les chercheurs de l’Inserm et de l’INRA révèle la découverte d’un candidat-médicament, appelé AN3661, qui réduit drastiquement l’infection de Cryptosporidium mais également celle de Toxoplasma, le parasite responsable de la toxoplasmose.
Les équipes de recherche révèlent aujourd’hui le mécanisme d’action de cette molécule en résolvant la structure tridimensionnelle de sa cible, appelé CPSF3, chez Cryptosporidium. AN3661 se lie au cœur de l’enzyme CPSF3 et empêche ainsi la maturation des ARN messagers, un processus essentiel à la survie du parasite. Des essais précliniques en modèle murin montrent une efficacité remarquable in vivo avec des traitements de l’infection en dose unique chez des souriceaux ou des souris immunodéprimées.Cette découverte majeure ouvre la voie vers de nouvelles stratégies et innovations thérapeutiques pour lutter contre la cryptosporidiose mais aussi les autres infections apparentées comme la toxoplasmose ou le paludisme.
Ces contenus pourraient aussi vous intéresser :
Metal-Captured Inhibition of pre-mRNA Processing Activity by CPSF3 controls very efficiently Cryptosporidium Infection. Christopher Swale1, Alexandre Bougdour1, Audrey Gnahoui-David2, Julie Tottey2, Sonia Georgeault3, Fabrice Laurent2*, Andrés Palencia1,4*†, Mohamed-Ali Hakimi1*† 1Institute for Advanced Biosciences (IAB), Host-Pathogen Interactions and Immunity to Infection, INSERM U1209, CNRS UMR 5309, University Grenoble Alpes, 38000 Grenoble, France. 2 INRA, Université François Rabelais de Tours, Centre Val de Loire, UMR1282 ISP, Laboratoire Apicomplexes et Immunité Mucosale, 37380 Nouzilly, France. 3Plateforme des Microscopies, Université et CHRU de Tours, 37000 Tours, France. 4Institute for Advanced Biosciences (IAB), Structural Biology of Novel Drug Targets in Human Diseases, INSERM U1209, CNRS UMR 5309, University Grenoble Alpes, 38000 Grenoble, France. *Corresponding author. Email: rf.mresni@imikah.ila-demahom (M.-A.H.); andres.palencia@univ- grenoble-alpes.fr (A.P.); rf.arni@tnerual.ecirbaf (F.L.) †These authors contributed equally to this work. Science Translational Medicine https://dx.doi.org/10.1126/scitranslmed.aax7161