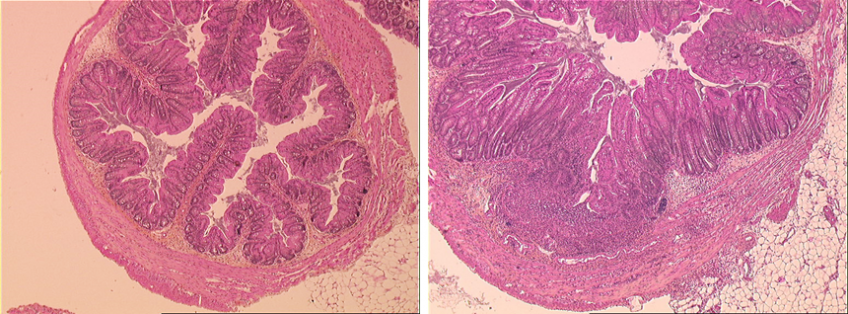
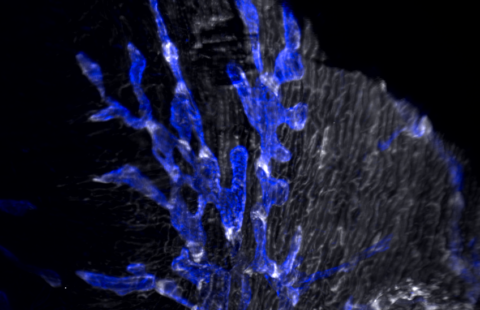
Les modifications du microbiote intestinal dans les maladies inflammatoires chroniques de l’intestin (maladie de Crohn et rectocolite hémorragique) sont à la fois cause et conséquence de ces dérèglements internes. C’est ce que montre une équipe de chercheurs français associant l’Inserm, l’Inra[1], l’UPMC et l’AP-HP qui décrit ces mécanismes et propose de nouvelles pistes thérapeutiques. Leurs travaux sont publiés le 9 Mai 2016 dans Nature Medicine
(c) Harry Sokol – Inserm
Les maladies inflammatoires chroniques de l’intestin (MICI) se caractérisent par une inflammation inappropriée du tube digestif. Elles évoluent par poussées inflammatoires de durée et de fréquence variables selon les patients. Ces maladies touchent le plus souvent de jeunes adultes et leur fréquence est plus élevée dans les pays industrialisés. Les chercheurs ont déjà découvert plusieurs gènes de susceptibilité comme NOD2, ATG16L1 ou encore CARD9 mais suspectent également des facteurs environnementaux et des modifications de la flore intestinale, sans que l’on sache quand et comment ces facteurs interviennent.
Or, le gène CARD9 code pour une protéine impliquée dans le système immunitaire et notamment dans la reconnaissance des micro-organismes. « L’association entre ce gène de prédisposition, l’immunité et les bactéries méritait d’être fouillée compte tenu du fait que tous ces acteurs sont impliqués dans les MICI », explique Harry Sokol, responsable de ces travaux.
Pour cela, son équipe a utilisé des souris déficientes pour ce gène. Les chercheurs ont alors constaté une sensibilité exacerbée de leur intestin en cas d’inflammation avec un défaut de cicatrisation de la muqueuse, associé à un déficit en interleukine (IL) 22 et à des perturbations de la flore bactérienne. Des observations qui ne les ont pas réellement surpris compte tenu du fait que « la protéine CARD9 exprimée par les cellules immunitaires, contribue à la production d’IL22 impliquée dans la cicatrisation et la protection de la muqueuse intestinale, ainsi qu’à la reconnaissance des micro-organismes », rappelle Harry Sokol.
Sauf qu’en transplantant la flore intestinale de ces animaux génétiquement modifiés à d’autres souris génétiquement indemnes mais sans flore intestinale, ces dernières sont devenues à leur tour, hypersensibles à l’inflammation intestinale. En outre, elles présentaient également un défaut de production d’IL22. « Autrement dit, le défaut génétique en lui-même n’est pas suffisant pour induire les dysfonctionnements observés. Les altérations de la composition de la flore intestinale qui découle de l’absence de CARD9 jouent un rôle majeur dans l’hypersensibilité intestinale et le défaut fonctionnel de la voie IL22 », clarifie Harry Sokol.
Les chercheurs ont donc voulu comprendre comment cette flore intestinale altérée pouvait conférer ces anomalies à l’animal receveur. Ils ont alors constaté que les bactéries présentes ne pouvaient pas, ou mal, transformer le tryptophane, un acide aminé apporté par l’alimentation, en dérivé indole qui se fixe sur des lymphocytes et stimule la production d’Il 22. Une observation qui a amené les chercheurs à conclure qu’une « mutation sur le gène CARD9 entraine une modification de la flore intestinale par l’intermédiaire d’un dysfonctionnement du système immunitaire. Celle-ci perd sa capacité à produire des dérivés indoles, contribuant à renforcer les anomalies immunitaires notamment de la voie Il22, propices à l’inflammation.
Ces résultats montrent combien tous ces mécanismes sont imbriqués ; génétique, système immunitaire et microbiote, résume Harry Sokol. Ainsi, les anomalies du microbiote dans les MICI sont à la fois cause et conséquence de l’inflammation».
Mais les chercheurs ont surtout montré que ces mécanismes étaient réversibles. En administrant des molécules capables de mimer les dérivés indoles à des souris déficientes en gène CARD9, ils ont observé une rémission des symptômes et un rétablissement normal de la voie Il22. Des résultats passionnants mais encore faut-il montrer qu’il en va de même chez l’homme. Les chercheurs ont déjà effectué une analyse de selles chez une centaine de patients atteints de MICI et ont constaté une diminution généralisée de la production de dérivés indoles par les bactéries intestinales par rapport à des sujets sains. En doublant ce travail d’une analyse génétique à la recherche de variants de gènes de susceptibilité, ils ont constaté que ce défaut était particulièrement sévère chez les patients présentant une mutation sur le gène CARD9. L’idée est maintenant de compenser ce déficit chez les malades. « On peut déjà très facilement repérer les patients ayant un défaut de production de dérivés indoles à partir d’une simple analyse de selles. Il suffirait donc de supplémenter ces patients en bactéries productrices de ces dérivés ou encore en leur administrant directement le dérivé en question ». Des travaux déjà engagés au sein du laboratoire.
[1] Equipe « Interactions des commensales et probiotiques avec l’hôte », Institut MICALIS (Inra-AgroParisTech), Jouy en Josas