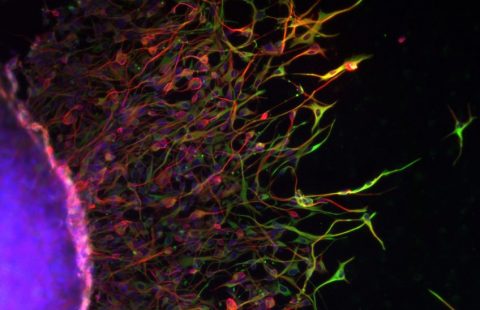
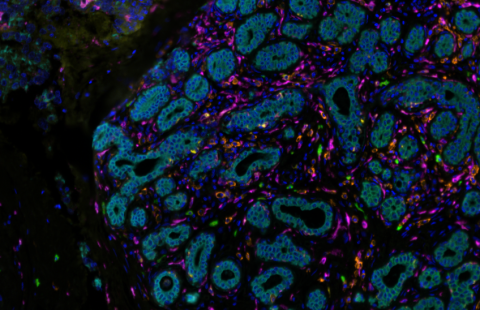
Organoïde neuronal avec environnement immunitaire grossi deux fois à gauche, 20 fois à droite : en vert les macrophages, en rouge et bleu les cellules neuronales progénitrices (microscopie à fluorescence) © Gustave Roussy
Organoïde neuronal avec environnement immunitaire grossi deux fois à gauche, 20 fois à droite : en vert les macrophages, en rouge et bleu les cellules neuronales progénitrices (microscopie à fluorescence) © Gustave Roussy
Des chercheurs français, singapouriens et anglais, menés par le Pr Florent Ginhoux, directeur d’une équipe de recherche à Gustave Roussy/Inserm, ont réussi à mettre en évidence dans un organoïde neuronal le rôle de l’environnement immunitaire du cerveau dans sa formation et son développement. La mise au point de ces structures en trois dimensions intégrant cellules neuronales et environnement immunitaire, est, à ce jour, un des modèles in vitro qui reflète de manière la plus complète le cerveau humain. Ces travaux sont publiés dans la revue Nature.
À Gustave Roussy, ces organoïdes sont utilisés pour modéliser le développement des cancers du cerveau de l’enfant, pour en comprendre les mécanismes et découvrir de nouvelles pistes de traitement.
« Si l’on sait que les cellules microgliales, cellules immunitaires issues de l’évolution (différenciation) de macrophages primitifs présents dans le cerveau embryonnaire, contribuent à de multiples aspects du développement et du fonctionnement du cerveau, leur rôle précis reste mal connu et peu étudié », déclare le Pr Florent Ginhoux, directeur d’une équipe de recherche à Gustave Roussy/Inserm et chercheur au Singapore Immunology Network A*STAR (SIgN) au moment des travaux. L’utilisation d’organoïdes neuronaux pour étudier leurs fonctions est une des voies aujourd’hui privilégiée par la recherche.
Un organoïde est une structure en 3D cultivée au laboratoire qui reproduit certaines caractéristiques morphologiques et fonctionnelles d’un organe ou d’un tissu du corps humain. En recherche, ces pseudo-organes issus de cultures cellulaires sont un nouveau modèle biologique en plein développement dans différents domaines, notamment en neurologie ; la plupart des études portant sur la formation des neurones (neurogenèse) étant réalisée à partir de modèles animaux.
Avec une structure en 3D, le fonctionnement et les propriétés de ces organoïdes se rapprochent de ceux d’un véritable organe sans pour autant être aussi abouti. Ils mesurent un millimètre et n’ont pas de pensées, de conscience ou d’émotion. En générant des organoïdes neuronaux à partir de cellules souches pluripotentes humaines induites dites « cellules iPS » (cellules spécialisées qui sont déprogrammées pour être reprogrammées différemment), il est possible de modéliser certaines caractéristiques clés du développement précoce du cerveau humain. « Cependant, les approches actuelles n’intègrent pas les cellules microgliales », précise le Pr Florent Ginhoux.
L’équipe internationale de chercheurs dirigée par le Pr Florent Ginhoux, a réussi à produire un nouveau type de modèle : des organoïdes neuronaux pourvus de microglie en cultivant ensemble des organoïdes, et des macrophages de type primitif, tous générés à partir d’une même culture de cellules souches induites iPS.
Les organoïdes et les macrophages de type primitifs sont d’abord préparés séparément. Il faut environ 25 jours pour les obtenir. Les macrophages sont ensuite mis au contact des organoïdes pendant 15 à 20 jours supplémentaires.
Dans le modèle que les chercheurs ont développé, les macrophages ont colonisé les organoïdes. Dans cet environnement 3D, en contact avec les cellules neuronales immatures, ils se sont différenciés en de cellules microgliales exprimant les gènes et les fonctions propres à ce type cellulaire. Ces cellules microgliales se sont révélées capables de contrôler la différenciation de précurseurs de neurones (dites cellules progénitrices neuronales), limitant ainsi leur multiplication (prolifération), tout en favorisant la création de synapses (synaptogenèse) et la croissance des axones (axonogenèse), deux éléments clés de la transmission du message nerveux de neurone à neurone.
Une découverte dans la découverte
L’équipe du Pr Florent Ginhoux a également observé que les cellules microgliales des organoïdes contiennent des niveaux élevés de périlipine 2, une molécule appartenant à une famille de protéines qui enrobent les lipides – dont le cholestérol – dans des gouttelettes, ce qui permet leur stockage dans les cellules et leur exportation hors de ces dernières. Armées de ces gouttelettes chargées en périlipine 2, les cellules microgliales facilitent le transport du cholestérol vers les organoïdes. Les cellules progénitrices neuronales qui absorbent ce cholestérol subissent alors une véritable reprogrammation métabolique durant leur processus de différenciation en cellules nerveuses.
L’approche développée par le Pr Florent Ginhoux et ses collaborateurs fait progresser de manière très significative la complexification des modèles d’organoïdes en y intégrant des cellules microgliales. Progrès que les chercheurs ont illustré par la découverte d’une voie clé de dialogue, portée par les lipides, entre la microglie et les cellules progénitrices neuronales, primordiale pour la synthèse de nouveaux neurones.
« Avec les cellules de la microglie incorporées, les organoïdes neuronaux que nous avons réussi à générer sont un nouveau modèle 3D plus complet et plus proche de la réalité. Nous savons que le système immunitaire joue un rôle fondamental dans le développement des cancers et à Gustave Roussy nous allons donc les utiliser pour mieux comprendre et découvrir les mécanismes qui régulent le développement des tumeurs cérébrales pédiatriques », conclut le Pr Florent Ginhoux.
Ces travaux ont été soutenus par la campagne « Guérir le cancer de l’enfant au 21e siècle » de la Fondation Gustave Roussy.
Ces contenus pourraient aussi vous intéresser :
iPSC-microglia promote brain organoid maturation via cholesterol transfer
Nature, Publié le 9 novembre, publication avancée en ligne le 1er novembre 2023
https://doi.org/10.1038/s41586-023-06713-1
Dong Shin Park1,2,*, Tatsuya Kozaki1,*, Satish Kumar Tiwari1, Marco Moreira3, Ahad Khalilnezhad1,2, Federico Torta4,5, Nicolas Olivié6, Chung Hwee Thiam2, Oniko Liani1, Aymeric Silvin1,3, Wint Wint Phoo7, Liang Gao4,5, Alexander Triebl4,5, Wai Kin Tham5, Leticia Gonçalves3, Wan Ting Kong1,3, Sethi Raman1, Xiao Meng Zhang1, Garett Dunsmore3, Charles Antoine Dutertre1,3, Salanne Lee1, Jia Min Ong1, Akhila Balachander1, Shabnam Khalilnezhad1,8, Josephine Lum1, Kaibo Duan1, Ze Ming Lim1, Leonard Tan1, Ivy Low1, Kagistia Hana Utami9, Xin Yi Yeo10, Sylvaine Di Tommaso11, Jean-William Dupuy12, Balazs Varga13, Ragnhildur Thora Karadottir13, Mufeeda Changaramvally Madathummal14, Isabelle Bonne2, Benoit Malleret1,2,14, Zainab Yasin Binte1, Ngan Wei Da1, Yingrou Tan1, Wei Jie Wong15, Jinqiu Zhang9, Jinmiao Chen1, Radoslaw M. Sobota7, Shanshan W. Howland1, Lai Guan Ng1, Frédéric Saltel11, David Castel16, Jacques Grill16, Veronique Minard3, Salvatore Albani8, Jerry K.Y. Chan17, Morgane Sonia Thion6, Jung Sangyong10, Markus R. Wenk4,5, Mahmoud A. Pouladi9, Claudia Pasqualini3, Veronique Angeli2, Olivier NF. Cexus5,10,18 and Florent Ginhoux1,2,3,8,15,#
1 Singapore Immunology Network (SIgN), Agency for Science, Technology and Research, Singapore 138648, Singapore,
2 Department of Microbiology and Immunology, Yong Loo Lin School of Medicine, National University of Singapore, Singapore 117545, Singapore,
3 INSERM U1015, Gustave Roussy Cancer Campus, Villejuif 94800, France
4 Department of Biochemistry, Yong Loo Lin School of Medicine, National University of Singapore, Singapore 117596, Singapore,
5 Singapore Lipidomics Incubator (SLING), Life Sciences Institute, National University of Singapore,
Singapore 119228, Singapore,
6 Institut de Biologie de l’Ecole Normale Supérieure (IBENS), Ecole Normale Supérieure, CNRS, INSERM, PSL Research University, Paris 75005, France,
7 Functional Proteomics Laboratory, SingMass National Laboratory, Institute of Molecular and Cell Biology, Agency for Science, Technology and Research, 61Biopolis Drive, #07-03, Singapore 138673, Singapore,
8 Translational Immunology Institute, SingHealth Duke-NUS Academic Medical Centre, Singapore 169856, Singapore,
9 Translational Laboratory in Genetic Medicine (TLGM), Agency for Science, Technology and Research, Singapore 138648, Singapore,
10 Institute of Molecular and Cell Biology (IMCB), Agency for Science, Technology and Research, Singapore 138673, Singapore,
11 Oncoprot Platform, TBM-Core US 005, F-33000 Bordeaux, France,
12 Bordeaux Protéome, University of Bordeaux, 33076, Bordeaux, France,
13 Wellcome Trust-Medical Research Council Cambridge Stem Cell Institute and Department of Veterinary Medicine, University of Cambridge, Cambridge, CB2 0AW, UK.,
14 A*STAR Microscopy Platform Electron Microscopy, Research Support Centre, Agency for Science, Technology and Research (A*STAR), Singapore 138673, Singapore,
15 Shanghai Institute of Immunology, Department of Immunology and Microbiology, Shanghai Jiao Tong University School of Medicine, Shanghai 200025, China,
16 INSERM U981, Molecular Predictors and New Targets in Oncology & Département de Cancérologie de l’Enfant et de l’Adolescent, Gustave Roussy, Université Paris-Saclay, Villejuif 94805, France,
17 Department of Reproductive Medicine, KK Women’s and Children’s Hospital, Singapore 229899, Singapore,
18 School of Biosciences, Faculty of Health and Medical Sciences, University of Surrey, Guildford, GU2 7XH, United Kingdom