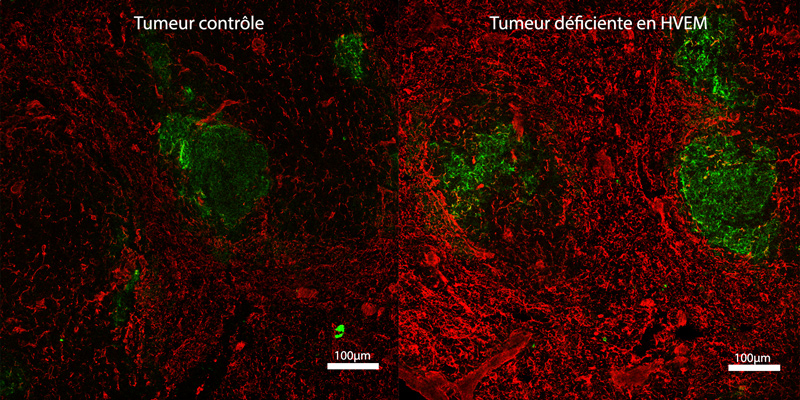
Les marquages fluorescents rouge et vert correspondent à différents types de cellules stromales, constituant la niche tumorale. L’intensité plus forte des deux marquages dans la tumeur déficiente en HVEM reflète une hyperactivation des cellules stromales. Image obtenue par microscopie confocale.
Crédit : F. Mourcin, MICA
On sait aujourd’hui utiliser des cellules immunitaires équipées pour cibler et détruire spécifiquement certains lymphomes. Des chercheurs rennais de l’unité MICA[1], en collaboration avec des collègues américains du MSKCC[2], vont plus loin aujourd’hui en démontrant que ces cellules peuvent être utilisées pour introduire dans la tumeur une molécule d’intérêt médical, identifiée en étudiant les altérations génétiques caractéristiques du lymphome. Ces travaux introduisant le concept de « micro-pharmacie » sont publiés dans la revue Cell datée du 6 octobre 2016.
Les chercheurs se sont intéressés au lymphome folliculaire, l’un des cancers du sang les plus fréquents (3 000 à 4 000 nouveaux cas chaque année en France). Ils ont tout d’abord identifié dans ce type de lymphome des altérations génétiques fréquentes qui aboutissent à une perte d’expression de la molécule HVEM (pour « Herpesvirus entry mediator »).
Ils ont ensuite montré qu’un déficit de cette molécule accélère le développement de tumeurs dans un modèle murin mimant le lymphome folliculaire. En effet, lorsqu’elle est normalement exprimée, la molécule HVEM vient se lier à un récepteur inhibiteur (BTLA pour « B- and T- lymphocyte attenuator) sur les lymphocytes B, limitant le développement du lymphome.
De plus, les chercheurs ont montré que l’absence d’HVEM vient stimuler le recrutement et l’activation de cellules à proximité du lymphome : celles-ci développent alors une « niche tumorale », véritable microenvironnement de soutien à la tumeur.
En laboratoire, l’utilisation de molécule HVEM soluble permet de bloquer à la fois l’activation des cellules cancéreuses et des cellules du microenvironnement de soutien à la tumeur. Cependant cette stratégie n’est pas directement utilisable chez les patients car il faudrait pouvoir amener la molécule thérapeutique directement au sein des tumeurs, ce qui reste très complexe.
Les deux équipes ont alors eu l’idée d’utiliser à cette fin des cellules immunitaires modifiées (CAR-T), actuellement utilisées avec des résultats très prometteurs dans de nombreux essais thérapeutiques. Ces lymphocytes T sont collectés chez les patients et sont équipés d’un récepteur qui les cible spécifiquement sur la tumeur. En introduisant dans les CAR-T le gène codant pour la molécule HVEM soluble, les chercheurs ont pu démontrer qu’on obtient une efficacité supérieure pour éradiquer les tumeurs chez la souris qu’avec les CAR-T classiques.
Ces travaux ont été menés sous la direction du professeur Karin Tarte, directrice de l’unité MICA, et du Dr Hans-Guido Wendel, du MSKCC.
[1] Unité « Microenvironnement et cancer», unité mixte de recherche 917 placée sous la co-tutelle de l’université de Rennes 1, de l’Inserm et de l’Établissement français du sang
[2] MSKCC : Memorial Sloan Kettering Cancer Center, New York (NY, É.-U.)