Contact scientifique
Christel Vérollet
Directrice de recherche Inserm
UMR 5089 CNRS/Université de Toulouse, Institut de pharmacologie et biologie structurale (IPBS)
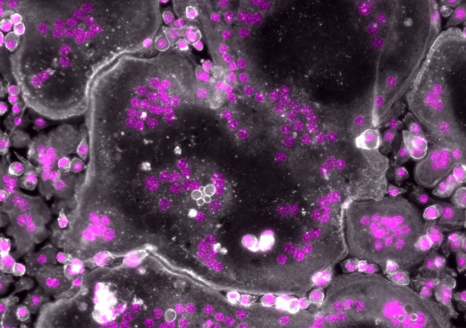 En l’absence de moésine, les ostéoclastes humains présentent des noyaux surnuméraires (en rose). L’actine est représentée en blanc. – Microscopie à fluorescence © Ophélie Dufrançais
En l’absence de moésine, les ostéoclastes humains présentent des noyaux surnuméraires (en rose). L’actine est représentée en blanc. – Microscopie à fluorescence © Ophélie Dufrançais
Comme un arbre, le squelette est vivant. Il se développe et doit être taillé pour rester harmonieux. Pour maintenir cet état, les ostéoclastes endossent le rôle de jardinier, élaguant les os usés. Ces grosses cellules, uniques par leur morphologie et leurs fonctions, jouent un rôle crucial dans l’équilibre du squelette, mais aussi dans certaines maladies osseuses, comme l’ostéoporose et le cancer. Une équipe de chercheuses et chercheurs de l’Inserm, du CNRS et de l’Université de Toulouse, en collaboration avec des équipes internationales, vient de mettre en évidence que leur formation et leur activité sont façonnées par une protéine : la moésine. Leurs travaux, publiés dans The Journal of Cell Biology, montrent que celle-ci contrôle la taille des ostéoclastes ainsi que leur capacité à détruire l’os. Ces découvertes ouvrent de nouvelles pistes qui pourraient, à terme, contribuer au développement de traitements innovants contre les maladies osseuses très souvent liées au vieillissement.
L’os est une structure rigide mais dynamique. Tout au long de la vie, il grandit, se casse, se répare, mais aussi se détériore. Le remodelage osseux est un processus complexe, qui nécessite une coopération entre différentes cellules, parmi lesquelles les ostéoblastes qui participent à la création de l’os, et les ostéoclastes qui le détruisent continuellement. Tout est une question d’équilibre dynamique entre formation et dégradation du tissu osseux.
Une instabilité dans ce processus provoque des maladies et des complications. Avec l’âge notamment, les ostéoclastes deviennent plus agressifs et se mettent à trop dégrader les os, entraînant des défauts et des pertes osseuses caractéristiques du vieillissement et des maladies associées comme l’ostéoporose. Cette hyper-agressivité des ostéoclastes est également observable dans les cancers osseux et métastases qui détruisent l’os.
Des équipes de recherche françaises et internationales, co-coordonnées par Christel Vérollet, directrice de recherche Inserm au sein de l’Institut de pharmacologie et biologie structurale (CNRS/Université de Toulouse), se sont penchées sur la raison de cette suractivité. Dans une nouvelle étude, elles s’intéressent à la moésine, une protéine à multiples fonctions connue notamment pour réguler l’architecture interne des cellules (le cytosquelette), et montrent qu’elle joue un rôle central dans la formation et l’activité des ostéoclastes.
Après avoir enlevé la moésine dans des ostéoclastes de souris pour évaluer les conséquences sur leur formation et leur fonction, les scientifiques ont pu répliquer in vitro les résultats sur des ostéoclastes humains, plus difficiles à cultiver en laboratoire. Ce modèle de souris dénuées de moésine, développé par une équipe à Philadelphie, a permis d’évaluer les conséquences de cette délétion sur l’os et d’obtenir une représentation plus complète – et à l’échelle du vivant – du rôle de cette molécule.
Toutes les observations semblent concorder : la moésine régulerait la formation mais aussi l’agressivité des ostéoclastes. Sans moésine, les ostéoclastes sont plus gros et plus actifs. Chez les souris dépourvues de la protéine, l’augmentation du nombre et de l’activité des ostéoclastes se matérialise par une perte osseuse visible aux scanners mais aussi détectable avec des marqueurs sanguins, similaires à ceux testés chez les patients atteints d’ostéoporose.
« Les ostéoclastes sont uniques. Ce sont les seules cellules du corps à pouvoir dégrader de l’os. Mais ce sont aussi des cellules à plusieurs noyaux car ils naissent de la fusion de plusieurs cellules », explique Christel Vérollet.
Les travaux des chercheuses et chercheurs montrent que la moésine contrôlerait, dans un premier temps, la fusion de ces cellules en régulant la formation de petits ponts à leur jonction (les nanotubes membranaires) qui sont essentiels à la communication entre deux cellules juste avant leur fusion. Dans un second temps, une fois les ostéoclastes formés, cette même moésine réorganiserait leur cytosquelette interne pour réguler leur action de destruction de l’os.
« Nous avons identifié une nouvelle protéine impliquée dans la fusion cellulaire des ostéoclastes. Ces résultats ouvrent la voie à une nouvelle avenue thérapeutique contre le vieillissement et les maladies de l’os, qui ciblerait non pas la viabilité des ostéoblastes, comme envisagé jusqu’à maintenant, mais leur fusion », détaille Christel Vérollet.
Malheureusement, la moésine n’est pas spécifique aux ostéoclastes. Elle joue de multiples rôles dans le corps et dans différentes cellules, ce qui pose un problème pour l’envisager comme cible thérapeutique primaire.
« Identifier des régulateurs de la moésine, spécifiques des ostéoclastes, pourrait avoir les applications thérapeutiques escomptées, à la fois contre le vieillissement osseux mais aussi contre les conséquences désastreuses de certains cancers sur l’os. Mais pour cela, des études sont encore nécessaires », conclut Christel Vérollet.
Une meilleure compréhension du rôle et des interacteurs de cette protéine au carrefour de la fusion cellulaire, de la communication intercellulaire et de la perte osseuse, est la clé de l’aboutissement de ces promesses.
Christel Vérollet
Directrice de recherche Inserm
UMR 5089 CNRS/Université de Toulouse, Institut de pharmacologie et biologie structurale (IPBS)
Moesin controls cell-cell fusion and osteoclast function
The Journal of Cell Biology, 27 octobre 2025
https://doi.org/10.1083/jcb.202409169
Ophélie Dufrancais1, Marianna Plozza1, Marie Juzans2,#, Arnaud Métais1,#, Sarah C Monard1, Pierre-Jean Bordignon1, Perrine Verdys1, Thibaut Sanchez1, Martin Bergert3, Julia Halper4, Christopher J Panebianco5, Rémi Mascarau1, Rémi Gence6, Gaëlle Arnaud1, Myriam Ben Neji1, Isabelle Maridonneau-Parini1, Véronique Le Cabec1, Joel D Boerckel5, Nathan J Pavlos7, Alba Diz-Muñoz3, Frédéric Lagarrigue1, Claudine Blin-Wakkach4, Sébastien Carréno8, Renaud Poincloux1, Janis K Burkhardt2, Brigitte Raynaud-Messina1,9, *¶ and Christel Vérollet1,9, *¶
1 Institut de Pharmacologie et Biologie Structurale (IPBS), Université de Toulouse, Centre National de la Recherche Scientifique, Université Toulouse III – Paul Sabatier (UT3), Toulouse, France
2 Children’s Hospital of Philadelphia Research Institute, University of Pennsylvania Perelman School of Medicine, Philadelphia, PA 19104
3 Cell Biology and Biophysics Unit, European Molecular Biology Laboratory, Heidelberg, Germany
4 Université Côte d’Azur, CNRS, LP2M, Nice, France.
5 Department of Orthopaedic Surgery and Department of Bioengineering, University of Pennsylvania, Philadelphia, PA, USA.
6 Centre de Recherches en Cancérologie de Toulouse, Inserm UMR1037 and Institut Universitaire du Cancer de Toulouse – Oncopôle, Toulouse, France.
7 School of Biomedical Sciences, The University of Western Australia, Nedlands, WA, 6009, Australia.
8 IRIC, Université de Montréal, Montréal, Québec H3C 3J7, Canada.
9 International research laboratory (IRP) CNRS “IM-TB/HIV” Toulouse, France and Buenos Aires, Argentina
# These authors contributed equally to this work
* These senior authors contributed equally to this work