Contact scientifique
Ali Amara
U944 Génome, Biologie Cellulaire et Thérapeutique
Institut de Recherche Saint-Louis
Vassili Soumelis
U976 Immunologie humaine, physiopathologie et immunothérapie – HIPI
Institut de Recherche Saint-Louis
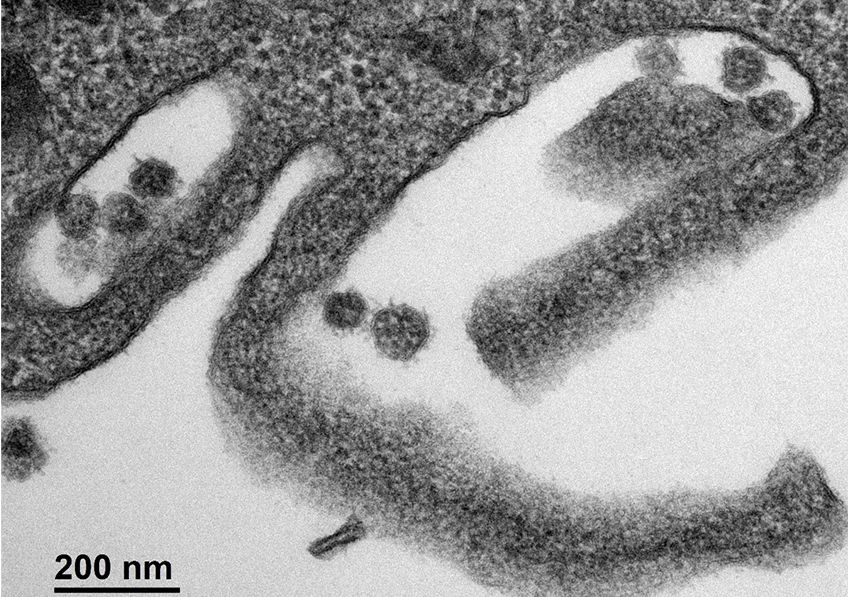
Cellule infectée par le SARS-CoV-2. © Sébastien Eymieux et Philippe Roingeard, INSERM – Université de Tours
Alors que la pandémie de Covid-19 se poursuit, les scientifiques font chaque jour des progrès notables pour mieux comprendre la transmission du coronavirus SARS-CoV-2 ainsi que la réponse immunitaire qu’il déclenche lors d’une infection. Des chercheurs de l’Inserm, de l’AP-HP et Université de Paris, en collaboration avec la Rockefeller University à New-York, apportent de nouvelles données concernant les étapes très précoces de la réponse immunitaire. Les résultats sont publiés dans le Journal of Experimental Medicine.
Comprendre la réponse immunitaire anti-SARS-CoV-2 est une étape essentielle dans l’identification des sujets à risque de maladie Covid-19 grave et dans la mise en place de stratégies thérapeutiques efficaces. Si de nombreuses études ont été réalisées chez des patients à des stades avancés de l’infection, lorsqu’ils présentent déjà des signes de gravité, les étapes très précoces de la réponse immunitaire contre le virus demeurent en grande partie inconnues.
Grâce à une collaboration étroite entre les équipes Inserm d’Ali Amara, virologue, et Vassili Soumelis, immunologiste à l’Institut de Recherche Saint-Louis (Université de Paris/Inserm/AP-HP), une étude publiée dans le Journal of Experimental Medicine a pu caractériser la réponse immunitaire innée[1] dans les 24 à 48h suivant un contact avec le virus SARS-CoV-2.
Les chercheurs ont utilisé des cellules immunitaires appelées « plasmocytoïdes pré-dendritiques » comme modèle de cellules immunitaires innées jouant un rôle essentiel dans l’immunité antivirale en produisant de grandes quantités d’interféron-alpha[2].
L’analyse de cette réponse reconstituée in vitro a permis de montrer que le SARS-CoV-2 induisait une activation efficace et complète des cellules plasmocytoïdes pré-dendritiques. Celles-ci produisaient alors des quantités importantes d’interféron-alpha (première ligne de défense contre les virus) et se différenciaient en cellules dendritiques capables d’activer les lymphocytes T (qui correspondent aux cellules de l’immunité spécifique). Les chercheurs ont par ailleurs pu montrer que cette activation des cellules plasmocytoïdes pré-dendritiques était partiellement inhibée par l’hydroxychloroquine, ce qui inciterait à la prudence dans l’utilisation de cette molécule.
Dans une deuxième partie du travail, les équipes ont collaboré avec l’équipe de Jean-Laurent Casanova de l’Institut Imagine (Inserm/université de Paris/AP-HP) et de la Rockefeller University à New-York, enfin d’étudier la réponse des cellules plasmocytoïdes pré-dendritiques issus de patients présentant des déficits génétiques pour certains gènes importants de l’immunité innée. L’objectif était de préciser les mécanismes moléculaires intervenant dans la réponse de ces cellules immunitaires au SARS-CoV-2.
Ces expériences effectuées à partir de prélèvements directement obtenus des patients ont montré que la réponse des cellules plasmocytoïdes pré-dendritiques est dépendante des molécules UNC93B et IRAK-4, deux molécules importantes de l’immunité innée antivirale. L’ensemble de ce travail permet de préciser la réponse immunitaire précoce au virus SARS-CoV-2 ainsi que certains de ses déterminants moléculaires.
[1] L’immunité innée constitue la première barrière de défense de l’organisme. Elle est déclenchée dès que l’organisme est exposé à une bactérie ou un virus (par exemple le SARS-CoV-2). Les cellules de l’immunité innée peuvent contribuer à détruire totalement les microbes détectés ou les présenter aux mécanismes de l’immunité acquise pour faciliter leur destruction par des mécanismes spécifiques (lymphocytes T et B)
[2] Les interférons sont des cytokines (protéines) dont la production est induite suite à une infection virale, une infection bactérienne, une infection parasitaire ou à la présence de cellule tumorales. Leur fonction principale est d’interférer avec la réplication virale, mais ils ont également une action antibactérienne, antiproliférative et d’activation d’autres cellules immunitaires.
Ali Amara
U944 Génome, Biologie Cellulaire et Thérapeutique
Institut de Recherche Saint-Louis
Vassili Soumelis
U976 Immunologie humaine, physiopathologie et immunothérapie – HIPI
Institut de Recherche Saint-Louis
SARS-CoV-2 induces human plasmacytoid pre-dendritic cell diversification via UNC93B and IRAK4
Fanny Onodi1, Lucie Bonnet-Madin2, Laurent Meertens2, Léa Karpf1, Justine Poirot1,
Shen-Ying Zhang3, 4, 5, Capucine Picard4, 6, 8, Anne Puel3, 4, 5, Emmanuelle Jouanguy3,
4, 5, Qian Zhang5, Jérôme Le Goff 1, 7, Jean-Michel Molina2, 7, Constance Delaugerre2,
7, Jean-Laurent Casanova3, 4, 5, 8, 9, Ali Amara2, # and Vassili Soumelis1, 10
1 Université de Paris, Institut de Recherche Saint-Louis, INSERM U976, Hôpital
Saint-Louis, 75010 Paris, France
2 Université de Paris, Institut de Recherche Saint-Louis, INSERM U944 CNRS 7212,
Hôpital Saint-Louis, 75010 Paris, France
3 Laboratory of Human Genetics of Infectious Diseases, Necker Branch, INSERM,
Necker Hospital for Sick Children, Paris, France, EU
4 Université de Paris; INSERM UMR 1163 Institut Imagine, France EU
5 St. Giles Laboratory of Human Genetics of Infectious Diseases, Rockefeller Branch,
The Rockefeller University, New York, NY, USA
6 Study center for primary immunodeficiencies, Necker Hospital for Sick Children
Assistance Publique-Hôpitaux (AP-HP) de Paris, Paris, France, EU
7 Laboratoire de Virologie et Département des Maladies Infectieuses, Hôpital Saint-
Louis, APHP, 75010 Paris, France
8 Pediatric Hematology and Immunology Unit, Necker Hospital for Sick Children, APHP,
Paris, France, EU
9 Howard Hughes Medical Institute, New York, NY, USA
10 Assistance Publique-Hôpitaux de Paris (AP-HP), Hôpital Saint-Louis, Laboratoire
d’Immunologie, F-75010, Paris, France