Alors qu’il est déjà possible d’obtenir in vitro des cellules pluripotentes (capables de générer tous les tissus d’un organisme) à partir de n’importe quelle cellule, les chercheurs de l’équipe de Maria-Elena Torres Padilla, directrice de recherche Inserm au sein de l’IGBMC (CNRS/Université de Strasbourg/Inserm) à Strasbourg sont parvenus pour la première fois à obtenir des cellules dites totipotentes, ayant les mêmes caractéristiques que celles des tous premiers stades embryonnaires, des cellules aux propriétés encore plus intéressantes. Ces résultats obtenus en collaboration avec Juanma Vaquerizas, du Max Planck Institute (Münster, Allemagne) sont publiés le 3 août dans la revue Nature Structural & Molecular Biology.
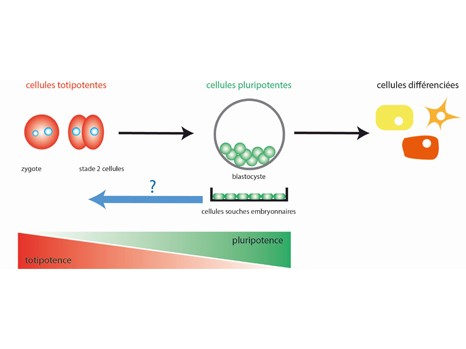
Juste après la fécondation, aux stades 1 ou 2 cellules, les cellules sont dites « totipotentes », c’est-à-dire capables de produire un embryon entier mais également le placenta et le cordon ombilical qui l’accompagnent. Ensuite, au fil des divisions cellulaires et ce jusqu’au stade blastocyste (près d’une trentaine de cellules), les cellules perdent cette plasticité. Devenues « cellules souches embryonnaires », elles sont encore pluripotentes et en mesure de se différencier en n’importe quel tissu. Elles ne peuvent cependant pas à elles seules donner naissance à un fœtus. La totipotence est donc un état beaucoup plus plastique que la pluripotence. Après le stade blastocyste, les cellules se spécialisent et forment les différents tissus de l’organisme, on parle alors des cellules différenciées.
Depuis quelques années, il est possible de transformer une cellule différenciée en une cellule pluripotente, mais pas en cellule totipotente. Afin de mieux comprendre les raisons pour lesquelles ce « retour » à l’état a totipotent n’était pas accessible, l’équipe de Maria-Elena Torres-Padilla s’est attelée à observer les caractéristiques des cellules totipotentes et à rechercher les facteurs d’induction de cet état.
A la recherche des clés de la totipotence © IGBMC
In vitro, il arrive que des cellules totipotentes apparaissent parmi les cellules pluripotentes ; elles sont qualifiées de « cellules semblables au stade 2 cellules ». Les chercheurs ont donc comparé ces cellules aux cellules de l’embryon précoce afin de trouver leurs caractéristiques communes, différentes des stades pluripotents. Ils ont notamment montré que leur ADN était moins condensé et que l’expression du complexe protéique CAF1 était diminuée dans ces cellules. CAF1, déjà connu pour son rôle dans l’assemblage de la chromatine (état organisé de l’ADN), serait ainsi responsable du maintien de l’état pluripotent en participant à la condensation de l’ADN.
Sur la base de cette hypothèse, les chercheurs sont parvenus à induire un état totipotent en inactivant l’expression de ce complexe, ayant pour effet une reprogrammation de la chromatine dans un état moins condensé
Ces résultats apportent de nouveaux éléments dans la compréhension de la totipotence et laissent entrevoir de prometteuses perspectives en médecine régénérative.