Contact Presse
CHU de Lille
Communication recherche et innovation
Inserm
Visualisation des collagènes constitutifs d’une fibrose cardiaque dans le coeur d’une souris modèle pour l’hypertrophie cardiaque causée provoquée par une sténose aortique. Le collagène I est marqué en vert, le collagène III en rouge. © C Heron et D Godefroy/ Inserm.licence CC-BY-NC 4.0 international.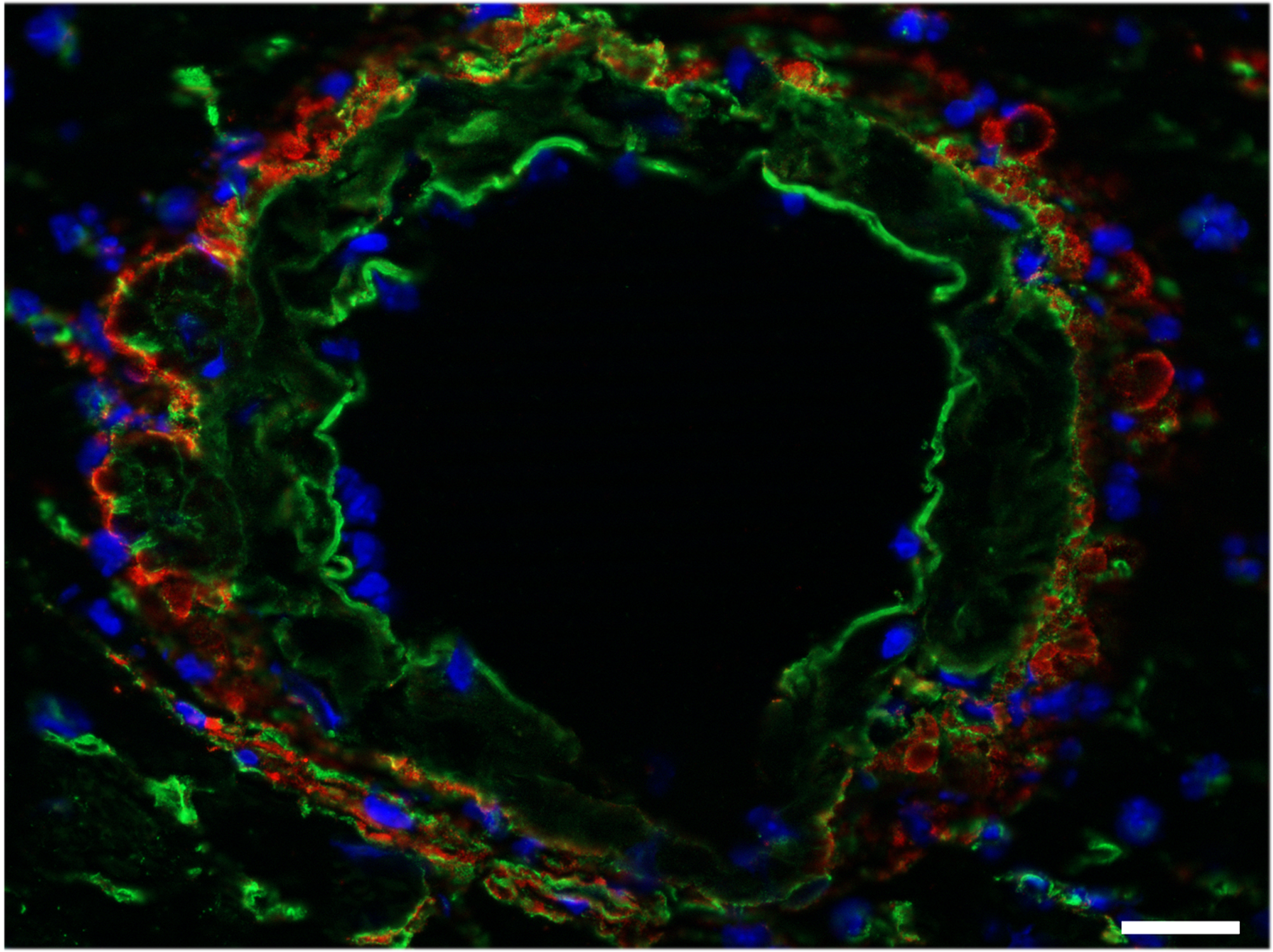
Elle est l’une des pathologies cardiaques les plus fréquentes chez le sujet âgé. En effet, la sténose aortique concerne près de 5 % des adultes de plus de 65 ans. Cette maladie grave, due à une calcification progressive de la valve aortique, demeure à ce jour sans traitement médicamenteux efficace. Une équipe de recherche du CHU de Lille, de l’Inserm, de l’Université de Lille et de Institut Pasteur de Lille, a priorisé ses recherches sur l’identification de médicaments capables de stopper ou de ralentir ce processus de calcification. Les résultats de ces travaux ont été publiés ce 24 février dans la revue Circulation.
« Cette découverte pourrait non seulement améliorer rapidement la prise en charge des patients souffrant de sténose aortique, mais également prolonger la durée de vie des prothèses valvulaires artificielles. » Prs Sophie SUSEN et Eric VAN BELLE, médecins-chercheurs au CHU de Lille.
Le rétrécissement aortique calcifié, appelé également sténose aortique dégénérative, est la maladie des valves cardiaques la plus fréquente dans le monde occidental. Sa fréquence augmente avec l’âge, car les tissus se rigidifient et se calcifient avec le temps. Elle se manifeste par un essoufflement à l’effort, parfois même au repos ; un gonflement des chevilles ou des jambes ; des douleurs thoraciques et parfois même des évanouissements à l’effort. En cas de sténose aortique sévère, le cœur doit travailler beaucoup plus à chaque battement pour pomper la même quantité de sang. Au lieu d’éjecter le sang à travers un orifice de la taille d’une pièce de deux euros, il doit le faire à travers un orifice de la taille d’une pièce de 50 centimes. En l’absence de traitement, le cœur devient plus gros et s’affaiblit progressivement. Cette maladie évolue classiquement vers une défaillance irréversible du cœur avec un risque d’œdème du poumon et de décès précoce. Une fois les symptômes présents, le taux de mortalité sans intervention TAVI (implantation de valve aortique par voie percutanée) ou chirurgicale est de plus de 30% à un an et 50% à deux ans.
La sténose aortique est un problème mécanique. L’orifice par lequel le sang est éjecté étant trop petit, le seul moyen actuel de l’agrandir est de remplacer la valve aortique. C’est dans cette optique que l’avènement des techniques de remplacement percutané a fortement progressé avec l’utilisation des bioprothèses. Toutefois, celles-ci ont tendance à calcifier également 10 à 15 ans après leur implantation, rendant nécessaire une nouvelle intervention, souvent risquée.
L’identification de cibles thérapeutiques permettant de ralentir ou de prévenir ces mécanismes de calcification reste un défi majeur en cardiologie. La communauté scientifique et les sociétés savantes considèrent la découverte de molécules capables de stopper ou ralentir ce processus comme une priorité. En ce sens, l’équipe des Pr Sophie SUSEN et Eric VAN BELLE (Inserm, Université de Lille, CHU de Lille, Institut Pasteur de Lille) a adopté une approche allant du modèle cellulaire au pré-clinique, combinant de multiples analyses permettant l’identification de cibles pharmacologiques innovantes, tout en favorisant le repositionnement de molécules déjà commercialisées.
En collaboration avec l’Hôpital Européen Georges Pompidou et l’European Homograft Bank de Bruxelles, l’équipe lilloise s’est appuyée sur des cohortes de patients suivis au CHU de Lille. Grâce à une approche d’étude de l’expression des gènes de valves calcifiées et non calcifiées, les chercheurs ont mis en évidence la forte réduction de l’expression de l’enzyme ALDH1A1 permettant la synthèse d’un dérivé de la vitamine A dans les valves atteintes de sténose aortique. Cette réduction impactant certaines cellules valvulaires et favorisant le développement d’une nature plus calcifiante.
Grâce à cette mise en évidence, les chercheurs se sont intéressés à l’acide rétinoïque, le principal produit synthétisé par l’enzyme à partir de la vitamine A. Ils ont découvert que celui-ci était efficace in vitro et dans deux modèles animaux précliniques de dégénérescence tissulaire pour contrer la calcification. Ces travaux, publiés ce 24 février dans la revue Circulation, confirment que l’acide rétinoïque protège les cellules valvulaires de toute transformation calcifiante. Déjà commercialisé et utilisé comme traitement pour des indications en oncologie ou dermatologie, l’acide rétinoïque offre une opportunité de disponibilité rapide et sûre pour traiter la sténose aortique et prévenir la dégénérescence des bioprothèses. Ces résultats ouvrent la voie à des essais cliniques, capables d’améliorer la qualité de vie des patients et de prolonger la durée de vie des bioprothèses.
CHU de Lille
Communication recherche et innovation
Inserm
Aortic Valve Calcification Is Induced by the Loss of ALDH1A1 and Can Be Prevented by Agonists of Retinoic Acid Receptor Alpha: Preclinical Evidence for Drug Repositioning
Mickael Rosa, Annabelle Dupont, David M. Smadja, Jérôme Soquet , Johan Abdoul , Thibault Pamart, Flavien Vincent , Christina Le Tanno , Eloise Borowczac, Timothée Bigot, Alexandre Ung, Bertrand Vaast, Mélanie Daniel, Ramadan Jashari, Frédéric Mouquet, Cedric Delhaye, Yoann Sottejeau, Jeanne Rancic, Delphine Corseaux, Francis Juthier , Bart Staels, Sophie Susen, and Eric Van Belle