Contact Chercheur
Etienne Joly
Chercheur Inserm
Institut de pharmacologie et biologie structurale (CNRS/Université Toulouse III – Paul Sabatier)
E-mail : moc.cam@ylojnta
Téléphone portable sur demande
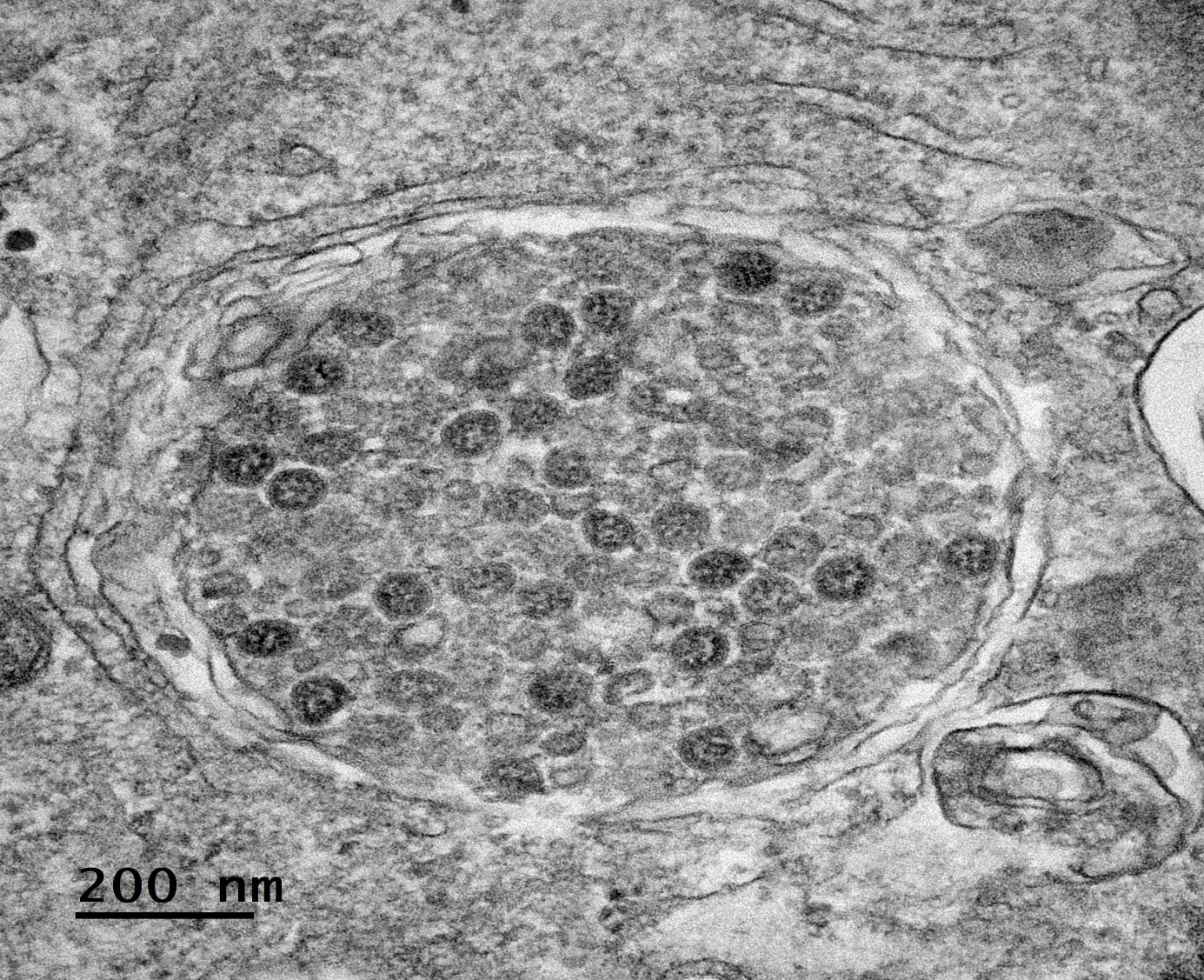
Cellules infectées par le SARS-CoV-2. © Sébastien Eymieux et Philippe Roingeard, Inserm – Université de Tours
Un nouveau test de détection des anticorps anti-Sars-CoV-2, fiable, bon marché et ne requérant aucun matériel spécialisé; c’est ce que propose une équipe scientifique internationale dont un chercheur de l’Inserm à l’Institut de pharmacologie et biologie structurale (CNRS/Université Toulouse III – Paul Sabatier). Ce test sérologique développé en collaboration avec l’université d’Oxford, repose sur un réactif unique qui provoque l’agglutination des globules rouges en présence d’anticorps spécifiques du virus Sars-CoV-2. Dans un premier temps, il pourrait être utilisé dans le cadre de la recherche clinique et épidémiologique. Ce travail est paru dans Nature Communications le 29 mars 2021.
Détecter les anticorps dirigés contre le virus Sars-CoV-2 est essentiel sur le plan épidémiologique pour suivre la progression de l’épidémie. C’est également nécessaire pour les scientifiques qui étudient les liens entre le fait d’avoir été en contact avec le virus et le fait d’être protégé contre une nouvelle infection.
Plusieurs tests sont déjà disponibles et présentent une bonne efficacité mais ils nécessitent des équipements élaborés et couteux, ce qui freine une utilisation à grande échelle, notamment dans les pays disposant de ressources plus limitées.
C’est pourquoi Etienne Joly, chercheur Inserm à l’Institut de pharmacologie et biologie structurale (CNRS/université Toulouse III – Paul Sabatier) a imaginé un nouveau test facile à réaliser et bon marché. En collaboration avec Alain Townsend à l’université d’Oxford au Royaume-Uni, il a développé un test s’appuyant sur l’hémagglutination, une méthode connue depuis plus de 50 ans et couramment utilisée pour la détermination des groupes sanguins.
Le procédé repose sur l’agglomération, détectable à l’œil nu, de globules rouges en présence d’anticorps spécifiques, ici dirigés contre le Sars-CoV-2. Le secret de la simplicité de ce test repose sur l’utilisation d’un seul réactif qui se compose d’une protéine recombinante associant un anticorps reconnaissant une molécule de surface des globules rouges (la glycophorine) au peptide RBD de la protéine Spike du Sars-CoV-2 (le domaine reconnu par les anticorps neutralisants contre le virus). Mis en contact avec du sang, ce réactif se fixe sur les globules rouges.

Le test nécessite deux puits à fonds coniques, dans chacun desquels on dilue 2 microlitres du sang à tester. Les puits de gauche, qui sont les contrôles négatifs, ne contiennent que le milieu de dilution, et les puits de droite contiennent en plus le réactif IH4-RBD. Après une heure d’incubation les globules rouges ont sédimenté et forment un bouton rouge au fond de tous les puits. La plaque est alors penchée à 80° pendant 30 secondes, et les globules rouges non hémagglutinés forment une larme, comme on peut le voir dans tous les puits de gauche. La présence d’anticorps dans l’échantillon testé sur la deuxième ligne est révélée par les globules rouges agglutinés par le réactif qui restent « en bouton » au fond du puit. © Etienne Joly
Si dans ce même échantillon de sang, les anticorps anti-Sars-CoV-2 sont présents, ils reconnaissent alors le fragment RBD du réactif présent à la surface des globules rouges. Ces anticorps se fixent simultanément sur des fragments RBD pouvant être sur deux globules rouges différents, ce qui relie ces derniers entre eux, aboutissant à la formation d’un amas. Cette agglomération révèle donc une infection récente ou passée.
90 % de sensibilité
Le test a été évalué sur plus de 400 sérums de patients pris en charge dans différents hôpitaux au Royaume-Uni et a présenté une sensibilité de 90 %. Cela signifie que sur 100 personnes ayant des anticorps, le test n’en détectera que chez 90 d’entre elles. Etienne Joly travaille actuellement à améliorer cette sensibilité car elle est un peu inférieure à celle des tests ELISA couramment utilisés par les laboratoires de diagnostic, néanmoins elle est déjà meilleure que celle des TROD COVID (test rapide d’orientation diagnostique) disponibles en pharmacie pour une dizaine d’euros. La spécificité de ce test est quant à elle très bonne : elle atteint 99 %. Sur 100 personnes n’ayant pas d’anticorps, le test sera faussement positif pour une seule d’entre elles.
Etienne Joly
Chercheur Inserm
Institut de pharmacologie et biologie structurale (CNRS/Université Toulouse III – Paul Sabatier)
E-mail : moc.cam@ylojnta
Téléphone portable sur demande
A haemagglutination test for rapid detection of antibodies to SARS-CoV-2
Townsend et al.
Nature Communications, mars 2021