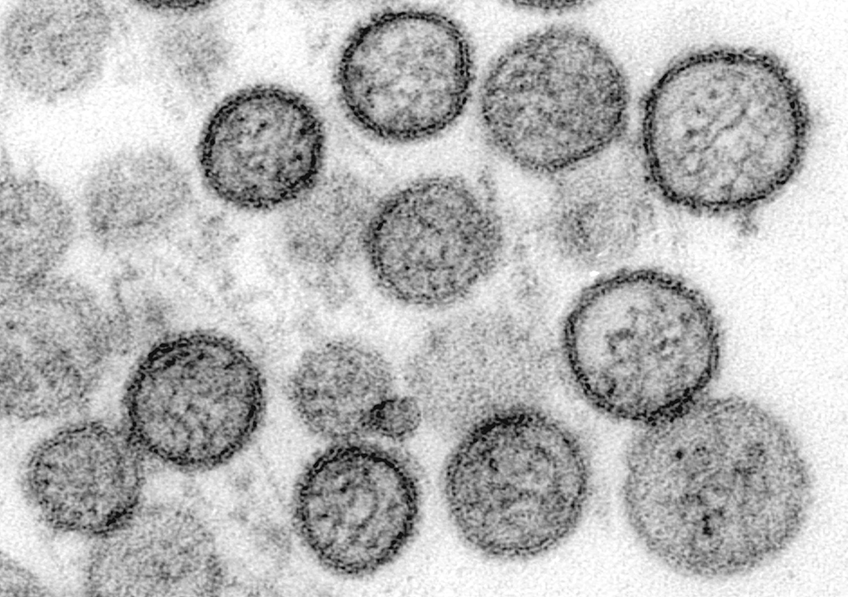
 Micrographie électronique à transmission du virus Sin Nombre. Hantavirus. © CDC/ Cynthia Goldsmith, Luanne Elliott
Micrographie électronique à transmission du virus Sin Nombre. Hantavirus. © CDC/ Cynthia Goldsmith, Luanne Elliott
Le 3 mai 2026, l’Organisation mondiale de la santé (OMS) a signalé un possible foyer d’infection à hantavirus à bord du navire de croisière MV « Hondius », parti d’Argentine à destination du Cap-Vert et transportant 147 passagers et membres d’équipage.
Que sait-on aujourd’hui de ce virus, dont l’OMS juge le risque de propagation hors du navire faible ? Quels sont les symptômes de l’infection, et où en est la recherche pour mieux la prévenir et la traiter ?
Un décryptage proposé par l’Inserm et l’ANRS MIE, agence de l’Inserm dédiée aux maladies infectieuses émergentes.
Qu’est-ce que l’hantavirus ?
Les hantavirus forment une grande famille de virus présents sur tous les continents. Ils circulent principalement chez les rongeurs sauvages, notamment les campagnols, mais aussi plus rarement chez d’autres animaux comme certaines chauves-souris, reptiles ou poissons.
Chaque hantavirus est généralement associé à une espèce animale précise. Chez ces hôtes naturels, l’infection est le plus souvent asymptomatique, mais ils peuvent transmettre le virus à l’être humain.
Ces virus ont été identifiés la première fois dans les années 1950, lors d’une épidémie survenue pendant la guerre de Corée. Plus de 3 000 soldats avaient alors développé des symptômes comme un syndrome grippal voire des hémorragies. Le nom « hantavirus » vient d’ailleurs d’une rivière coréenne, la rivière Hantaan.
Pourquoi l’OMS a-t-elle sonné l’alerte ?
Le 3 mai 2026, l’OMS a alerté sur un possible foyer d’infection à hantavirus à bord du navire de croisière MV « Hondius », parti d’Argentine vers le Cap-Vert, et transportant 147 passagers et membres d’équipage.
À ce jour, deux cas d’infection ont été confirmés en laboratoire et cinq autres sont suspectés. Sur les sept personnes malades, trois sont décédées et une se trouve actuellement en soins intensifs en Afrique du Sud. Le premier décès est survenu chez un homme de 70 ans qui a été le premier à présenter des symptômes grippaux. Son épouse de 69 ans est également tombée malade à bord du navire et a été évacuée vers l’Afrique du Sud où elle est décédée à hôpital de Johannesburg.
Le séquençage du virus, c’est-à-dire l’analyse de son code génétique, a pu être réalisé, en parallèle d’enquêtes épidémiologiques. Ces investigations, qui consistent à définir quelle est la souche exacte qui circule (a priori la souche des Andes, d’après le ministre de la Santé sud-africain), ont pour objectif de retracer précisément les contacts, les déplacements et les circonstances d’exposition des personnes malades, afin de comprendre comment le virus s’est propagé et transmis entre les passagers.
Dans ce contexte, le navire n’a pas été autorisé à accoster, et les passagers comme les membres d’équipage font l’objet d’une prise en charge médicale adaptée.
À ce stade, le risque d’une propagation hors du navire est considéré comme faible par l’OMS[i].
Comment le virus se transmet-il ?
Les hantavirus se transmettent le plus souvent aux humains par voie indirecte, en inhalant des poussières contaminées par les excréments et urines de rongeurs infectés. Plus rarement, la contamination peut avoir lieu à la suite d’un contact direct ou d’une morsure.
Les personnes les plus exposées sont celles qui travaillent dans les champs ou dans les forêts, dans des zones à risque, en manipulant du bois, en nettoyant des locaux poussiéreux…
Il est rare qu’un hantavirus se transmette d’un être humain à un autre. Cela a été été observé pour la première fois en 1996 dans le sud de l’Argentine, et ne semble concerner que le virus des Andes, présent de façon stable dans ce pays, sans avoir pour autant provoqué une flambée de cas. D’après les dernières informations recueillies sur le séquençage du virus, c’est bien cette souche des Andes qui circulerait à bord du navire. Il s’agit de la seule souche, parmi les 38 connues, à pouvoir se transmettre d’une personne à l’autre bien que ce mode de transmission reste marginal par rapport à l’exposition indirecte aux rongeurs infectés.
La période où le virus se transmet le plus facilement correspond au tout début de la maladie, lors de la phase dite prodromique, lorsque les premiers symptômes apparaissent mais que la personne n’est généralement pas encore hospitalisée. Dans cette phase, ce sont surtout les proches qui sont exposés, en particulier lors de contacts étroits, notamment les relations sexuelles, ou dans des espaces confinés.
Quels sont les symptômes ?
Chez les humains, les hantavirus peuvent être responsables d’infections de gravité très variable, parfois mortelles. Après une phase d’incubation pouvant aller de une à six semaines (en moyenne deux), les premiers symptômes (fièvre, maux de tête, douleurs musculaires), évoquent le plus souvent ceux d’une grippe. Les personnes contaminées peuvent également développer une toux et avoir une respiration plus difficile, entre un et cinq jours après le début des symptômes.
On distingue principalement deux formes de la maladie. La première, la forme hémorragique avec atteinte rénale, est surtout observée en Europe et en Asie. Elle évolue en plusieurs phases et s’accompagne d’une mortalité relativement faible, comprise entre 0,4 et 10 %.
La seconde est une forme cardio-pulmonaire, plus brutale, marquée par une défaillance respiratoire et cardiaque, et associée à une mortalité plus élevée, de l’ordre de 30 à 60 %. Elle est principalement décrite sur le continent américain.
Dans les deux cas, les symptômes s’expliquent par une atteinte des vaisseaux sanguins, qui deviennent anormalement perméables. Cela entraîne une fuite de liquide vers les tissus.
Comment se pose le diagnostic ?
En cas de suspicion d’une infection à hantavirus, les patients sont d’abord interrogés concernant leurs symptômes, et la possibilité qu’ils aient été récemment exposés à des rongeurs. Le diagnostic est ensuite confirmé grâce à des analyses biologiques. Les tests les plus utilisés sont la PCR et les tests sérologiques, qui recherchent dans le sang la présence d’anticorps produits par l’organisme en réponse au virus.
Comment se protéger des hantavirus ?
À ce jour, il n’existe pas de traitement spécifique ni de vaccin validés contre les hantavirus. La prise en charge repose donc essentiellement sur l’apaisement des symptômes. Dans les formes les plus sévères, les patients doivent être hospitalisés, souvent en unité de soins intensifs, avec une surveillance étroite et, si nécessaire, une aide respiratoire (oxygénothérapie, voire ventilation).
En l’absence de traitement spécifique, la stratégie la plus efficace pour se protéger des hantavirus repose sur la prévention. Elle consiste avant tout à réduire le risque d’exposition aux rongeurs et à leurs excrétions, notamment dans les environnements à risque.
Où en est la recherche ?
Les vaccins contre les hantavirus font l’objet de nombreuses recherches, avec des approches variées visant à améliorer leur efficacité et leur sécurité. Toutefois, malgré ces avancées, aucun vaccin n’est encore approuvé, en raison de défis persistants liés à l’efficacité, à la durée de protection, aux modalités d’administration pouvant améliorer fortement l’immunogénicité, et à la production à grande échelle.
Parmi les approches déjà testées, les vaccins inactivés, comme Hantavax® développé en Corée du Sud, ont montré une réduction de l’incidence des infections. Cependant, leur efficacité diminue avec le temps, ce qui nécessite des rappels réguliers, et ils ne protègent pas contre tous les types d’hantavirus. Des essais cliniques ont notamment montré une bonne réponse immunitaire juste après vaccination, mais une baisse significative des anticorps quelques mois plus tard[ii].
Plusieurs autres stratégies vaccinales sont actuellement à l’étude : des vaccins recombinants, utilisant des vecteurs viraux comme le virus de la stomatite vésiculaire (VSV)[iii], qui déclenchent des réponses immunitaires fortes chez l’animal ; et des vaccins à ADN, capables d’induire une réponse contre plusieurs types d’hantavirus à la fois[iv]. Ces stratégies montrent des résultats encourageants, notamment en ce qui concerne la production d’anticorps neutralisants, mais elles doivent encore être confirmées chez l’humain à grande échelle.
En parallèle des vaccins, plusieurs approches thérapeutiques sont explorées pour traiter l’infection. Parmi les principaux candidats, la ribavine, un médicament antiviral, pourrait avoir un intérêt si elle est administrée très tôt, notamment dans les formes avec atteinte rénale[v]. Mais les résultats restent contrastés, et certains essais n’ont pas montré d’effet significatif sur la charge virale[vi].
Une autre molécule, le favipiravir, a montré des résultats encourageants en laboratoire et chez les hamsters[vii], avec une réduction de la charge virale et une amélioration des chances de survie.
D’autres stratégies thérapeutiques cherchent soit à empêcher le virus de pénétrer dans les cellules, soit à renforcer la réponse immunitaire de l’organisme. Par exemple, la lactoferrine, une protéine testée chez l’animal, semble avoir un effet protecteur lorsqu’elle est administrée précocement[viii].
D’autres approches reposent sur les ARN interférents (siARN), qui visent à bloquer directement l’expression des gènes du virus. Cependant, ces stratégies restent encore expérimentales, notamment en raison de difficultés à stabiliser ces molécules dans l’organisme et à les acheminer vers les cellules ciblées[ix].
Enfin, l’immunothérapie est une piste prometteuse. Elle repose notamment sur l’utilisation de plasma provenant de patients guéris, qui a été bien toléré chez l’humain lors d’un essai non randomisé[x]. Par ailleurs, des anticorps monoclonaux, comme MIB22 et JL16, obtenus à partir de sérums de convalescents, ont montré une efficacité protectrice chez le hamster contre l’infection par un hantavirus[xi].
Quels sont les principaux défis pour les scientifiques qui tentent de mettre au point des traitements ?
En l’attente d’un vaccin, une priorité est de limiter la réaction inflammatoire excessive déclenchée par l’infection. Celle-ci contribue fortement aux formes graves, en particulier via des atteintes des vaisseaux sanguins. Les recherches se concentrent notamment sur les cytokines et chimiokines, impliquées dans ce phénomène.
Parallèlement, l’effort de recherche devra accélérer la mise au point de vaccins et d’approches combinées associant antiviraux et immunothérapies. L’objectif est de disposer de traitements capables d’agir rapidement sur le virus et d’assurer une protection plus durable.
Enfin, les modèles animaux actuels reproduisent imparfaitement la maladie humaine. Leur amélioration est essentielle pour mieux tester les traitements et comprendre les mécanismes de l’infection.
Quels sont les programmes de recherche dans lesquels est engagée l’ANRS MIE, agence de l’Inserm dédiée à la lutte contre les maladies infectieuses émergentes ?
L’ANRS MIE, agence de l’Inserm dédiée aux maladies infectieuses émergentes, soutient, anime et coordonne la recherche sur les hantavirus.
Dans ce cadre, elle a financé un projet via son appel à projets Émergence PRFI 2025, avec le projet en cours TRANSVI, qui étudie les chaînes de transmission des hantavirus entre faune sauvage et humains dans la péninsule du Yucatán (Mexique).
En 2025, un des prix de thèse Virus émergents, décerné par l’ANRS MIE et la Société française de virologie (SFV), a été attribué à Quentin Durieux Trouilleton pour des travaux intitulés Analyse structurale et fonctionnelle de la réplication et de la transcription des Bunyavirus, portant notamment sur deux hantavirus et ayant permis d’observer pour la première fois la polymérase d’un hantavirus.
L’ANRS MIE participe également au réseau de l’OMS des Collaborative Open Research Consortium (CORC), en lien avec l’UKHSA, qui pilote le CORC Bunyavirales consacré à la préparation aux épidémies à hantavirus.
Enfin, les hantavirus sont abordés dans plusieurs actions coordonnées, notamment Fièvres hémorragiques virales, Interactions hôte-virus et Transmission interhumaine des virus respiratoires.
Cet article a été écrit avec le soutien et relu par Nathan Claveau et Vincent Ronin et l’équipe du pôle Crises de l’ANRS MIE, agence autonome de l’Inserm
[i] HANTAVIRUS CASES | UNifeed. https://media.un.org/unifeed/en/asset/d356/d3565401
[ii] Immunogenicity and safety of a modified three-dose priming and booster schedule for the Hantaan virus vaccine (Hantavax): A multi-center phase III clinical trial in healthy adults – PubMed. https://pubmed.ncbi.nlm.nih.gov/33131933/
[iii] Single dose recombinant VSV based vaccine elicits robust and durable neutralizing antibody against Hantaan virus | npj Vaccines. https://www.nature.com/articles/s41541-024-00814-2
[iv]ClinicalTrials.gov.
https://clinicaltrials.gov/study/NCT02116205?cond=hantavirus&viewType=Card&sort=StudyFirstPostDate&page=2&rank=14
[v] Prospective, double-blind, concurrent, placebo-controlled clinical trial of intravenous ribavirin therapy of hemorrhagic fever with renal syndrome – PubMed. https://pubmed.ncbi.nlm.nih.gov/1683355/
[vi] Insufficient efficacy and safety of intravenous ribavirin in treatment of haemorrhagic fever with renal syndrome caused by Puumala virus – PubMed. https://pubmed.ncbi.nlm.nih.gov/28276794/
[vii] Antiviral efficacy of favipiravir against two prominent etiological agents of hantavirus pulmonary syndrome – PubMed. https://pubmed.ncbi.nlm.nih.gov/23856782/
[viii] Characterization of in vitro and in vivo antiviral activity of lactoferrin and ribavirin upon hantavirus – PubMed. https://pubmed.ncbi.nlm.nih.gov/11459009/
[ix] eIF4E Signaling Pathway – PubMed. https://pubmed.ncbi.nlm.nih.gov/35847100/
[x] A non-randomized multicenter trial of human immune plasma for treatment of hantavirus cardiopulmonary syndrome caused by Andes virus – PubMed. https://pubmed.ncbi.nlm.nih.gov/25316807/
[xi] Two recombinant human monoclonal antibodies that protect against lethal Andes hantavirus infection in vivo – PubMed. https://pubmed.ncbi.nlm.nih.gov/30463919/