L’exposition prolongée au monoxyde de carbone (CO), dans des conditions mimant la pollution citadine, conduit chez le rat sain à des modifications de la morphologie et de la fonction cardiaque. Chez ces animaux, des mécanismes compensateurs sont mis en place pour maintenir une activité cardiaque normale. Cependant, ils seront plus vulnérables aux pathologies cardiaques. Ces résultats, publiés le 15 mars 2010 dans la revue American Journal of Respiratory and Critical Care Medicine par des chercheurs du CNRS et de l’Inserm, apportent les preuves cellulaires, chez le rat, d’un effet direct de la pollution urbaine sur la fonction cardiaque. Des travaux sont en cours pour vérifier ces données chez l’Homme.
Les études épidémiologiques relient la pollution atmosphérique au monoxyde de carbone (CO) de type urbain à des accidents cardiovasculaires et un risque accru de mortalité cardiaque, notamment chez des sujets fragilisés par une pathologie sous-jacente. Cependant, chez les sujets sains, les effets du CO sont mal cernés et les mécanismes cellulaires peu étudiés.
Des chercheurs CNRS au laboratoire UMR-637 (Inserm/Université Montpellier 1 & 2) ont, en collaboration avec des chercheurs de l’Université d’Avignon, exposé des rats sains pendant 4 semaines à de l’air pur ou à de l’air enrichi en CO(1) à un niveau reproduisant des conditions de pollution urbaine. L’objectif de cette étude : évaluer les effets d’une pollution chronique au CO sur la fonction cardiaque dans un modèle expérimental sain, à la fois in vivo, par des échocardiographies et des électrocardiogrammes (ECG), et in vitro, par la mesure de différents paramètres sur des cardiomyocytes (cellules cardiaques).
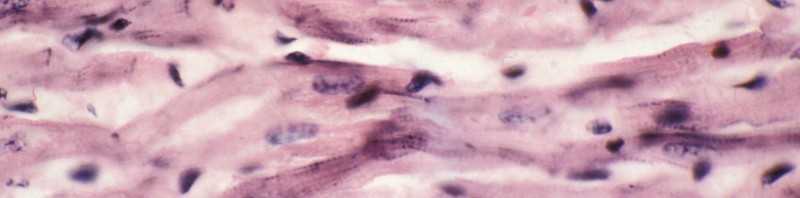
© Inserm Fibres myocardiques, tissu musculaire du coeur. Le myocarde est composé de cellules musculaires cardiaques spécialisées, les cardiomyocytes
Les résultats montrent que la pollution chronique au CO entraîne des changements de la morphologie et de la fonction cardiaque. Chez les rats du groupe CO, on observe en effet des différences au niveau du ventricule gauche(2), ainsi que des signes de stress et de remodelage cardiaque localisés. Au niveau cellulaire, les cardiomyocytes présentent des défauts de contractilité et des troubles du rythme. Un état « hyperadrénergique » modéré, révélateur d’un état de stress et connu pour son implication dans le développement de l’hypertrophie cardiaque et de la fibrose, de tachycardies, et de risques de mort subite cardiaque, est également observé. Enfin, un dysfonctionnement des échanges calciques dans les cardiomyocytes est également mis en évidence, pouvant déclencher des extrasystoles et des tachycardies ventriculaires à risque de mort subite.
Chez le rat sain, l’exposition chronique au CO conduit donc à des altérations cellulaires observées classiquement dans l’insuffisance cardiaque. Le phénotype in vivo, moins sévère, suggère que des mécanismes compensateurs se mettent en place. « Annulant » les effets du CO, ils permettent au myocarde de fonctionner normalement. Mais ils placent les cellules cardiaques dans un état de stress chronique. Et si un stress additionnel survient, comme un infarctus du myocarde, les conséquences seront plus lourdes pour le coeur. Les deux mêmes équipes (Avignon et Montpellier) viennent également de montrer que l’exposition chronique au CO augmente de manière très significative les dommages cardiaques induits par un infarctus du myocarde.
Au niveau du diagnostic, si ces résultats sont potentiellement extrapolables à l’Homme, cette étude montre que les effets néfastes de la pollution au CO seraient difficiles à détecter par des investigations cliniques de routine comme l’échocardiographie ou les enregistrements ECG courts, car ils sont surtout observés dans des conditions de stress et au niveau cellulaire. Des résultats préliminaires semblent néanmoins montrer que chez l’Homme sain, après un test d’effort, il existe une corrélation entre le taux de carboxy-hémoglobine dans le sang, représentatif du CO atmosphérique analysable par une simple prise de sang, et la survenue d’évènements arythmiques.
Les recherches en cours visent à voir dans quelles conditions et après quelle durée d’exposition, les effets observés au niveau cellulaire entraînent des effets pathologiques in vivo plus sévères chez l’animal, puis chez l’Homme.
(1) Groupe contrôle exposé à de l’Air pur ou sain : CO (2) Augmentation du rapport ventricule gauche (VG)/poids du corps, augmentation de la fibrose interstitielle et fibrose périvasculaire au niveau du VG.