Déduire de simples biopsies du côlon, la présence et l’importance des lésions dans le cerveau de patients atteints de la maladie de Parkinson est le dernier résultat surprenant des recherches menées par des équipes de l’Inserm à Nantes. Pascal Derkinderen, Michel Neunlist, Stanislas Bruley des Varannes et leurs collaborateurs de l’Unité Inserm 913 « neuropathies du système nerveux entérique et pathologies digestives : implication des cellules gliales entériques « , du centre d’investigation clinique et du CHU de Nantes » ont mis en évidence que des anomalies bien connues dans les neurones des malades sont retrouvées à l’identique dans les neurones digestifs. De plus, l’importance des lésions observées était corrélée à la sévérité de la maladie. Ces travaux sont publiés aujourd’hui dans la revue Plos One.
La maladie de Parkinson est depuis longtemps identifiée comme une maladie neurodégénérative du système nerveux central, à l’origine des signes moteurs de la maladie (rigidité musculaire et difficultés à effectuer les gestes alternatifs rapides). Toutefois, il est désormais clairement établi que les lésions de la maladie de Parkinson ne se limitent pas au système nerveux central mais qu’elles touchent aussi des systèmes nerveux périphériques.
Cette avancée récente a permis de résoudre un problème pratique majeur dans l’étude de la maladie de Parkinson : étudier les lésions sur des patients vivants. Effectivement, alors que l’accès au système nerveux central n’est possible qu’après le décès des malades, les systèmes nerveux périphériques et notamment le système entérique (cf encadré) présentent l’avantage de pouvoir être étudiés in vivo.
Les chercheurs ont donc analysé de simples biopsies du colon obtenues en routine chez 39 patients (29 atteints de la maladie de Parkinson et 10 témoins). Forts de leur expérience dans la connaissance du système nerveux entérique, ils ont réussi à quantifier et qualifier les neurones digestifs issus des biopsies.
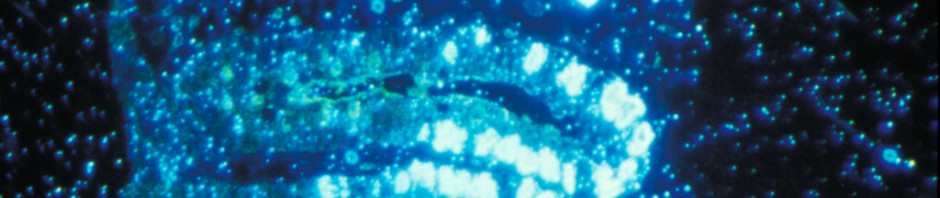
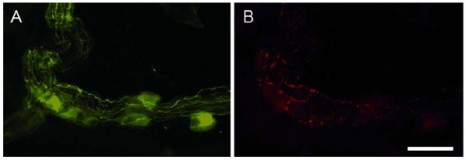
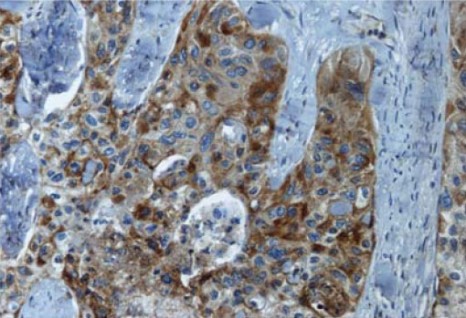
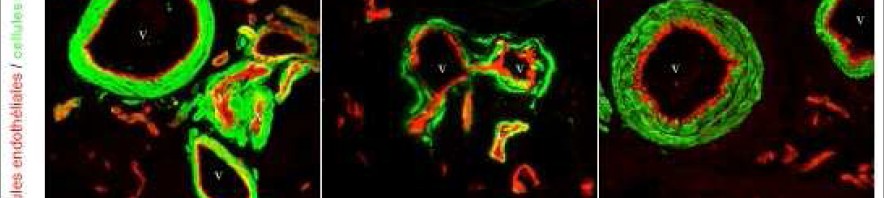
Immunomarquage du plexus sous-muqueux prélevé à partir de biopsies coliques. A. marquage permettant le comptage du nombre de neurones et l’identification des prolongements B : identification des inclusions pathologiques (neurites de Lewy) dans certains prolongements identifiés par le marquage des neurofilaments. Echelle 30 µM. © Inserm U913, P. Derkinderen
Chez 21 des 29 patients parkinsoniens, les chercheurs de l’Inserm ont mis en évidence des anomalies des neurones digestifs identiques aux anomalies présentes dans le système nerveux central (les neurites de Lewy1) (Figure). Ils ont également pu établir un parallèle entre les lésions et les signes cliniques : l’importance des lésions étant corrélée à la sévérité de la maladie de Parkinson.
Les résultats de cette étude montrent pour la première fois que l’analyse du système nerveux entérique est une vraie « fenêtre ouverte » sur le système nerveux central. Par ailleurs, le lien observé entre les lésions et les signes cliniques représente un marqueur de sévérité intéressant pour la maladie de Parkinson. « L’avancement de la maladie pourrait ainsi être déterminé à partir de l’analyse de simples biopsies coliques effectuées à l’hôpital lors de coloscopies ou de recto-sigmoidoscopies » explique Pascal Derkinderen. « Si nos résultats se confirment à grande échelle, il serait possible de faire un diagnostic de sévérité de la maladie de Parkinson du vivant du patient et d’ajuster le traitement et la prise en charge » concluent les chercheurs.
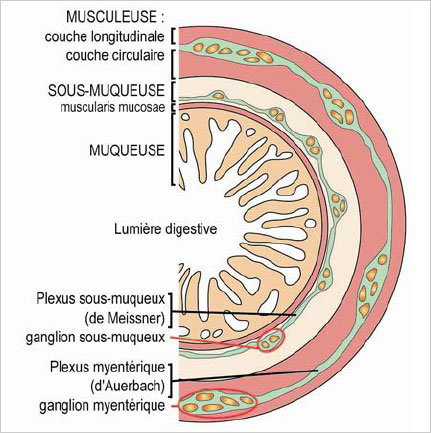
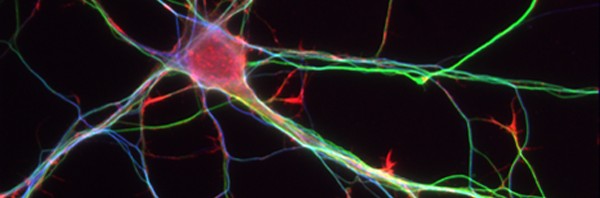
Coupe transversale de tube digestif permettant de voir le système nerveux entérique, organisé en un réseau neuronal, composé d’un plexus sous-muqueux et d’un plexus myentérique. Les biopsies coliques obtenues par endoscopie permettent d’analyser le plexus sous-muqueux. © Inserm U913, P. Derkinderen
Coupe transversale de tube digestif permettant de voir le système nerveux entérique, organisé en un réseau neuronal, composé d’un plexus sous-muqueux et d’un plexus myentérique. Les biopsies coliques obtenues par endoscopie permettent d’analyser le plexus sous-muqueux. © Inserm U913, P. Derkinderen