Chez la souris, pendant la fécondation, un mécanisme physiologique permet le ciblage et l’élimination d’une sous-population anormale de spermatozoïdes. Ce mécanisme, mis en place par les spermatozoïdes eux-mêmes, augmente les chances de fécondation et diminue le risque de fécondation avec un spermatozoïde défectueux. Ces résultats sont publiés le 26 avril 2010 dans la revue Journal of Clinical Investigation par des chercheurs du CNRS et de l’Inserm, appartenant à l’Institut des neurosciences de Grenoble, en collaboration avec des chercheurs japonais. Transposés à l’homme, ils permettraient de mieux sélectionner les spermatozoïdes pour les techniques de procréation médicalement assistée (PMA) et d’augmenter ainsi les chances d’avoir un enfant pour les couples infertiles.
Environ 15 % des couples présentent des problèmes d’infertilité, dont la moitié est due à des déficiences de l’homme. Au cours des trente dernières années, différentes techniques ont été mises au point pour répondre aux besoins des couples infertiles et aujourd’hui, dans les pays industrialisés, près de 2% des enfants naissent grâce à la procréation médicalement assistée (PMA). Malgré ces progrès indéniables, de nombreux couples infertiles ne parviennent pas à avoir d’enfant. De plus, le risque de mettre au monde un enfant ayant une maladie génétique rare, quoique très faible, est sensiblement supérieur chez les enfants nés grâce aux techniques de PMA(1) . Plusieurs causes ont été évoquées dont un risque plus élevé de sélection défectueuse du spermatozoïde dans les techniques de PMA par rapport aux processus de sélection naturels. Dans ce contexte, le choix des gamètes utilisés revêt une importance toute particulière : sur quels critères doivent-ils être sélectionnés ?
Les équipes de Christophe Arnoult, chercheur CNRS au sein de l’institut des neurosciences de Grenoble (Unité Inserm 836, Université Joseph Fourier, Grenoble), Gérard Lambeau, chercheur CNRS à l’Institut de pharmacologie moléculaire et cellulaire (CNRS/Université de Nice) et l’équipe de Makoto Murakami (The Tokyo Metropolitan Institute of Medical Science, Japon) viennent de montrer, chez la souris, l’existence d’un mécanisme physiologique qui permet de cibler et d’éliminer une sous-population de spermatozoïdes présentant des anomalies sur les lipides composant leur membrane plasmique.
En effet, après leur entrée dans les voies génitales femelles, certains spermatozoïdes vont relâcher au cours de leur maturation une enzyme, appelée phospholipase A2 sécrétée de groupe X. Cette dernière détruit l’acrosome(2) des spermatozoïdes défectueux, ce qui les rend incapables de fusionner avec l’ovocyte. Ils sont ainsi rendus infertiles et écartés de la « course à la fécondation ».
Les chercheurs ont réalisé des expériences qui montrent que l’absence de phospholipase A2 sécrétée de groupe X (animaux modifiés génétiquement ou inhibition par des antagonistes spécifiques) diminue le taux de fécondation et altère le développement embryonnaire. Inversement, si l’on ajoute une forte concentration d’enzyme synthétique à une population de spermatozoïdes, on observe une augmentation du taux de fécondation de 30% dans un modèle animal très fertile (des souris normales), et de 100% dans un modèle animal peu fertile (des souris consanguines chez lesquelles le taux de reproduction est très faible). L’enzyme permet donc bien d’éliminer une grande partie des spermatozoïdes défectueux.
Ces travaux révèlent le « travail coopératif » des spermatozoïdes qui se trient mutuellement pour diminuer les spermatozoïdes défectueux lors de la fécondation. Ils mettent également en évidence l’importance des lipides membranaires du spermatozoïde dans les mécanismes de maturation des spermatozoïdes et de fécondation.
Les chercheurs vont désormais étudier l’efficacité et l’innocuité d’un traitement des spermatozoïdes par la phospholipase A2 sécrétée de groupe X dans un modèle primate. Les applications concernant l’utilisation de ce type de molécules (phospholipase A2) dans le cadre des techniques de procréation assistée et de la contraception ont été brevetées.
Si leurs travaux sont validés, cette découverte pourrait ensuite permettre, chez l’Homme, d’améliorer les techniques de procréation médicalement assistée (PMA). La qualité des lipides membranaires des spermatozoïdes pourrait en effet être un nouveau critère retenu par les praticiens qui sélectionnent les spermatozoïdes pour ces techniques. Ils pourraient ainsi augmenter leur efficacité, et donc les chances de succès, et permettre de diminuer les risques d’anomalies chez les enfants nés grâce à la PMA.
© Christophe Arnoult
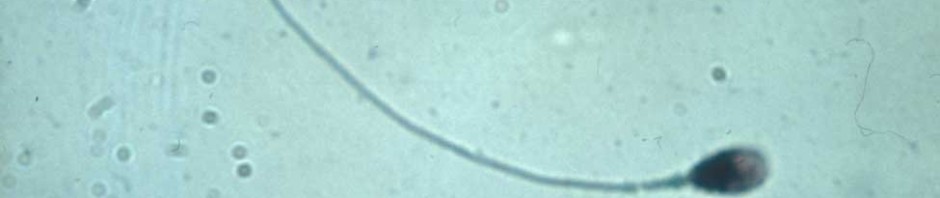
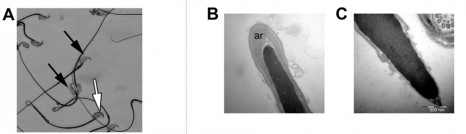
Figure A : spermatozoïdes murins traités avec la phospholipase A2 sécrétée de groupe X en microscopie optique. Flèche blanche : acrosome intact, flèche noire : les spermatozoïdes ont perdu leur acrosome et sont devenus infertiles.
Figure B : partie apicale de la tête d’un spermatozoïde, contrôle en microscopie électronique. L’acrosome (ar) est intact.
Figure C : Partie apicale de la tête d’un spermatozoïde traité avec la phospholipase A2 sécrétée de groupe X. L’acrosome a disparu.
(1) Palermo et al, 2008, Genetic and epigenetic characteristics of ICSI children, Reproductive BioMedicine Online, 17,820-833; Alukal J and Lamb D, 2008, Intracytoplasmic Sperm Injection (ICSI) – What are the risks?, 35(2): 277–288)
(2) L’acrosome est le capuchon qui entoure la tête du spermatozoïde. Au cours de la fécondation, la fusion de la membrane de l’acrosome et de la membrane plasmique du spermatozoïde entraîne la libération d’enzymes qui permettent la fusion avec la membrane de l’ovocyte.