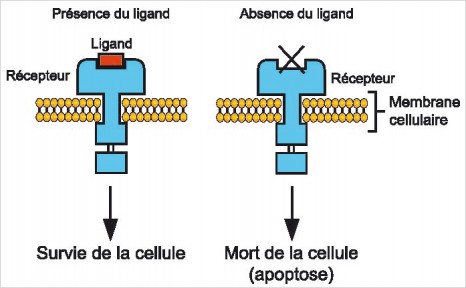
Dix-sept projets français sélectionnés par un jury international vont être financés à hauteur de 2,6 m€ dans le cadre du plan Cancer 2009-2013.
Bien que le diagnostic et la thérapeutique des cancers aient fortement évolué ces dernières décennies, d’immenses progrès sont encore indispensables afin d’améliorer leur diagnostic précoce et leur traitement. Le développement de nouveaux outils est donc au coeur des orientations stratégiques inscrites dans le Plan Cancer 2009-2013.
C’est dans cette optique qu’a été lancé, dans le cadre du volet Recherche du plan Cancer 2009-2013 l’appel à projets de recherche « Physique, mathématiques, Sciences de l’ingénieur appliquées au Cancer », organisé conjointement par les ITMOs Cancer et Technologies pour la santé d’Aviesan (Alliance nationale pour les sciences de la vie et de la santé), avec la collaboration de l’INCa, et dont la gestion opérationnelle et financière a été confiée à l’Inserm.
L’objectif général de cet appel à projets était d’attirer dans le champ de la recherche sur le cancer, des chercheurs physiciens, mathématiciens et des ingénieurs. Une première en France.
Dix-sept projets viennent d’être sélectionnés par un comité d’évaluation international mis en place par l’Inserm. Il s’agit de projets fondés sur la physique, les sciences de l’ingénieur ou les mathématiques et susceptibles d’améliorer le diagnostic ou la prise en charge thérapeutiques du cancer.
Pour M. Jean BARTHE, vice-président du comité d’évaluation, et Conseiller Scientifique du Laboratoire National Henri Becquerel, CEA, Gif-sur-Yvette, « les 17 projets retenus-sur les 64 proposés- ont été financés pour un budget global plus élevé que prévu initialement montrant l’intérêt porté par Aviesan à la collaboration synergique entre physiciens, mathématiciens, biologistes et radio-biologistes dans la recherche de nouvelles connaissances et de nouveaux concepts de mesure tant matériels que logiciels pour la lutte contre le cancer. » Fort du succès rencontré par cet appel d’offres, cet appel à projets sera renouvelé en 2012 et 2013, selon les objectifs du plan cancer annonce Fabien Calvo, Directeur de l’Institut Cancer d’Aviesan.
Liste des projets sélectionnés
François AMBLARD
Titre du projet : Imagerie thermique impulsionnelle du mélanome
Laboratoire de Physico-Chimie Curie-UMR 168, Paris
Manuel BARDIES
Titre du projet : DosiTest : Intercomparaison des approches de dosimétrie clinique en radiothérapie moléculaire par simulation Monte-Carlo
Centre de Recherche sur le Cancer de Toulouse – UMR 1037, Toulouse
Claude BOCCARA
Titre du projet : Tomographie optique et elastique des tumeurs pour le diagnostic peroperatoire
Institut Langevin-ESPCI ParisTech – Paris
Joseph CICCOLINI
Titre du projet : Modelisation biomathematique des processus metastatiques : étude expérimentale chez l’animal porteur de tumeur
Laboratoire de Pharmacocinétique – UMR MD3, Marseille
Nicolas FORAY
Titre du projet : MICROMEGAS: Liens (Relations?) mathématiques entre les événements radioinduits précoces : MICROdépôts, chroMatinE siGnAliSation
Centre de Recherche en Cancérologie de Lyon – U1052, Lyon
Paul FORCE
Titre du projet : Contrôle qualité du traitement et de la dose délivrée en temps réel pour l’hadrontherapie par la mesure en ligne de l’activité de radioélément émetteur de positron
Laboratoire de Physique Corpusculaire de Clermont – UMR 6533, Aubière
Jean-Yves GIRAUD
Titre du projet : Amélioration de la dosimétrie clinique en curiethérapie de prostate par implantation permanente de grains d’iode 125, grâce à un calcul Monte Carlo prenant en compte l’orientation 3D des sources radioactives
Institut de Neurosciences – Université Joseph Fourier Grenoble 1, Grenoble
Julien HENRIET
Titre du projet : Construction d’un fantôme thoracique dynamique (respirant) 3D personnalisé (« THORAX-4D »)
FEMTO-ST – UMR 6174, Montbéliard
Sébastien JAN
Titre du projet : IMADRON : Simulations numériques pour le contrôle par imagerie des traitements par hadronthérapie et radioimmunothérapie
Service Hospitalier Frédéric Joliot – CEA, Orsay
Jean-Michel LETANG
Titre du projet : ProTom : Tomographie par faisceaux de protons appliquée à la planification de traitement en protonthérapie
CREATIS/ Centre de Recherche en Acquisition et Traitement de l’Image pour la Santé- UMR 5220, Villeurbanne
Lydia MAIGNE
Titre du projet : DOsimétrie par simulations Monte Carlo GATE d’un traitement novateur du MElanome par radiothérapie interne vectorisée. (DOGME)
Laboratoire de Physique Corpusculaire – UMR6533, Aubière
Jean-Baptiste MANNEVILLE
Titre du projet : Microrhéologie intracellulaire des cellules tumorales
Institut Curie – Equipe Compartimentation et dynamique cellulaires – UMR 144, Paris
Laurent MENARD
Titre du projet : Nouveaux systèmes d’imagerie per-opératoire radioisotopique pour l’aide à la chirurgie cancéreuse
Imagerie et Modélisation en Neurobiologie et Cancérologie – UMR 8165, Orsay
Pierre NASSOY
Titre du projet : Nouvelle méthode de formation de sphéroïdes multicellulaires assistée par la microfluidique – Etude biophysique expérimentale et numérique de la régulation biomécanique de la progression tumorale in vitro
Physico-Chimie Curie – Institut Curie – UMR 168, Paris
Olivier PIOT
Titre du projet : Développement en champ proche optique de la spectroscopie Raman (TERS) pour son utilisation en nanoanalyse biologique
Biophotonique, Médicaments, Dynamique Cellulaire et Tissulaire – Université de Reims Champagne Ardenne, Reims
Cédric RAY
Titre du projet : Assurance qualité en hadronthérapie carbone avec l’imagerie par vertex d’interaction de protons
Institut de Physique Nucléaire de Lyon – UMR 5822, Villeurbanne
Benjamin RIBBA
Titre du projet : Optimisation in silico de l’administration sunitinib/irinotecan chez la souris nude porteuse de tumeurs coliques
INRIA EPI NUMED -, Lyon
Composition du comité d’évaluation
Président Alex MUELLER, Directeur Adjoint Scientifique, CNRS-IN2P3, Paris
Vice-président Jean BARTHE, Conseiller Scientifique, Laboratoire National Henri Becquerel, CEA, Gif-sur-Yvette
Membres
Habib AMMARI, Directeur de Recherche, Ecole Normale Supérieure, Paris
Klaus BACHER, Assistant professor, Department of Medical Physics and Radiation Protection, Ghent University, Ghent
Roberto CIRIO, Department of Experimental Physics, Faculty of Medicine and Surgery, University of Torino, Turin
Antonio GIULIETTI, Directeur de Recherche, Responsable UOS « Adriano Gozzini », Istituto Nazionale di Ottica, Pise
Christian MOREL, Professeur des Universités, Centre de Physique des Particules de Marseille – CNRS-IN2P3, Marseille
Francis R. VERDUN, Professeur associé, Directeur suppléant à l’Institut de radiophysique du CHUV, Lausanne
Jean-Philippe VUILLEZ, PU-PH de Biophysique et Médecine Nucléaire, Clinique de Médecine Nucléaire – CHU, Président de la SFMN, Grenoble
Stephan WALRAND, Médecine Nucléaire, Cliniques Universitaires Saint-Luc, Bruxelles