Comment réagit un mélanome malin à la chimiothérapie ? Une équipe de l’Inserm apporte aujourd’hui de nouveaux éléments de compréhension, ouvrant la voie à la mise au point de traitements plus efficaces pour guérir et éviter les récidives. Les travaux de l’équipe de Corine Bertolotto (Centre méditerranéen de médecine moléculaire de Nice) sont publiés ce jour sur le site de la revue Genes & Development.
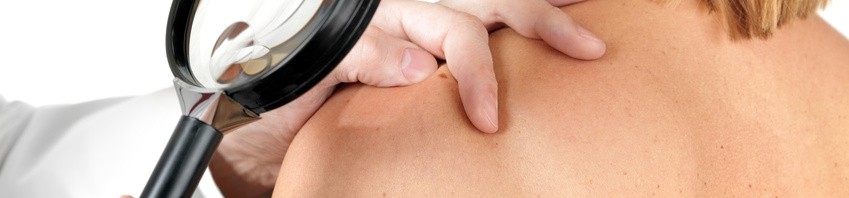
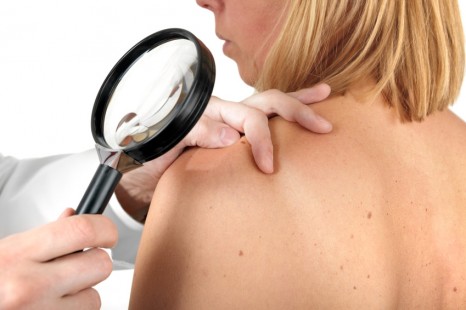
Les cancers de la peau sont les plus fréquents des cancers. Ils se guérissent très bien, sauf lorsqu’il s’agit d’un mélanome malin. Ce cancer rare, mais grave est lié à l’exposition aux rayons UV (soleil). Il est en constante augmentation. S’il peut survenir à tout âge, les cas chez les enfants restent exceptionnels, et le mélanome touche plus fréquemment les personnes entre 40 et 50 ans. En 2010, plus de 8 255 nouveaux cas de mélanome ont été diagnostiqués en France dont 53% chez les femmes et 47% chez les hommes. Dans cette maladie, qui fait plus de 1500 morts par an (1), le dépistage précoce augmente les chances de guérison, car sur une tumeur bien installée, les médicaments chimiothérapeutiques n’amènent généralement qu’une guérison incomplète, souvent suivie de rechutes fatales.
© Fotolia
Sénescence contre apoptose
Sous l’effet des médicaments chimiothérapeutiques, ou d’autres facteurs, comme le stress oxydatif, certaines cellules du mélanome ne « meurent pas » mais peuvent entrer en sénescence. La sénescence est un programme présent dans toutes les cellules normales qui empêche la multiplication des cellules génétiquement « instables », potentiellement précurseurs de tumeurs. Ce programme reste latent dans certaines cellules cancéreuses comme les cellules de mélanome. Il peut être réactivé en certaines circonstances. D’où le potentiel intérêt thérapeutique de « pousser » les cellules vers la voie de la sénescence qui pourrait constituer une stratégie thérapeutique a priori intéressante. Or, les données publiées ce jour par l’équipe de l’Inserm permettent de mieux comprendre comment l’induction de la sénescence pourrait, en fait, être impliquée dans l’échec thérapeutique du mélanome.
Le sécrétome du mélanome
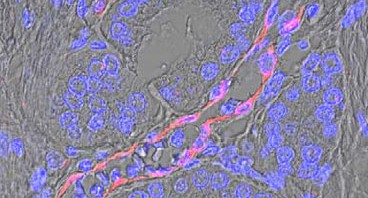
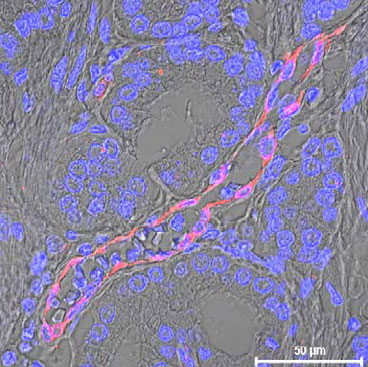
Les cellules en sénescence bien que ne proliférant plus, restent métaboliquement actives et sont capables de produire un ensemble de facteurs pro-inflammatoires, appelé sécrétome, qui modifie le microenvironnement de la tumeur. Les chercheurs en donnent confirmation, ayant pu établir que les cellules sénescentes du mélanome, exposées aux médicaments de chimiothérapie les plus couramment utilisés dans le mélanome (temozolomide et fotemustine), deviennent sénescentes et produisent un sécrétome aux propriétés pro-invasives et pro-tumorigènes. Les cellules tumorales deviennent non seulement de plus en plus difficiles à éliminer, mais elles deviennent plus mobiles, favorisant ainsi le développement de métastases à distance. « Nos données révèlent une partie des mécanismes contribuant à l’échec des chimiothérapies anti-mélanome et à l’émergence des rechutes. » résume Corine Bertolotto, Directrice de recherche Inserm, qui a dirigé cette étude.
Une nouvelle stratégie thérapeutique
Dès lors, la question dont se saisissent Corine Bertolotto et ses collaborateurs est : Comment se forme ce sécrétome ? Quelle est sa composition précise ? Une partie des événements moléculaires impliqués ont été déterminés par l’équipe niçoise et le sécrétome des cellules de mélanome entrées en sénescence a été caractérisé.
En particulier, un acteur essentiel du sécrétome semble être un messager cellulaire appelé CCL2 (chemokine-ligand-2) : son activité est responsable de l’augmentation de la capacité d’invasion des cellules non-sénescentes du mélanome et favorise le développement du mélanome in vivo.
Reste maintenant aux chercheurs à déterminer avec précision la composition exacte et le fonctionnement de tous les acteurs du sécrétome pour identifier des cibles d’interventions thérapeutiques pertinentes.
Note
(1) Données issues de la projection de l’incidence et de la mortalité par cancer en France en 2010, rapport InVS-INCa-Francim-HCL, avril 2010