Une équipe de recherche Inserm de Toulouse vient de décrypter les mécanismes à l’origine des différences d’absorption du fer entre les hommes et les femmes et montre chez la souris, comment, avec un médicament déjà utilisé dans le traitement de certains cancers bronchiques, on peut « contrer » cette action de l’hormone mâle.
Les résultats sont publiés dans la revue Hepatology du mois d’août 2013.
Le métabolisme du fer n’est pas régulé de façon équivalente chez les hommes et chez les femmes. En conséquence, les maladies chroniques du foie associées à une capacité réduite à produire de l’hepcidine – une hormone qui inhibe l’absorption du fer par le duodénum-, sont souvent plus sévères chez les hommes que chez les femmes. C’est le cas de l’hépatite C, de la maladie alcoolique du foie et de l’hémochromatose héréditaire.
© Fotolia
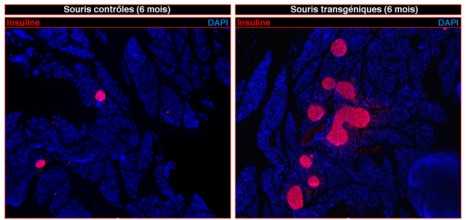
Dans le but de mieux comprendre les mécanismes sous-tendant ce dimorphisme sexuel, Marie-Paule Roth et ses collaborateurs du centre de physiopathologie de Purpan (Unité mixte Inserm, CNRS, Université Paul Sabatier, Toulouse) ont tiré parti des grandes différences d’expression de l’hepcidine et de la surcharge en fer observées entre des souris mâles et femelles présentant un trouble du métabolisme du fer.
Les chercheurs ont montré que la testostérone était un répresseur puissant de l’hepcidine chez ces souris car, dans le foie, elle active les récepteurs d’un facteur de croissance, l’EGF. Or, lorsque ces récepteurs de l’EGF sont inhibés par un médicament utilisé dans le traitement de certains cancers bronchiques chez les souris mâles, la répression exercée par la testostérone est levée. La production d’hepcidine est augmentée significativement.
La castration des souris mâles s’accompagne non seulement d’une augmentation de l’hepcidine mais également d’une très forte réduction de la surcharge en fer cardiaque et pancréatique de ces souris.
En conclusion, Marie-Paule Roth et son équipe soulignent : « ces résultats indiquent que la répression de l’hepcidine par la testostérone peut avoir des répercussions cliniques chez les patients qui, pour différentes raisons, ne sont capables de produire de l’hepcidine qu’en quantité limitée ». Inhiber l’activation des récepteurs de l’EGF chez ces patients pourrait les aider à produire davantage d’hepcidine et limiterait ainsi la surcharge en fer qui aggrave le pronostic des maladies chroniques du foie, expliquent-ils.