Malgré le déclin progressif des fonctions physiologiques lié à l’âge, l’organisme dispose de mécanismes de protection essentiels. Parmi eux, la « tolérance aux maladies » constitue une stratégie immunitaire encore largement méconnue, qui vise à limiter les dommages provoqués par les agents pathogènes. Une étude, menée par des chercheurs et chercheuses de l’Inserm, du CNRS et d’université Côte d’Azur, publiée dans Immunity, identifie le rôle clé des cellules immunitaires p16High comme des régulateurs centraux de cette « tolérance aux maladies ». Les scientifiques sont parvenus à augmenter leur prolifération grâce à un vaccin à ARN messager dirigé contre le virus de la Covid-19, et ont constaté que ces cellules permettaient de stabiliser les réponses inflammatoires, de préserver l’intégrité des tissus et d’assurer la survie de l’organisme face à des agressions sévères.
Le vieillissement se manifeste par la détérioration progressive des fonctions physiologiques au fil du temps, affectant tous les tissus et les organes. Chez l’humain, ce déclin peut induire le développement de multiples pathologies comme le cancer, le diabète, ou encore des maladies neurodégénératives. Afin de contrer la détérioration des tissus avec l’âge, l’organisme possède une fonction appelée « sénescence », qui entraîne un arrêt des divisions cellulaires par l’activation de protéines spécifiques et permet d’empêcher les cellules endommagées de proliférer.
Une protéine connue qui participe au mécanisme de sénescence est p16, qui permet de ralentir les divisions cellulaires. Une équipe de recherche dirigée par Dmitry Bulavin, chercheur Inserm, à l’Institut de recherche sur le cancer et le vieillissement (Inserm/CNRS/Université Côte d’Azur), s’est intéressée à cette protéine afin de comprendre son implication dans la « tolérance aux maladies », une stratégie immunitaire, permettant non pas d’éliminer les agents pathogènes, mais de limiter les dommages qu’ils provoquent lors d’une infection.
Dans un premier temps, dans des modèles murins, les scientifiques se sont intéressés aux cellules immunitaires appelées « p16High » riches en protéine p16. Ils ont constaté que ces cellules s’accumulaient dans les tissus avec l’âge à différents endroits de l’organisme et que leur nombre augmentait en cas d’inflammation ou d’endommagement des tissus chez la jeune souris, améliorant significativement la survie dans les cas d’inflammation sévère. Leur production précoce et durable était par ailleurs associée à une amélioration significative de la durée de vie en bonne santé.
Ces résultats suggèrent que les cellules immunitaires p16High pourraient constituer un axe protecteur inédit dans la régulation immunitaire liée à la « tolérance aux maladies ». L’activation tout au long de la vie des voies biologiques permettant leur production pourrait ainsi avoir des effets bénéfiques à long terme.
En ciblant une catégorie spécifique de cellules immunitaires, les macrophages dits « résidents », qui ont une durée de vie particulièrement longue, les chercheuses et chercheurs ont observé que ceux qui étaient riches en protéine p16 exprimaient moins de marqueurs biologiques de sénescence. Leur enrichissement en protéine p16 était permis principalement par l’activation de voies biologiques, dont une en particulier appelée TLR7. Or cette dernière est aussi connue pour être la cible biologique activée par les vaccins à ARN messager dirigés contre le virus de la Covid-19.
Les scientifiques se sont ensuite penchés sur l’intérêt du vaccin à ARNm anti-SARS-CoV-2 dans la « tolérance aux maladies ». Toujours chez la souris, ils ont observé que le vaccin induisait efficacement la présence de cellules immunitaires p16High en activant la voie TLR7 et que ces cellules protégeaient contre l’inflammation sévère et l’endommagement des tissus. Chez l’humain [1], l’utilisation du vaccin a permis d’induire la production de p16High dans des cas sévères de Covid-19.
Il a été montré dans des études antérieures que les cellules immunitaires p16High étaient particulièrement diminuées dans les cas sévères de Covid. Nos résultats suggèrent que les vaccins à ARNm déclencheraient une “reprogrammation” du système immunitaire, favorisant l’émergence de cellules immunitaires p16High, l’instauration d’un état de “tolérance aux maladies” et la limitation des réponses inflammatoires excessives chez la souris et l’humain. Ils actionneraient une première ligne de défense jusqu’ici insoupçonnée, fondée sur la tolérance plutôt que sur l’élimination des agents pathogènes.
Dmitry Bulavin
Ces travaux ouvrent ainsi la voie à de nouvelles approches thérapeutiques visant à renforcer la « tolérance aux maladies », en s’appuyant sur des mécanismes immunitaires naturels et modulables, dont les vaccins à ARNm pourraient constituer un levier majeur. « Maintenir un niveau élevé de cellules immunitaires p16High dès le plus jeune âge pourrait représenter une stratégie pour limiter l’inflammation chronique et favoriser un vieillissement en meilleure santé », conclut Dmitry Bulavin.
[1] Cohorte CovImmune pilotée par le CHU de Nice, recrutée entre avril 2020 et septembre 2021 à la suite d’une consultation aux urgences après la manifestation des symptômes de la Covid-19, ou en tant que cas contact du Covid-19 diagnostiqué.

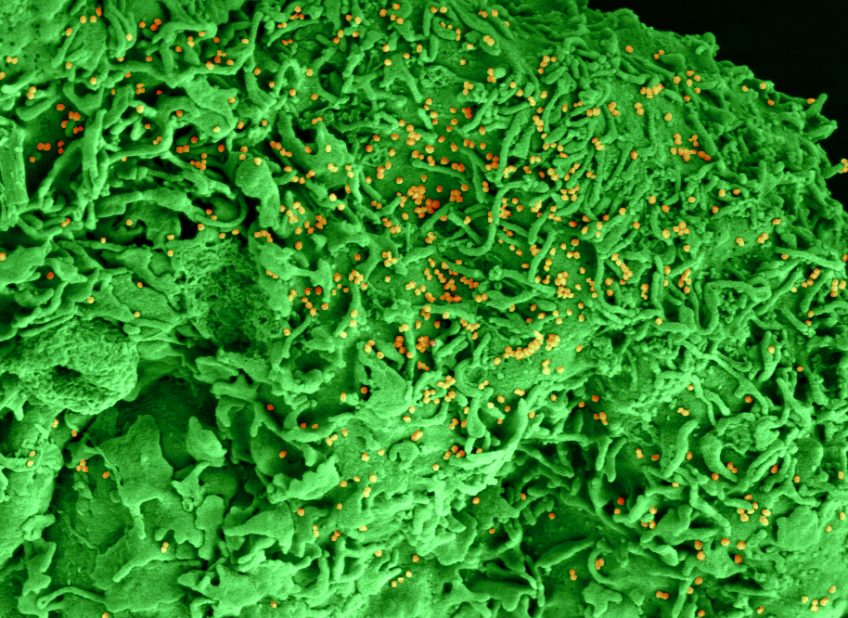
 Cette image montre le virus du SARS-CoV-2 (en jaune). © National Institute of Allergy and Infectious Diseases – Rocky Mountain Laboratories, NIH
Cette image montre le virus du SARS-CoV-2 (en jaune). © National Institute of Allergy and Infectious Diseases – Rocky Mountain Laboratories, NIH