50% des fractures ne cicatrisent pas seules et ont besoin d’une reconstruction osseuse chirurgicale, ce qui représente un million de patients en Europe. Le projet REBORNE (Régénération des défauts osseux utilisant de nouvelles approches d’ingénierie biomédicale) financé par la Commission Européenne et coordonné par l’Inserm, vient d’obtenir l’accord de l’Agence nationale de sécurité du médicament et des produits de santé pour débuter un essai clinique en chirurgie orthopédique visant à réparer les os à partir de cellules souches adultes, combinées à un biomatériau. L’essai clinique se déroulera en France dans le CHU de Créteil et le CHRU de Tours avec la collaboration de l’Etablissement Français du Sang.
L’originalité du projet REBORNE, commencé il y a 3 ans, réside dans le fait d’utiliser des cellules souches mésenchymateuses (CSM), présentes dans la moelle osseuse, pour intervenir dans la cicatrisation des fractures. Il s’agit d’amplifier en culture, puis d’associer les cellules souches adultes du patient à un biomatériau, et de greffer l’ensemble au niveau de la fracture. Les tests précliniques prometteurs permettent aujourd’hui le lancement de ce nouvel essai clinique.
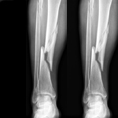
Après un traumatisme (chute ou accident de la route), le risque de retard ou d’absence de consolidation du tibia, du fémur ou de l’humérus est très élevé et nécessite souvent une greffe osseuse autologue (prélèvement d’os du patient). Cependant, la quantité de greffon disponible est limitée et des complications au niveau du site de prélèvement sont très souvent observées.
Les partenaires du projet européen REBORNE proposent un traitement alternatif à l’aide de cellules souches mésenchymateuses autologues, associées à un substitut osseux synthétique.
© P. Layrolle, Inserm
A partir d’un prélèvement de moelle osseuse effectué sous anesthésie locale, les cellules souches mésenchymateuses sont isolées et amplifiées en culture pendant 21 jours, avant d’être associées en salle d’opération à des granulés en céramique de phosphate de calcium, puis finalement implantées là où la consolidation des os est retardée. Le biomatériau servant ainsi « d’échafaudage », favorise la prolifération des cellules souches. Celles-ci se différencient ensuite en cellules osseuses et régénèrent le tissu osseux au niveau de la fracture. 
© P. Layrolle, Inserm
L’Agence nationale de sécurité du médicament et des produits de santé a donné son accord le 03 janvier 2013 pour que l’essai, promu par l’Inserm, débute dès à présent en France avec 7 patients suivis au CHU de Créteil et au CHRU de Tours. D’ici la fin du projet (fin 2014), 30 patients seront recrutés en France, Espagne, Allemagne et Italie dans cette étude multicentrique européenne.
« L’objectif de l’essai est de démontrer que l’utilisation des biomatériaux et des cellules souches est sans danger et au moins équivalente aux traitements standards, sans leurs inconvénients. Cette chirurgie est moins invasive et préserve le stock osseux du patient. Pour ces raisons, elle est préférable à la greffe afin de déclencher la cicatrisation osseuse. »
explique Pierre Layrolle, directeur de recherche Inserm et coordinateur du projet REBORNE.Pour en savoir plus
REBORNE – Régénération des défauts osseux utilisant de nouvelles approches d’ingénierie biomédicale
Le projet REBORNE a pour objectif de développer de nouveaux biomatériaux qui stimulent la formation de tissu osseux pour corriger les défauts de régénération osseuse en chirurgie orthopédique et maxillo-faciale. Les biomatériaux, combinés à l’utilisation des cellules souches, sont des alternatives intéressantes aux greffes biologiques.
REBORNE a démarré en janvier 2010 et dure 5 ans, avec un budget total d’environ 12 millions d’euros de l’Union Européenne (PC7). Le projet implique 24 partenaires, basés dans 8 pays européens : https://www.reborne.org/presentation.html
Créé en 1964, l’Institut national de la santé et de la recherche médicale (Inserm) est un établissement public à caractère scientifique et technologique, placé sous la double tutelle du Ministère de l’Enseignement supérieur et de la recherche et du ministère de la Santé.
Ses chercheurs ont pour vocation l’étude de toutes les maladies, des plus fréquentes aux plus rares, à travers leurs travaux de recherches biologiques, médicales et en santé des populations.
Avec un budget 2011 de 905 M€, l’Inserm soutient quelque 300 laboratoires répartis sur le territoire français. L’ensemble des équipes regroupe près de 13 000 chercheurs, ingénieurs, techniciens, gestionnaires…
L’Inserm est membre de l’Alliance nationale pour les sciences de la vie et de la santé, fondée en avril 2009 avec le CNRS, le CEA, l’Inra, l’Inria, l’IRD, l’Institut Pasteur, la Conférence des Présidents d’Université (CPU) et la Conférence des directeurs généraux de centres hospitaliers régionaux et universitaires. Cette alliance s’inscrit dans la politique de réforme du système de recherche visant à mieux coordonner le rôle des différents acteurs et à renforcer la position de la recherche française dans ce secteur par une programmation concertée.
L’Inserm est le premier porteur de projets européens « Santé » avec 28 projets coordonnés par l’institut dans le cadre PC7.
Etablissement public placé sous tutelle du ministère de la Santé, l’Etablissement français du sang a été créé en 2000. Dans le cadre du don de sang éthique, il a pour mission première d’assurer l’autosuffisance en produits sanguins sur tout le territoire. Au-delà de ce cœur de métier, l’EFS développe des activités thérapeutiques et des activités de recherche ayant pour objectif le progrès scientifique et médical au service des patients. L’EFS compte près de 10 000 collaborateurs.
L’EFS est, un acteur majeur de l’ingénierie cellulaire en France, mettant à disposition des CHU plus de la moitié des plateformes de thérapie cellulaires en France. Environ 60% des prélèvements de cellules souches sont préparés, conservés et distribués dans 18 sites de l’EFS (répartis dans 12 des 14 établissements de métropoles).
Grâce à ses plateformes l’EFS assure déjà majoritairement la mise en place des productions pour les essais de phase 1 et 2 au niveau national, les équipes de recherche liées à ces plates-formes faisant le lien indispensable entre recherche et production pour l’usage clinique.
L’EFS, ayant vocation à acquérir le statut d’Etablissement pharmaceutique MTI, structure un réseau de plateformes innovantes dédiées aux phases I & II. Ces plateformes expertes sont reconnues et cofinancées dans le cadre de projets nationaux (plateforme ECELLFRANCE de médecine régénérative, STEMRED pour la production de globules rouges de culture à partir de cellules pluripotentes induites) et européens (programme Cascade, Reborne et ADIPOA).
Le maillage territorial, associé au savoir-faire de l’EFS, en font un acteur et un moteur incontournable de la thérapie cellulaire et de la médecine régénérative.