Pendant 5 semaines, 5 équipes de recherche internationales vont conduire une expédition scientifique au Népal, au cœur de l’Himalaya, proche du sommet du Manaslu (8156 m). La partie française de l’expédition, coordonnée par un chercheur de l’Inserm (Unité 1042 « Hypoxie et physiopathologies cardiovasculaire et respiratoire » Inserm/Université Joseph Fourier), va y mener un projet original sur l’impact cérébral et cardiaque de l’altitude et sur les altérations du sommeil qu’elle induit. Les chercheurs français étudieront également l’intérêt d’un masque spécifique d’amélioration de l’oxygénation pour combattre les symptômes du mal aigu des montagnes. Pour cela, 50 volontaires les accompagneront dans ce trek à plus de 5000 mètres d’altitude. Les internautes pourront suivre cette expédition en temps réel sur les réseaux sociaux grâce au hashtag #scienceausommet
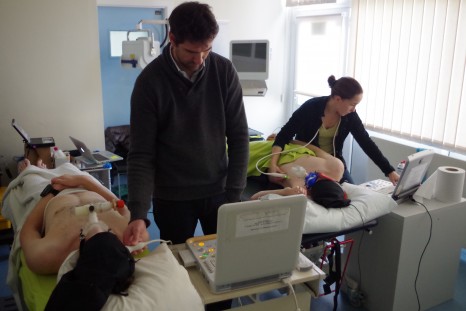
Echocardiographie réalisée au sommet du Mont Blanc lors d’une précédente expédition © Samuel Verges
Le développement des loisirs, la multiplication des séjours en moyenne et haute altitude pour des personnes parfois peu expérimentées pose la question de l’intolérance à l’altitude. Ces difficultés d’adaptations résultent de mécanismes physiopathologiques associés à la diminution de la disponibilité en oxygène au fur et à mesure que l’on s’élève en altitude.
Ces pathologies, invalidantes au point d’imposer l’interruption du séjour en altitude, parfois graves voire fatales sont le mal aigu des montagnes (associations de symptômes tels le mal de tête, fatigue, nausées, etc…), l’œdème pulmonaire de haute altitude (généralement associé à une toux, un essoufflement et lié à une accumulation de liquide dans les poumons pouvant s’avérer grave) et l’œdème cérébral de haute altitude (fuites de liquide dans le cerveau constituant un phénomène particulièrement grave, avec des troubles importants du comportement). Les formes aiguës surviennent chez des personnes peu acclimatées à l’altitude, rapidement après l’exposition (6 h à 4 jours). Les formes foudroyantes surviennent même après acclimatation, à des altitudes supérieures à 5000 mètres. De manière générale, une personne sur deux est touchée par le mal aigu des montagnes au-delà de 4000 mètres, trois sur quatre au-dessus de 5000 mètres.
Ces conditions peuvent, dans une certaine mesure, être évitées par le respect de règles simples de prévention. Mais, il semble aussi que certaines personnes soient plus susceptibles que d’autres de développer ces symptômes en altitude. Les facteurs prédictifs de la tolérance à l’altitude, les mécanismes sous-jacents aux difficultés d’adaptation, leur prise en charge et les stratégies optimales d’acclimatation restent particulièrement méconnus.
Ce sont les thèmes qui seront étudiés par l’équipe de recherche française, sous la coordination de Samuel Vergès, chargé de recherche Inserm au sein de l’Unité 1042 « Hypoxie et physiopathologies cardiovasculaire et respiratoire ». L’équipe est composée de 6 scientifiques et médecins expérimentés ayant tous une expérience de la haute montagne et d’expéditions scientifiques de ce type.
Un premier projet de recherche sur le cœur et le cerveau
Autour de 3 grands axes, ce projet vise, en faisant appel à des techniques innovantes et transportables (utilisables en haute altitude) à préciser les effets d’un séjour en haute altitude sur le cerveau et le cœur et d’évaluer l’effet d’un masque de ventilation par pression expiratoire positive sur ces réponses cérébrales et cardiaques.
- Manque d’oxygène et cerveau
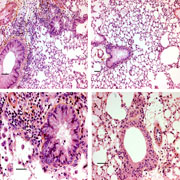
Des études in vitro et in vivo montrent que le manque d’oxygène altère la fonction neuronale et diminuerait les performances cognitives humaines. Une série d’études en laboratoire et en haute altitude (Observatoire VALLOT, massif du Mont-Blanc) ont mis en évidence des perturbations cérébrales significatives induites par l’hypoxie, à la fois dans les premières heures d’exposition et après plusieurs jours. L’anatomie du cerveau, la perfusion et l’oxygénation cérébrales ainsi que la fonction des neurones moteurs en particulier sont altérées par l’hypoxie, ce qui conduit à reconsidérer les mécanismes d’adaptation à l’altitude en incluant le versant cérébral comme un facteur jouant probablement un rôle majeur.
- Altitude et fonctionnement du cœur
L’exposition à l’altitude est associée à des modifications majeures au niveau cardiaque. Des études antérieures ont démontré que l’hypoxie aigüe entraîne une altération des propriétés de relaxation du myocarde. Une diminution des propriétés contractiles des cardiomyocytes pourrait être responsable de ce phénomène sans que des preuves objectives n’aient été encore obtenues. De nombreuses études ont également montré que l’exposition à l’altitude engendre des altérations au niveau du ventricule droit qui pourrait être impliqué de manière importante dans le relâchement du ventricule gauche, sans que les phénomènes mécaniques en cause ne soient totalement établis.
Depuis peu, à partir d’une nouvelle technologie d’échographie par poursuite des signatures acoustiques (Speckle Tracking Imaging), la mesure des vitesses et des déformations myocardiques peut être réalisée de manière globale, permettant une investigation de la contractilité et des capacités de relaxation myocardiques, ouvrant ainsi de nouvelles perspectives de compréhension des effets de l’hypoxie d’altitude sur le cœur.
- Développement d’un masque minimisant les effets délétères de l’altitude
L’ajout d’une pression expiratoire positive, dite PEP, au niveau de la bouche d’un personne en condition d’altitude permet une augmentation artificielle des pressions intra-pulmonaires et a été suggéré par certaines équipes de recherche comme méthode susceptible de prévenir ou de minimiser les effets délétères de l’altitude. Les chercheurs du laboratoire Hypoxie-Physiopathologie (HP2) de Grenoble ont récemment démontré l’intérêt de cette méthode pour augmenter l’oxygénation sanguine et musculaire[1].
Leurs résultats suggèrent qu’un équipement de type masque portatif induisant une augmentation de la pression expiratoire pourrait constituer une méthode non-pharmacologique originale et efficace pour améliorer l’acclimatation à l’altitude et les symptômes associés au mal aigu des montagnes. Une étude de grande ampleur et de terrain en haute montagne est nécessaire pour déterminer si la PEP est susceptible de devenir une méthode à diffuser largement. La commercialisation d’un système de masque PEP pourra être envisagée, avec l’avantage d’être une méthode portable, peu encombrante, non-médicamenteuse et utilisable par le plus grand nombre.
Un second projet sur l’altération du sommeil en altitude
L’altitude est connue pour profondément perturber le sommeil et provoquer des apnées du sommeil, dites d’origine centrale. Dès 2500 mètres d’altitude, on observe une diminution moyenne ainsi que des oscillations cycliques de l’oxygénation du sang. Le développement de ces troubles s’accompagne également d’une diminution de l’efficacité du sommeil, d’une augmentation du temps d’endormissement, d’une diminution de la durée des phases de sommeil profond ainsi que d’une augmentation importante des éveils intrasommeil. La quantification de ces troubles a longtemps été limitée à l’analyse des oscillations de la saturation artérielle en O2.
Une question n’a cependant à l’heure actuelle pas encore trouvé de réponse claire : les apnées centrales sont-elles un marqueur d’une mauvaise ou d’une bonne adaptation de l’organisme à l’altitude ? Cette question est importante car de grandes différences existent d’un sujet à l’autre en termes d’intensité des perturbations du sommeil induites par une exposition à l’altitude. Il a été récemment montré dans le laboratoire dirigé par Samuel Vergès, que des individus qui présentent des symptômes sévères d’intolérance à la haute altitude ont (au cours d’une nuit en altitude simulée en laboratoire) moins d’apnée du sommeil que des individus comparables mais qui eux tolèrent bien la haute altitude. Il reste cependant à l’établir sur le terrain en haute altitude.
L’étude de cette question devrait améliorer la compréhension des mécanismes d’adaptation à l’altitude et influencer les conseils et évaluations proposés aux personnes se rendant en altitude.
L’étude portée par le groupe français au sein de l’expédition scientifique a donc pour objectif :
– D’évaluer les effets du masque à résistance expiratoire (ventilation avec PEP) sur l’oxygénation artérielle et tissulaire, sur les fuites extravasculaires pulmonaires ainsi que sur les symptômes de mal des montagnes lors d’un séjour en haute altitude pour un grand échantillon de volontaires.
– D’étudier sur la base de nouvelles technologies (spectroscopie proche infrarouge, échographie par Speckle Tracking) les altérations cérébrales et cardiaques induites par le manque d’oxygène (hypoxie) de haute altitude et évaluer leur réversibilité grâce au port du masque.
– De comparer les modifications du sommeil induites par l’altitude chez des trekkeurs s’adaptant bien à l’altitude comparé à ceux présentant des symptômes de mal aigu des montagnes.
L’étude par les chercheurs des effets du manque d’oxygène sur des organismes sains en haute altitude doit permettre de mieux comprendre les conséquences du manque d’oxygène chez certains patients en plaine, par exemple atteints de pathologies respiratoires. La haute altitude est ainsi un véritable laboratoire à ciel ouvert constituant un modèle original d’étude des capacités et des limites d’adaptation de l’organisme humain.
Une première phase d’étude en plaine
Tous les participants au trek et à l’ascension du Manaslu se sont prêtés, du 16 au 23 février dernier, à une batterie d’évaluations scientifiques et médicales au niveau de la mer au Pays de Galles (Bangor University). L’ensemble des mesures qui seront effectuées en haute altitude ont été réalisées au niveau de la mer, permettant d’obtenir ainsi les valeurs de référence pour chaque sujet auxquelles seront comparées les mesures de haute altitude.
Mesures en plaine © Samuel Verges
La phase de test en plaine a été l’occasion d’aborder les questions techniques et logistiques à résoudre pour que les tests puissent être répétés dans les meilleures conditions possibles en haute altitude lorsque que la pression atmosphérique sera réduite (ce qui impacte fortement le matériel), que le froid sera présent (jusqu’à -20°C) et que les organismes tant des chercheurs que des sujets volontaires seront durement touchés par l’altitude.
Un laboratoire scientifique installé à 5000 mètres
5 groupes de 10 personnes partiront de Katmandou avec 1 jour d’intervalle chacun pour étaler les mesures. 10 jours sont nécessaires pour arriver à destination. Les 5 équipes de recherche internationales installeront alors leur laboratoire et toute la logistique nécessaire (tentes, production d’énergie solaire et par éolienne, etc…) légèrement au-dessus du camp de base du Manaslu à un peu plus de 5000 mètres d’altitude. L’essentiel des mesures de haute altitude seront réalisées sur l’ensemble des participants au trek qui arriveront jour après jour. D’autres mesures seront réalisées au cours du trek et lors de l’ascension du Larkya Peak (6249 m). L’ensemble de l’expédition durera 5 semaines entre le 21 mars et le 26 avril.
Comme en plaine, les évaluations consisteront à mesurer le liquide extravasculaire pulmonaire par échographie pleuropulmonaire, la perfusion cérébrale par Doppler transcranien, l’oxygénation cérébrale par spectroscopie proche infrarouge et la fonction cardiaque par échographie en Speckle Tracking avant et pendant une ventilation sous pression expiratoire positive. Les symptômes seront évalués par questionnaire. Enfin, le sommeil sera évalué au cours des nuits passées sous tente au camp de base du Manaslu par la pose de différents capteurs permettant d’identifier la qualité du sommeil, la survenue d’apnée du sommeil associée à une chute de l’oxygénation du sang telles que fréquemment observées en haute altitude. Ces mesures sont identiques aux tests dits de polygraphie réalisés au sein des laboratoires du sommeil des hôpitaux afin de diagnostiquer chez les patients un syndrome d’apnée du sommeil.
Après 4 jours d’acclimatation à 5000 mètres, cette batterie de test sera reconduite afin de voir les adaptations du corps humain à cette altitude élevée. L’ensemble des participants restera 10 jours au camp de base puis l’équipe bouclera le tour du Manaslu avec une descente en 3 jours jusqu’à Besisahar.
Les participants à ce trek présentent un profil classique de population prenant part à des treks en haute altitude, âgés de 22 à 65 ans, de condition physique et d’expérience de l’altitude relativement variées. Ils se sont portés volontaires pour réaliser un trek de plusieurs semaines autour du Manaslu et pour, dans ce cadre, se prêter à des expériences scientifiques en particulier pendant 5 jours consécutifs au camp situé au point culminant du tour du Manaslu, où seront installés les laboratoires.
Les 4 autres projets scientifiques internationaux menés dans le cadre du projet MEDEX
MEDEX (www.medex.org.uk) a été créé en 1992 en Grande Bretagne pour encourager des projets d’expéditions scientifiques et médicales. Plusieurs expéditions scientifiques de grandes envergures ont été depuis organisées tous les 4-5 ans, en 1994 sur l’Everest, en 1998 au Kanchejunga, en 2003 en Hongu et en 2008 dans la Hidden Valley. Ces expéditions ont conduit à des avancées scientifiques et médicales majeures en lien avec l’altitude, avec à la clef des publications scientifiques ainsi que des communications grands publics et des actions de formation des professionnels et pratiquants de la haute montagne.
Lors de cette expédition, 4 autres projets scientifiques seront conduits en parallèle des 2 menés par l’équipe de Samuel Verges.
– Comment faire face au stress pour les travailleurs en altitude –équipe de Sue Paddon (Advanced Personnel Management, Australia-UK))
– Influence de la préparation physique et mentale sur le succès d’une expédition en haute altitude – équipe de Sam Olivier et Jamie Macdonald (Bangor University)
– Perturbation de la fréquence cardiaque comme indicateur du mal aigu des montagnes ? Jamie Macdonald (Bangor University)
– Impact des treks sur la santé des personnels Népalais employés pour accompagner les expéditions – Mary Morrell (Impérial College of London)
Le dispositif d’accompagnement sur les médias sociaux
Pour faire vivre une expédition scientifique aux internautes comme s’ils y étaient alors même que l’endroit (le sommet du Manaslu) est particulièrement inaccessible, l’Inserm se mobilise pour suivre l’expédition. Des contenus enrichis (photos ou vidéos) seront postés chaque jour sur @Insermlive et sur la page Facebook de l’Institut : du quotidien (avion, arrivée sur place, installation) au détail des expérimentations scientifiques (quels dispositifs, quels buts, quelles mesures, etc…)
Un hashtag #scienceausommet
Un relais sur @inserm_en pour la communauté internationale est également prévu.
Sur la salle de presse de l’Inserm, un module de discussion instantanée sera ouvert pour poser des questions aux chercheurs avant leur départ et après leur retour.
[1] Ces résultats ont été publiés dans PlosOne