Chaque année, l’obésité tue 2,8 millions de personnes dans le monde. Face à un poids morbide – et au diabète de type 2 qui en est une conséquence directe – la chirurgie s’impose en dernier recours. Étrangement, chez les patients opérés, le diabète disparait avant et indépendamment de la perte du poids. Des chercheurs de l’Inserm, avec l’aide des médecins de l’hôpital Bichat, AP-HP, révèlent que l’intestin remodelé par l’intervention pourrait être à l’origine de ce meilleur contrôle de la glycémie. Cette étude est parue dans Gastroenterology.
La surcharge pondérale même légère n’est jamais inoffensive. A l’origine de maladies cardiovasculaires, de troubles musculo-articulaires et du développement d’un diabète de type 2, elle peut mener à un décès prématuré.
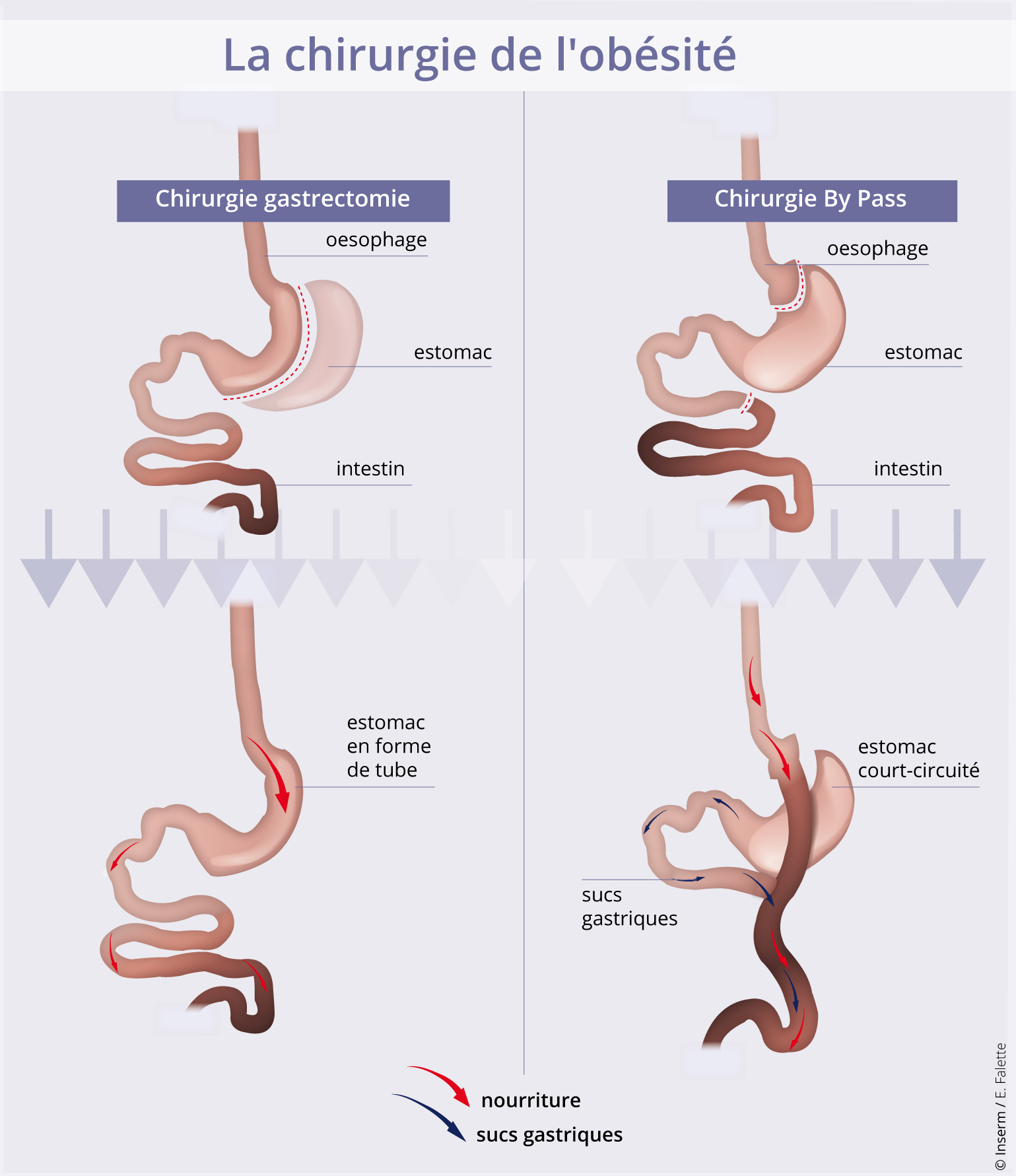
Lorsque l’excès de poids est tel qu’il menace la santé, il ne reste parfois qu’une solution : la chirurgie bariatrique pour réduire l’appétit du patient. Les interventions les plus couramment proposées sont la gastrectomie en manchon et le bypass gastrique. Quelle que soit la solution choisie, cela implique l’élimination d’une majeure partie de l’estomac. Dans le premier cas, l’estomac est remodelé pour ne former plus qu’un tube. Dans le cas du bypass, le circuit alimentaire est modifié : le chirurgien connecte directement une toute petite poche du haut de l’estomac à l’intestin formant la « branche Y ». Le reste de l’estomac, désormais exclu du trajet des aliments, continue à fournir les enzymes nécessaires à la digestion. Celles-ci rejoignent le circuit des aliments plus bas dans le tube digestif.
Curieusement, si les patients maigrissent rapidement dans les mois qui suivent l’opération, les médecins ont remarqué une nette amélioration de leur diabète de type 2, pratiquement dès leur sortie de l’hôpital. Comment expliquer ce phénomène ? Pour les chercheurs de l’Inserm, la réponse est claire : la chirurgie n’a pas qu’un simple effet sur la prise alimentaire mais modifie également le métabolisme de l’intestin.
Afin de confirmer leur hypothèse, les scientifiques ont reproduit les deux techniques chez un modèle de rat obèse.
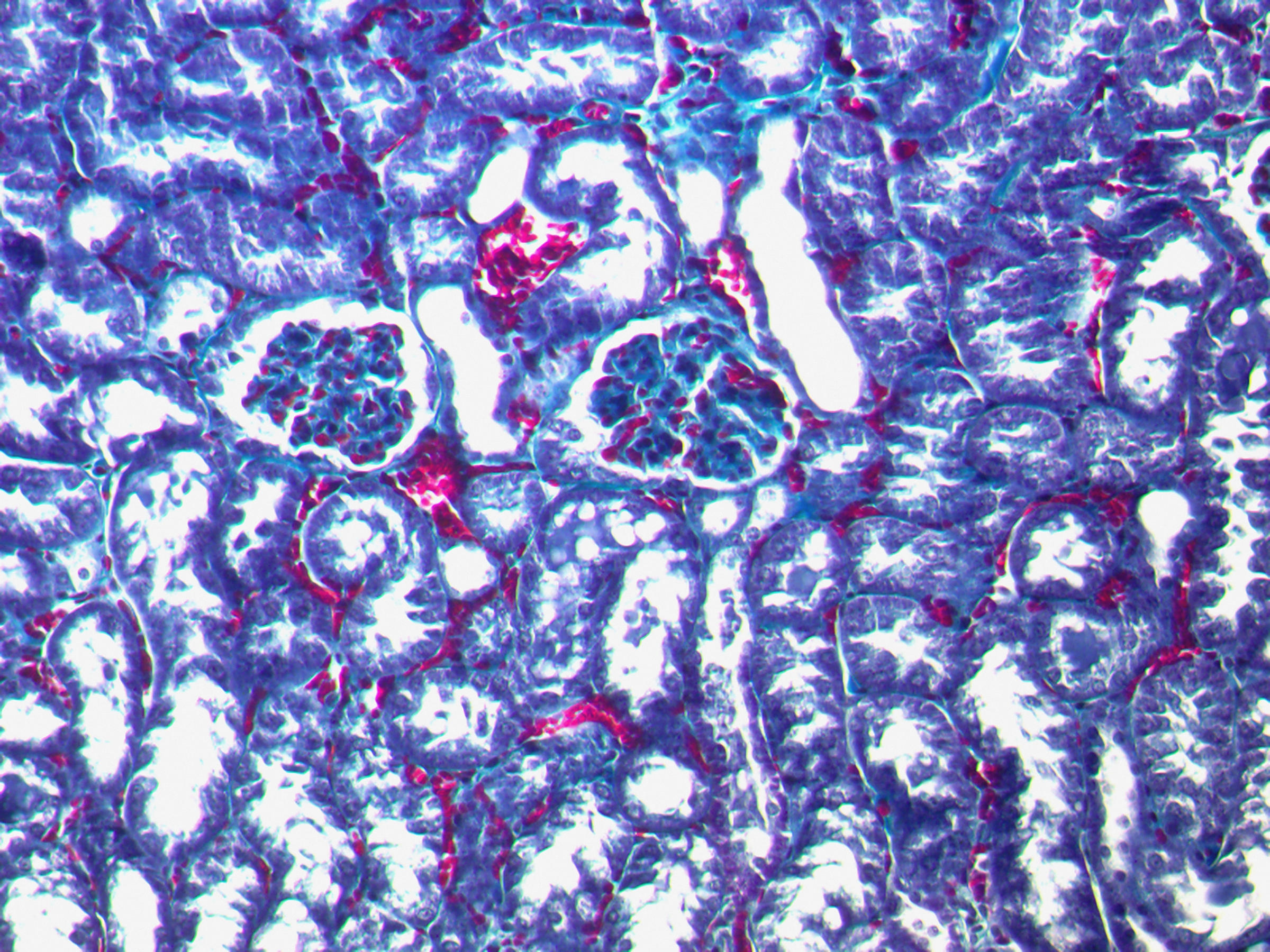
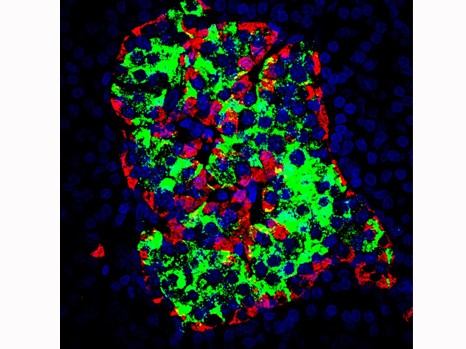
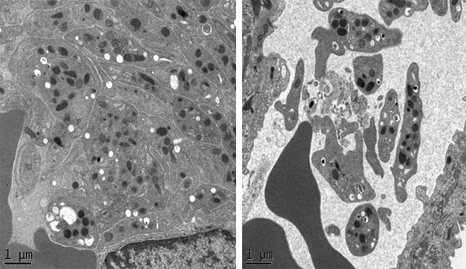
A la suite du bypass, la branche Y des rongeurs grossit remarquablement car les cellules qui la constituent prolifèrent anormalement. De plus ces cellules exposent à leur surface un type de transporteur du glucose inhabituel pour l’intestin Ces observations sont retrouvées chez les patients opérés au sein de l’hôpital Bichat. Les personnes atteintes de diabète de type 2 sécrètent de l’insuline mais leurs organes ne lui répondent plus. Le taux du sucre dans le sang n’est plus contrôlé et reste anormalement élevé après chaque repas ce qui endommage les tissus.
« Nous avons marqué le glucose pour suivre son trajet. Après la chirurgie, l’intestin nouvellement remodelé du patient, comme celui du rat, se met à consommer des quantités très importantes de glucose, explique Maude Le Gall, chargée de recherche Inserm. Il détourne le glucose alimentaire et sanguin pour sa propre consommation. Ce phénomène, qui se met en place au bout d’à peine quelques jours, pourrait contribuer à l’amélioration rapide de la glycémie et la disparition du diabète. »
La gastrectomie, un mécanisme différent pour un résultat similaire
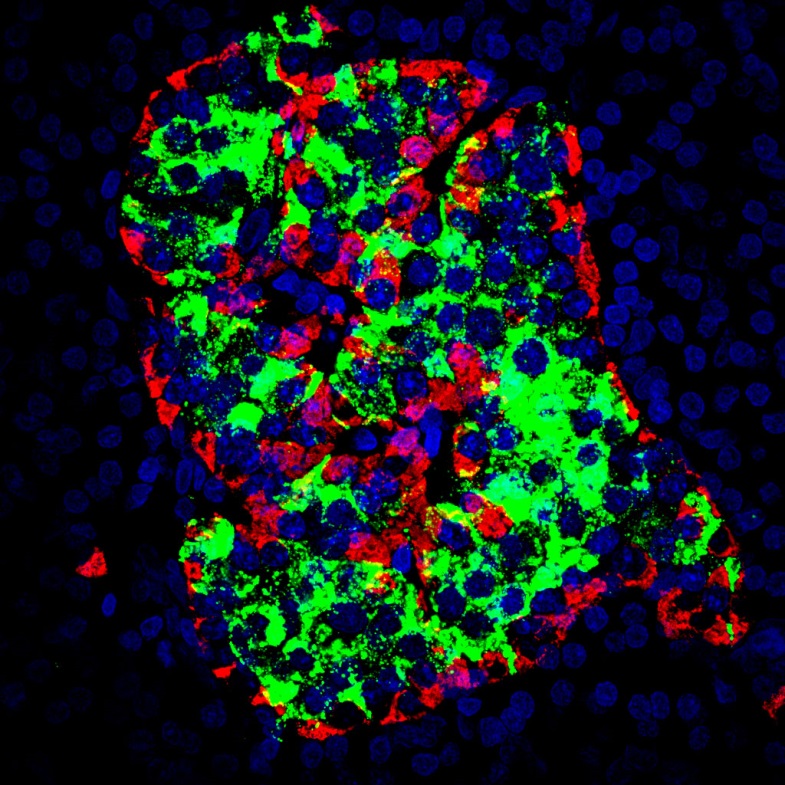
L’opération par gastrectomie, quant à elle, n’influe pas sur la taille de l’intestin mais agit aussi sur son fonctionnement cellulaire. L’absorption du glucose alimentaire par les cellules intestinales devient moins importante. En revanche, le nombre de cellules sécrétant le peptide GLP-1 augmente considérablement, alors que sa production est habituellement défaillante chez les personnes obèses. Celui-ci agit sur le pancréas pour augmenter sa production d’insuline. En conséquence, le contrôle de la glycémie en réponse à l’ingestion de nutriments est plus rapide.
« Ces résultats sont la preuve que la gastrectomie en manchon et le bypass gastrique, alors qu’ils ont des effets très semblables, sur le diabète n’impliquent pas les mêmes mécanismes, ajoute Maude Le Gall. En même temps, ils révèlent le rôle de l’intestin en tant qu’acteur majeur du contrôle de la glycémie »
Si plus d’études sont nécessaires pour comprendre ces processus, cette découverte profile l’espoir de nouvelles alternatives pour traiter le diabète de type 2 sans passer par la chirurgie.