Une découverte présentée par Raphaël Scharfmann, biologiste Inserm et publiée dans le numéro de septembre de The Journal of Clinical Investigation.
C’est une nouvelle première scientifique ! Des chercheurs de l’Insermet du CNRS viennent de créer des cellules β pancréatiques humaines, ces cellules défectueuses dans les deux types de diabète 1 et 2 et si importantes pour réguler le taux de sucre dans l’organisme. Ces travaux ont été dirigés par Raphael Scharfmann, directeur de recherche Inserm au sein de l’Unité 845 « Centre de recherche Croissance et signalisation » en collaboration avec l’équipe CNRS de Philippe Ravassard du Centre de recherche de l’institut du cerveau et de la moelle épinière (CNRS/UPMC/Inserm)EndoCells, la start-up née de cette collaboration scientifique a permis la production de ces cellules attendues par les chercheurs du monde entier depuis près de 30 ans. Ces résultats sont publiés dans la revue The Journal of Clinical investigation.
Le pancréas est un organe complexe,à la fois site de production d’hormones et acteur de leur libération dans l’organisme.La partie endocrine (productrice d’hormones) du pancréas est composée entreautres, de cellules alpha, et beta qui produisent respectivement du glucagon et de l’insuline, deux hormones qui régulent le taux de sucre dans l’organisme. Ces cellules sont organisées dans le pancréas en ilots, appelés ilots de Langerhans.
La destruction des cellules β productrices d’insuline conduit au diabète de type 1 tandis que la perturbation du fonctionnement de ces cellules conduit au diabète de type 2.Ces maladies touchent plus trois millions de personnes en France. Depuis 30 ans, les chercheurs du monde entier tentent sans succès de reproduire ces cellules β en laboratoire pour les étudier et comprendre leurs dysfonctionnements.
Dans cette nouvelle étude, Raphaël Scharfmann, directeur de recherche à l’Inserm en collaboration avec l’équipe de Philippe Ravassard au CNRS a réussi à générer les premières lignées de cellules bêta pancréatiques humaines fonctionnelles productrices et sécrétrices d’insuline.
Un protocole complexe en plusieurs étapes
Dans un premier temps, un vecteur viral comprenant un gène « immortalisant » sous contrôle d’un promoteur spécifique des cellules β est transféré dans un fragment de pancréas fœtal humain. En d’autres termes, ce vecteur viral peut s’intégrer dans l’ADN de très nombreuses cellules (finalement au hasard), mais le gène immortalisant a la spécificité de ne s’exprimer que dans les cellules β. Ce transfert de gènes assure donc un avantage sélectif aux cellules β qui vont alors se multiplier sans jamais mourir.

© Inserm, F. Koulikoff
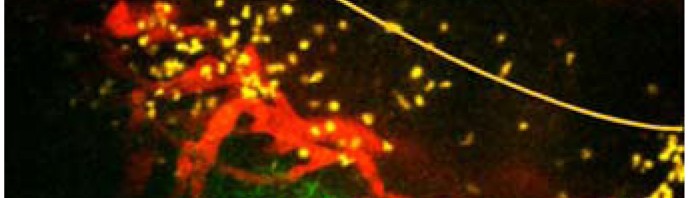
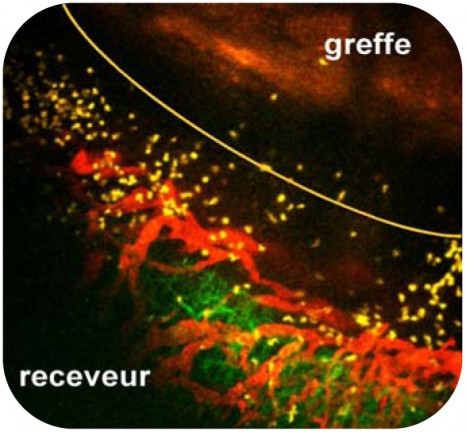
Le tissu pancréatique est ensuite transplanté dans l’organisme d’une souris immunodéficiente (scid) permettant la différenciation et l’amplification des cellules β matures. Après plusieurs mois, la tumeur formée est retirée et dissociée. Les cellules générées sont amplifiées en culture et des lignées de cellules β stables obtenues.
Grâce à ce protocole innovant, les chercheurs ont réussi à obtenir plusieurs lignées. « Certaines d’entre elles ont des propriétés moléculaires et fonctionnelles très proches d’une cellule β humaine adulte. Ces cellules expriment tous les gènes d’une cellule β. Aucune expression significative des autres hormones du pancréas endocrine ni des marqueurs du pancréas exocrine n’a été retrouvée, explique Raphaël Scharfmann, directeur de recherche à l’Inserm ».
Pour tester l’efficacité des cellules ainsi obtenues, les chercheurs les ont ensuite greffées à une souris diabétique chez laquelle elles restaurent alors parfaitement le contrôle de la glycémie indique Philippe Ravassard, co auteur de cette étude.
Grâce à cette découverte, de nombreuses équipes de recherche vont maintenant pouvoir travailler avec ces cellulesβ humainestant attendues et tenter de mieux connaitre leurs propriétés et leur dysfonctionnement ou leur destruction observées dans les diabètes de type 2 et 1.
Ces cellules permettront également derechercher de nouvelles molécules régulant la prolifération et la fonction des cellules β humaines ou d’être utilisées comme modèles précliniques de thérapie cellulaire du diabète.
Bien qu’il reste encore quelques étapes à franchir avant de pouvoir faire de ces cellules un véritable traitement pour les diabétiques, ces travaux représentent une base solide pour la définition de nouvelles approches thérapeutiques des diabètes.