Quand on vous parle de mémoire, vous pensez au cerveau ! Peut-être aussi à notre système immunitaire qui garde en mémoire certaines informations pour réagir de manière plus efficace lorsqu’un virus ou une bactérie nous infecte une deuxième fois. Mais auriez-vous imaginé que nos glandes endocrines se souviennent également de certaines choses ? A l’instar du cerveau, une équipe de chercheurs de l’Inserm et du CNRS dirigée par Patrice Mollard à l’Institut de génomique fonctionnelle (1) (Montpellier) vient de montrer, chez la souris, que les cellules endocrines hypophysaires qui régulent la lactation s’organisent en réseau lors d’un premier allaitement. Ce réseau est alors conservé, comme « mis en mémoire » pour être encore plus opérationnel lors de l’allaitement d’une seconde portée. C’est la première fois qu’une forme de mémoire dans le système endocrinien est mise en évidence. Ces travaux font l’objet d’un article publié dans la revue Nature communications datée du 3 janvier 2012.
La plasticité des systèmes biologiques permet à des organismes de modifier dynamiquement leur physiologie de façon à s’adapter aux conditions environnementales existantes. Au niveau cellulaire, ce processus est associé habituellement au système immunitaire ; au niveau tissulaire, il a été caractérisé il y a plusieurs années dans le cerveau et est au cœur d’une intense recherche en neurobiologie.
En dehors de ces deux systèmes permettant de garder en mémoire des informations à long terme, rien n’indiquait que d’autres cellules pouvaient fonctionner de façon similaire.
L’hypophyse est un organe qui constitue un modèle idéal pour vérifier cette hypothèse car elle comprend des populations distinctes de cellules endocrines organisées en réseaux et qui régulent une multitude de fonctions physiologiques par la sécrétion de différentes hormones.
L’équipe de Patrice Mollard à Montpellier a travaillé avec celle de Paul Le Tissier à Londres (NIMR-MRC (2)) afin de déterminer si les réseaux de cellules endocrines possèdent des capacités de mémorisation. Ils ont pris comme modèle les cellules qui sécrètent la prolactine (l’hormone de la lactation). La sécrétion de prolactine commande un éventail de réponses cruciales pour permettre de nourrir des souriceaux, comprenant la production de lait.
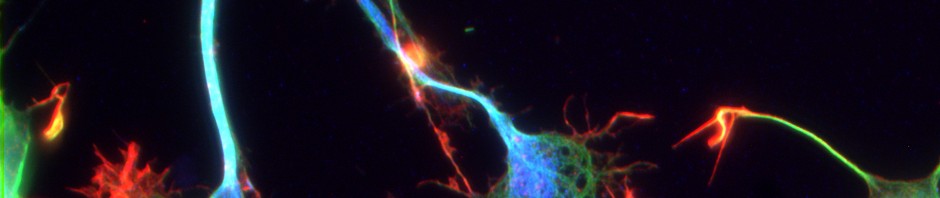
La production de prolactine et donc de lait maternel chez la souris est stimulée d’une part, par la levée d’un signal inhibiteur (dopaminergique) provenant du cerveau et d’autre part, par le phénomène de tétée. Grâce à l’imagerie calcique à deux photons, les chercheurs ont pu distinguer les interactions entre les cellules productrices de prolactine, avant, pendant et après une période d’allaitement.
Avant l’allaitement, ces cellules sont faiblement connectées les unes des autres.
Au moment de l’allaitement, les cellules répondent à la lactation en augmentant la communication intercellulaire coordonnée, la connectivité fonctionnelle et la production tissulaire.
L’originalité de cette découverte réside dans le fait que 3 mois après le sevrage, le réseau reste en place, comme s’il avait été mis en mémoire. « Par la suite, explique Patrice Mollard, un même stimulus (tétée) entraînera une réponse plus coordonnée et plus efficace. Le réseau sécrétera plus de prolactine et provoquera à nouveau un accroissement de la production tissulaire. »
Toutefois cette mise en réseau ne se produit pas si la puissance du stimulus de tétée est réduite. Chez les souris dont les portées sont souvent importantes (8 petits par portée en moyenne), si, seuls 3 petits sont mis à la tétée, le stimulus est trop faible pour déclencher cette mise en réseau.
C’est la première fois que des chercheurs mettent en évidence une forme de mémoire dans un tel système. « Il ouvre un champ des possibilités assez immense. Nous pensons que cette découverte pourrait notamment s’appliquer à d’autres systèmes endocriniens tels que celui des cellules bêta pancréatiques et les cellules endocrines du tractus gastro-intestinal », concluent les auteurs.